Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
PPDPF 通过调节 SOS1 的 GEF 活性促进突变 KRAS 驱动的胰腺导管腺癌的发展
Advanced Science ( IF 14.3 ) Pub Date : 2022-12-01 , DOI: 10.1002/advs.202202448
Qian-Zhi Ni 1, 2 , Bing Zhu 1 , Yan Ji 1 , Qian-Wen Zheng 3 , Xin Liang 1 , Ning Ma 4 , Hao Jiang 5 , Feng-Kun Zhang 1 , Yu-Rong Shang 1 , Yi-Kang Wang 1 , Sheng Xu 1 , Er-Bin Zhang 1 , Yan-Mei Yuan 1 , Tian-Wei Chen 1 , Fen-Fen Yin 1 , Hui-Jun Cao 1 , Jing-Yi Huang 1 , Ji Xia 1 , Xu-Fen Ding 1 , Xiao-Song Qiu 3 , Kai Ding 1 , Chao Song 6 , Wen-Tao Zhou 6 , Meng Wu 7 , Kang Wang 2 , Rui Lui 8 , Qiu Lin 1 , Wei Chen 9 , Zhi-Gang Li 4 , Shu-Qun Cheng 2 , Xiao-Fan Wang 10 , Dong Xie 1, 3, 11 , Jing-Jing Li 1
Affiliation
|
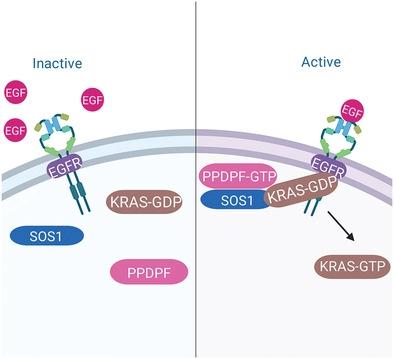
鸟嘌呤核苷酸交换因子 (GEF) SOS1 催化 RAS 上 GDP 交换为 GTP。然而,对 GEF 活动的监管仍然难以捉摸。在这里,作者报告说 PPDPF 是 SOS1 的重要调节因子。 PPDPF在胰腺导管腺癌(PDAC)中的表达显着增加,与PDAC患者的不良预后和复发相关。 PPDPF 的过表达可促进 PDAC 细胞在体外和体内的生长,而 PPDPF 敲除则发挥相反的作用。在 KRAS G12D驱动的 PDAC 遗传小鼠模型中,胰腺特异性 PPDPF 缺失可显着抑制肿瘤的发展。 PPDPF可以结合GTP并将GTP转移到SOS1。 GTP 结合位点的突变严重损害了 PPDPF 的促肿瘤作用。一致的是,介导 SOS1-PPPDF 相互作用的关键氨基酸的突变会显着损害 SOS1 的 GEF 活性。因此,本研究展示了一种通过 PPDPF-SOS1 轴激活 KRAS 的新模型,并为 PDAC 提供了一个有前景的治疗靶点。

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号