当前位置:
X-MOL 学术
›
ACS Pharmacol. Transl. Sci.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Validating the Arrhythmogenic Potential of High-, Intermediate-, and Low-Risk Drugs in a Human-Induced Pluripotent Stem Cell-Derived Cardiac Microphysiological System
ACS Pharmacology & Translational Science ( IF 4.9 ) Pub Date : 2022-07-29 , DOI: 10.1021/acsptsci.2c00088
Verena Charwat 1 , Bérénice Charrez 1 , Brian A Siemons 1 , Henrik Finsberg 2 , Karoline H Jæger 2 , Andrew G Edwards 2 , Nathaniel Huebsch 1 , Samuel Wall 2 , Evan Miller 3 , Aslak Tveito 2 , Kevin E Healy 1, 4
ACS Pharmacology & Translational Science ( IF 4.9 ) Pub Date : 2022-07-29 , DOI: 10.1021/acsptsci.2c00088
Verena Charwat 1 , Bérénice Charrez 1 , Brian A Siemons 1 , Henrik Finsberg 2 , Karoline H Jæger 2 , Andrew G Edwards 2 , Nathaniel Huebsch 1 , Samuel Wall 2 , Evan Miller 3 , Aslak Tveito 2 , Kevin E Healy 1, 4
Affiliation
|
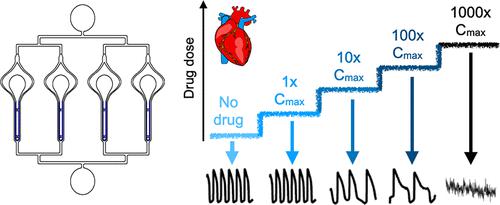
Evaluation of arrhythmogenic drugs is required by regulatory agencies before any new compound can obtain market approval. Despite rigorous review, cardiac disorders remain the second most common cause for safety-related market withdrawal. On the other hand, false-positive preclinical findings prohibit potentially beneficial candidates from moving forward in the development pipeline. Complex in vitro models using cardiomyocytes derived from human-induced pluripotent stem cells (hiPSC-CM) have been identified as a useful tool that allows for rapid and cost-efficient screening of proarrhythmic drug risk. Currently available hiPSC-CM models employ simple two-dimensional (2D) culture formats with limited structural and functional relevance to the human heart muscle. Here, we present the use of our 3D cardiac microphysiological system (MPS), composed of a hiPSC-derived heart micromuscle, as a platform for arrhythmia risk assessment. We employed two different hiPSC lines and tested seven drugs with known ion channel effects and known clinical risk: dofetilide and bepridil (high risk); amiodarone and terfenadine (intermediate risk); and nifedipine, mexiletine, and lidocaine (low risk). The cardiac MPS successfully predicted drug cardiotoxicity risks based on changes in action potential duration, beat waveform (i.e., shape), and occurrence of proarrhythmic events of healthy patient hiPSC lines in the absence of risk cofactors. We showcase examples where the cardiac MPS outperformed existing hiPSC-CM 2D models.
中文翻译:

在人诱导多能干细胞来源的心脏微生理系统中验证高风险、中风险和低风险药物的致心律失常潜力
在任何新化合物获得市场批准之前,监管机构都需要对致心律失常药物进行评估。尽管经过严格审查,心脏病仍然是安全相关市场退出的第二大常见原因。另一方面,假阳性的临床前发现阻碍了潜在有益的候选者在开发过程中取得进展。使用源自人诱导多能干细胞 (hiPSC-CM) 的心肌细胞的复杂体外模型已被确定为一种有用的工具,可以快速且经济高效地筛查致心律失常药物风险。目前可用的 hiPSC-CM 模型采用简单的二维 (2D) 培养形式,与人类心肌的结构和功能相关性有限。在这里,我们展示了使用由 hiPSC 衍生的心脏微肌肉组成的 3D 心脏微生理系统 (MPS) 作为心律失常风险评估的平台。我们采用了两种不同的 hiPSC 系,并测试了七种具有已知离子通道效应和已知临床风险的药物:多非利特和贝普地尔(高风险);胺碘酮和特非那丁(中等风险);以及硝苯地平、美西律和利多卡因(低风险)。心脏 MPS 根据动作电位持续时间、搏动波形(即形状)的变化以及在缺乏风险辅因子的情况下健康患者 hiPSC 系发生致心律失常事件的情况,成功预测了药物心脏毒性风险。我们展示了心脏 MPS 优于现有 hiPSC-CM 2D 模型的示例。
更新日期:2022-07-29
中文翻译:

在人诱导多能干细胞来源的心脏微生理系统中验证高风险、中风险和低风险药物的致心律失常潜力
在任何新化合物获得市场批准之前,监管机构都需要对致心律失常药物进行评估。尽管经过严格审查,心脏病仍然是安全相关市场退出的第二大常见原因。另一方面,假阳性的临床前发现阻碍了潜在有益的候选者在开发过程中取得进展。使用源自人诱导多能干细胞 (hiPSC-CM) 的心肌细胞的复杂体外模型已被确定为一种有用的工具,可以快速且经济高效地筛查致心律失常药物风险。目前可用的 hiPSC-CM 模型采用简单的二维 (2D) 培养形式,与人类心肌的结构和功能相关性有限。在这里,我们展示了使用由 hiPSC 衍生的心脏微肌肉组成的 3D 心脏微生理系统 (MPS) 作为心律失常风险评估的平台。我们采用了两种不同的 hiPSC 系,并测试了七种具有已知离子通道效应和已知临床风险的药物:多非利特和贝普地尔(高风险);胺碘酮和特非那丁(中等风险);以及硝苯地平、美西律和利多卡因(低风险)。心脏 MPS 根据动作电位持续时间、搏动波形(即形状)的变化以及在缺乏风险辅因子的情况下健康患者 hiPSC 系发生致心律失常事件的情况,成功预测了药物心脏毒性风险。我们展示了心脏 MPS 优于现有 hiPSC-CM 2D 模型的示例。































 京公网安备 11010802027423号
京公网安备 11010802027423号