Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Responsive Multivesicular Polymeric Nanovaccines that Codeliver STING Agonists and Neoantigens for Combination Tumor Immunotherapy
Advanced Science ( IF 14.3 ) Pub Date : 2022-06-16 , DOI: 10.1002/advs.202201895 Ting Su 1, 2 , Furong Cheng 2 , Jialong Qi 2 , Yu Zhang 2 , Shurong Zhou 2 , Lei Mei 2 , Shiwei Fu 3, 4 , Fuwu Zhang 3, 4 , Shuibin Lin 1 , Guizhi Zhu 2
Advanced Science ( IF 14.3 ) Pub Date : 2022-06-16 , DOI: 10.1002/advs.202201895 Ting Su 1, 2 , Furong Cheng 2 , Jialong Qi 2 , Yu Zhang 2 , Shurong Zhou 2 , Lei Mei 2 , Shiwei Fu 3, 4 , Fuwu Zhang 3, 4 , Shuibin Lin 1 , Guizhi Zhu 2
Affiliation
|
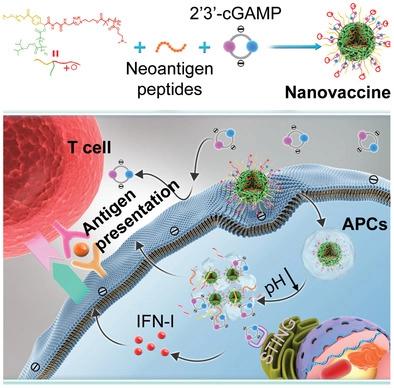
Immune checkpoint blockade (ICB) has significantly advanced cancer immunotherapy, yet its patient response rates are generally low. Vaccines, including immunostimulant-adjuvanted peptide antigens, can improve ICB. The emerging neoantigens generated by cancer somatic mutations elicit cancer-specific immunity for personalized immunotherapy; the novel cyclic dinucleotide (CDN) adjuvants activate stimulator of interferon genes (STING) for antitumor type I interferon (IFN-I) responses. However, CDN/neoantigen vaccine development has been limited by the poor antigen/adjuvant codelivery. Here, pH-responsive CDN/neoantigen codelivering nanovaccines (NVs) for ICB combination tumor immunotherapy are reported. pH-responsive polymers are synthesized to be self-assembled into multivesicular nanoparticles (NPs) at physiological pH and disassembled at acidic conditions. NPs with high CDN/antigen coloading are selected as NVs for CDN/antigen codelivery to antigen presenting cells (APCs) in immunomodulatory lymph nodes (LNs). In the acidic endosome of APCs, pH-responsive NVs facilitate the vaccine release and escape into cytosol, where CDNs activate STING for IFN-I responses and antigens are presented by major histocompatibility complex (MHC) for T-cell priming. In mice, NVs elicit potent antigen-specific CD8+ T-cell responses with immune memory, and reduce multifaceted tumor immunosuppression. In syngeneic murine tumors, NVs show robust ICB combination therapeutic efficacy. Overall, these CDN/neoantigen-codelivering NVs hold the potential for ICB combination tumor immunotherapy.
中文翻译:

Codeliver STING 激动剂和新抗原的响应性多囊聚合物纳米疫苗用于组合肿瘤免疫治疗
免疫检查点阻断(ICB)显着提高了癌症免疫治疗的进展,但其患者反应率普遍较低。疫苗,包括免疫刺激剂佐剂的肽抗原,可以改善 ICB。癌症体细胞突变产生的新兴新抗原可引发癌症特异性免疫,用于个性化免疫治疗;新型环状二核苷酸 (CDN) 佐剂可激活干扰素基因刺激剂 (STING),以产生抗肿瘤 I 型干扰素 (IFN-I) 反应。然而,CDN/新抗原疫苗的开发因抗原/佐剂共传递较差而受到限制。在此,报道了用于 ICB 联合肿瘤免疫治疗的 pH 响应 CDN/新抗原共传递纳米疫苗 (NV)。 pH 响应聚合物被合成,在生理 pH 下自组装成多囊纳米颗粒 (NP),并在酸性条件下分解。选择具有高 CDN/抗原共负载的 NP 作为 NV,将 CDN/抗原共同递送至免疫调节淋巴结 (LN) 中的抗原呈递细胞 (APC)。在 APC 的酸性内体中,pH 响应性 NV 促进疫苗释放并逃入细胞质,其中 CDN 激活 STING 进行 IFN-I 反应,并且主要组织相容性复合体 (MHC) 呈递抗原以启动 T 细胞。在小鼠中,NVs 引发具有免疫记忆的有效抗原特异性 CD8 + T 细胞反应,并减少多方面的肿瘤免疫抑制。在同基因小鼠肿瘤中,NVs 显示出强大的 ICB 联合治疗功效。总体而言,这些 CDN/新抗原共传递 NV 具有 ICB 联合肿瘤免疫治疗的潜力。
更新日期:2022-06-16
中文翻译:

Codeliver STING 激动剂和新抗原的响应性多囊聚合物纳米疫苗用于组合肿瘤免疫治疗
免疫检查点阻断(ICB)显着提高了癌症免疫治疗的进展,但其患者反应率普遍较低。疫苗,包括免疫刺激剂佐剂的肽抗原,可以改善 ICB。癌症体细胞突变产生的新兴新抗原可引发癌症特异性免疫,用于个性化免疫治疗;新型环状二核苷酸 (CDN) 佐剂可激活干扰素基因刺激剂 (STING),以产生抗肿瘤 I 型干扰素 (IFN-I) 反应。然而,CDN/新抗原疫苗的开发因抗原/佐剂共传递较差而受到限制。在此,报道了用于 ICB 联合肿瘤免疫治疗的 pH 响应 CDN/新抗原共传递纳米疫苗 (NV)。 pH 响应聚合物被合成,在生理 pH 下自组装成多囊纳米颗粒 (NP),并在酸性条件下分解。选择具有高 CDN/抗原共负载的 NP 作为 NV,将 CDN/抗原共同递送至免疫调节淋巴结 (LN) 中的抗原呈递细胞 (APC)。在 APC 的酸性内体中,pH 响应性 NV 促进疫苗释放并逃入细胞质,其中 CDN 激活 STING 进行 IFN-I 反应,并且主要组织相容性复合体 (MHC) 呈递抗原以启动 T 细胞。在小鼠中,NVs 引发具有免疫记忆的有效抗原特异性 CD8 + T 细胞反应,并减少多方面的肿瘤免疫抑制。在同基因小鼠肿瘤中,NVs 显示出强大的 ICB 联合治疗功效。总体而言,这些 CDN/新抗原共传递 NV 具有 ICB 联合肿瘤免疫治疗的潜力。






























 京公网安备 11010802027423号
京公网安备 11010802027423号