当前位置:
X-MOL 学术
›
Anal. Chem.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Real-Time Detection of ESR1 Mutation in Blood by Droplet Digital PCR in the PADA-1 Trial: Feasibility and Cross-Validation with NGS
Analytical Chemistry ( IF 6.7 ) Pub Date : 2022-04-13 , DOI: 10.1021/acs.analchem.2c00446
Celine Callens 1 , Francois-Clement Bidard 2, 3 , Anaïs Curto-Taribo 1 , Olfa Trabelsi-Grati 1 , Samia Melaabi 1 , Suzette Delaloge 4 , Anne-Claire Hardy-Bessard 5 , Thomas Bachelot 6 , Florian Clatot 7 , Thibault De La Motte Rouge 8 , Jean-Luc Canon 9 , Laurent Arnould 10 , Fabrice Andre 4 , Sandrine Marques 11 , Marc-Henri Stern 12 , Jean-Yves Pierga 3, 13 , Anne Vincent-Salomon 14 , Camille Benoist 15 , Emmanuelle Jeannot 1 , Frederique Berger 16 , Ivan Bieche 1 , Anne Pradines 17, 18
Analytical Chemistry ( IF 6.7 ) Pub Date : 2022-04-13 , DOI: 10.1021/acs.analchem.2c00446
Celine Callens 1 , Francois-Clement Bidard 2, 3 , Anaïs Curto-Taribo 1 , Olfa Trabelsi-Grati 1 , Samia Melaabi 1 , Suzette Delaloge 4 , Anne-Claire Hardy-Bessard 5 , Thomas Bachelot 6 , Florian Clatot 7 , Thibault De La Motte Rouge 8 , Jean-Luc Canon 9 , Laurent Arnould 10 , Fabrice Andre 4 , Sandrine Marques 11 , Marc-Henri Stern 12 , Jean-Yves Pierga 3, 13 , Anne Vincent-Salomon 14 , Camille Benoist 15 , Emmanuelle Jeannot 1 , Frederique Berger 16 , Ivan Bieche 1 , Anne Pradines 17, 18
Affiliation
|
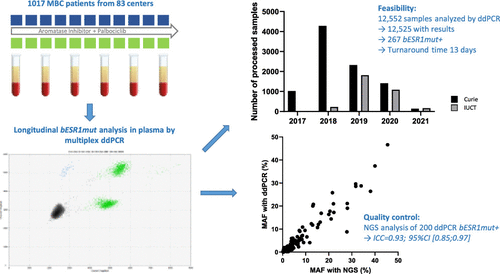
The clinical actionability of circulating tumor DNA requires sensitive detection methods with a short turnaround time. In the PADA-1 phase 3 trial (NCT03079011), metastatic breast cancer patients treated with an aromatase inhibitor and palbociclib were screened every 2 months for activating ESR1 mutations in blood (bESR1mut). We report the feasibility of the droplet digital polymerase chain reaction (ddPCR) and cross-validation with next-generation sequencing (NGS). bESR1mut testing was centralized in two platforms using the same ddPCR assay. Results were reported as copies/mL of plasma and mutant allele frequency (MAF). We analyzed 200 positive ddPCR samples with an NGS assay (0.5–1% sensitivity). Overall, 12,552 blood samples were collected from 1017 patients from 83 centers. Among the 12,525 available samples with ddPCR results, 11,533 (92%) were bESR1mut-negative. A total of 267 patients newly displayed bESR1mut (26% patients/2% samples) with a median copy number of 14/mL (range: 4–1225) and a median MAF of 0.83% (0.11–35), 648 samples (20% patients/5% samples) displayed persistent bESR1mut, and 77 (<1%) samples encountered a technical failure. The median turnaround time from blood drawing to result notification was 13 days (Q1:9; Q3:21 days). Among 200 ddPCR-positive samples tested, NGS detected bESR1mut in 168 (84%); 25 of the 32 cases missed by NGS had low MAF and/or low coverage. In these 200 samples, bESR1mut MAF by both techniques had an excellent intraclass correlation coefficient (ICC = 0.93; 95% CI [0.85; 0.97]). These results from a large-scale trial support the feasibility and accuracy of real-time bESR1mut tracking by ddPCR, opening new opportunities for therapeutic interventions.
中文翻译:

在 PADA-1 试验中通过液滴数字 PCR 实时检测血液中的 ESR1 突变:与 NGS 的可行性和交叉验证,在 PADA-1 试验中通过液滴数字 PCR 实时检测血液中的 ESR1 突变:与 NGS 的可行性和交叉验证
循环肿瘤 DNA 的临床可操作性需要灵敏的检测方法和较短的周转时间。在 PADA-1 3 期试验 (NCT03079011) 中,每 2 个月对接受芳香化酶抑制剂和 palbociclib 治疗的转移性乳腺癌患者进行筛查,以检测其激活血液中的ESR1突变 ( bESR1 mut )。我们报告了液滴数字聚合酶链反应 (ddPCR) 和与下一代测序 (NGS) 交叉验证的可行性。bESR1突变测试集中在两个平台上,使用相同的 ddPCR 分析。结果报告为血浆拷贝数/mL 和突变等位基因频率 (MAF)。我们用 NGS 检测分析了 200 个阳性 ddPCR 样本(灵敏度为 0.5-1%)。总体而言,从 83 个中心的 1017 名患者中收集了 12,552 份血液样本。在具有 ddPCR 结果的 12,525 个可用样本中,11,533 个(92%)是bESR1 mut阴性。共有 267 名患者新显示bESR1 mut(26% 患者/2% 样本),中位拷贝数为 14/mL(范围:4-1225),中位 MAF 为 0.83%(0.11-35),648 个样本( 20% 患者/5% 样本)显示出持续的 bESR1 mut,并且 77 个 (<1%) 样品遇到了技术故障。从抽血到结果通知的中位周转时间为 13 天(Q1:9;Q3:21 天)。在检测的 200 个 ddPCR 阳性样本中,NGS在 168 个(84%)中检测到bESR1 mut ;NGS 遗漏的 32 例病例中有 25 例 MAF 低和/或覆盖率低。在这 200 个样本中,两种技术的bESR1 mut MAF 具有出色的组内相关系数(ICC = 0.93;95% CI [0.85;0.97])。这些来自大规模试验的结果支持了 ddPCR 实时bESR1 mut跟踪的可行性和准确性,为治疗干预开辟了新的机会。,循环肿瘤 DNA 的临床可操作性需要灵敏的检测方法和较短的周转时间。在 PADA-1 3 期试验 (NCT03079011) 中,每 2 个月对接受芳香化酶抑制剂和 palbociclib 治疗的转移性乳腺癌患者进行筛查,以检测其激活血液中的ESR1突变 ( bESR1 mut )。我们报告了液滴数字聚合酶链反应 (ddPCR) 和与下一代测序 (NGS) 交叉验证的可行性。bESR1突变测试集中在两个平台上,使用相同的 ddPCR 分析。结果报告为血浆拷贝数/mL 和突变等位基因频率 (MAF)。我们用 NGS 检测分析了 200 个阳性 ddPCR 样本(灵敏度为 0.5-1%)。总体而言,从 83 个中心的 1017 名患者中收集了 12,552 份血液样本。在具有 ddPCR 结果的 12,525 个可用样本中,11,533 个(92%)是bESR1 mut阴性。共有 267 名患者新显示bESR1 mut(26% 患者/2% 样本),中位拷贝数为 14/mL(范围:4-1225),中位 MAF 为 0.83%(0.11-35),648 个样本( 20% 患者/5% 样本)显示出持续的 bESR1 mut,并且 77 个 (<1%) 样品遇到了技术故障。从抽血到结果通知的中位周转时间为 13 天(Q1:9;Q3:21 天)。在检测的 200 个 ddPCR 阳性样本中,NGS在 168 个(84%)中检测到bESR1 mut ;NGS 遗漏的 32 例病例中有 25 例 MAF 低和/或覆盖率低。在这 200 个样本中,两种技术的bESR1 mut MAF 具有出色的组内相关系数(ICC = 0.93;95% CI [0.85;0.97])。这些来自大规模试验的结果支持了 ddPCR 实时bESR1 mut跟踪的可行性和准确性,为治疗干预开辟了新的机会。
更新日期:2022-04-13
中文翻译:

在 PADA-1 试验中通过液滴数字 PCR 实时检测血液中的 ESR1 突变:与 NGS 的可行性和交叉验证,在 PADA-1 试验中通过液滴数字 PCR 实时检测血液中的 ESR1 突变:与 NGS 的可行性和交叉验证
循环肿瘤 DNA 的临床可操作性需要灵敏的检测方法和较短的周转时间。在 PADA-1 3 期试验 (NCT03079011) 中,每 2 个月对接受芳香化酶抑制剂和 palbociclib 治疗的转移性乳腺癌患者进行筛查,以检测其激活血液中的ESR1突变 ( bESR1 mut )。我们报告了液滴数字聚合酶链反应 (ddPCR) 和与下一代测序 (NGS) 交叉验证的可行性。bESR1突变测试集中在两个平台上,使用相同的 ddPCR 分析。结果报告为血浆拷贝数/mL 和突变等位基因频率 (MAF)。我们用 NGS 检测分析了 200 个阳性 ddPCR 样本(灵敏度为 0.5-1%)。总体而言,从 83 个中心的 1017 名患者中收集了 12,552 份血液样本。在具有 ddPCR 结果的 12,525 个可用样本中,11,533 个(92%)是bESR1 mut阴性。共有 267 名患者新显示bESR1 mut(26% 患者/2% 样本),中位拷贝数为 14/mL(范围:4-1225),中位 MAF 为 0.83%(0.11-35),648 个样本( 20% 患者/5% 样本)显示出持续的 bESR1 mut,并且 77 个 (<1%) 样品遇到了技术故障。从抽血到结果通知的中位周转时间为 13 天(Q1:9;Q3:21 天)。在检测的 200 个 ddPCR 阳性样本中,NGS在 168 个(84%)中检测到bESR1 mut ;NGS 遗漏的 32 例病例中有 25 例 MAF 低和/或覆盖率低。在这 200 个样本中,两种技术的bESR1 mut MAF 具有出色的组内相关系数(ICC = 0.93;95% CI [0.85;0.97])。这些来自大规模试验的结果支持了 ddPCR 实时bESR1 mut跟踪的可行性和准确性,为治疗干预开辟了新的机会。,循环肿瘤 DNA 的临床可操作性需要灵敏的检测方法和较短的周转时间。在 PADA-1 3 期试验 (NCT03079011) 中,每 2 个月对接受芳香化酶抑制剂和 palbociclib 治疗的转移性乳腺癌患者进行筛查,以检测其激活血液中的ESR1突变 ( bESR1 mut )。我们报告了液滴数字聚合酶链反应 (ddPCR) 和与下一代测序 (NGS) 交叉验证的可行性。bESR1突变测试集中在两个平台上,使用相同的 ddPCR 分析。结果报告为血浆拷贝数/mL 和突变等位基因频率 (MAF)。我们用 NGS 检测分析了 200 个阳性 ddPCR 样本(灵敏度为 0.5-1%)。总体而言,从 83 个中心的 1017 名患者中收集了 12,552 份血液样本。在具有 ddPCR 结果的 12,525 个可用样本中,11,533 个(92%)是bESR1 mut阴性。共有 267 名患者新显示bESR1 mut(26% 患者/2% 样本),中位拷贝数为 14/mL(范围:4-1225),中位 MAF 为 0.83%(0.11-35),648 个样本( 20% 患者/5% 样本)显示出持续的 bESR1 mut,并且 77 个 (<1%) 样品遇到了技术故障。从抽血到结果通知的中位周转时间为 13 天(Q1:9;Q3:21 天)。在检测的 200 个 ddPCR 阳性样本中,NGS在 168 个(84%)中检测到bESR1 mut ;NGS 遗漏的 32 例病例中有 25 例 MAF 低和/或覆盖率低。在这 200 个样本中,两种技术的bESR1 mut MAF 具有出色的组内相关系数(ICC = 0.93;95% CI [0.85;0.97])。这些来自大规模试验的结果支持了 ddPCR 实时bESR1 mut跟踪的可行性和准确性,为治疗干预开辟了新的机会。

































 京公网安备 11010802027423号
京公网安备 11010802027423号