当前位置:
X-MOL 学术
›
ACS Appl. Mater. Interfaces
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
CeO2 中 pH 驱动的仿生行为的生物催化机制的密度泛函理论研究
ACS Applied Materials & Interfaces ( IF 8.3 ) Pub Date : 2022-03-01 , DOI: 10.1021/acsami.1c24686
Hongyang Ma 1 , Zhao Liu 2 , Pramod Koshy 1 , Charles C Sorrell 1 , Judy N Hart 1
ACS Applied Materials & Interfaces ( IF 8.3 ) Pub Date : 2022-03-01 , DOI: 10.1021/acsami.1c24686
Hongyang Ma 1 , Zhao Liu 2 , Pramod Koshy 1 , Charles C Sorrell 1 , Judy N Hart 1
Affiliation
|
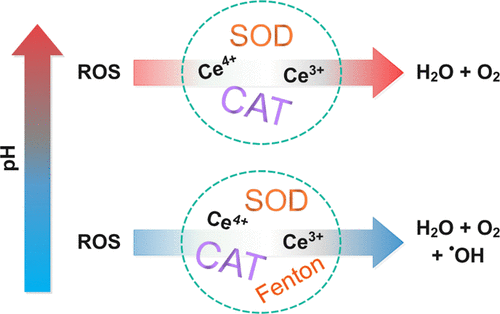
氧化铈 (CeO 2 ) 纳米粒子在生物医学中的 pH 依赖性、可切换、生物催化特性引起了相当大的兴趣,其中这些材料在碱性生理 pH 值下表现出对活性氧 (ROS) 的有益抗氧化活性,但在生理 pH 值下表现出细胞毒性促氧化活性。酸性癌细胞pH微环境。虽然氧空位作用的一般特征是已知的,但它们在不同 pH 条件下在原子尺度上的作用机制尚未阐明。目前的工作应用密度泛函理论 (DFT) 计算在原子尺度上解释 CeO 2稳定 {111} 表面的 pH 诱导行为含有氧空位。对表面吸附介质种类的分析揭示了 pH 值对 ROS( • O 2 –和 H 2 O 2)与有缺陷的 CeO 2 {111} 表面之间相互作用的关键作用。在碱性条件下,超氧化物歧化酶(SOD)和过氧化氢酶(CAT)的仿生反应可以循环进行,清除并分解活性氧为无害产物,使CeO 2成为一种优良的抗氧化剂。然而,在酸性条件下,由于 Ce 3+ ↔ Ce 4+的有限可逆性和氧空位的形成 ↔ 湮灭,CAT 仿生反应受到阻碍。芬顿仿生反应(H2 O 2 + Ce 3+ → Ce 4+ + OH – + • OH) 预计与SOD和CAT仿生反应同时发生,导致羟基自由基的形成,使CeO 2成为细胞毒性促氧化剂。

"点击查看英文标题和摘要"
更新日期:2022-03-01

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号