当前位置:
X-MOL 学术
›
J. Am. Chem. Soc.
›
论文详情
Our official English website, www.x-mol.net, welcomes your feedback! (Note: you will need to create a separate account there.)
铜基金属-有机框架通过系统性破坏动态平衡的细胞氧化还原稳态来克服癌症化学抗性
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2022-02-22 , DOI: 10.1021/jacs.1c11856 Jia Liu 1 , Ye Yuan 1, 2 , Yanni Cheng 1 , Daan Fu 1, 2 , Zhongyin Chen 1 , Yang Wang 1 , Lifang Zhang 1 , Chundong Yao 1 , Lin Shi 1 , Mingyi Li 1 , Cheng Zhou 1, 2 , Meizhen Zou 3 , Guobin Wang 2 , Lin Wang 1, 3 , Zheng Wang 1, 2
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2022-02-22 , DOI: 10.1021/jacs.1c11856 Jia Liu 1 , Ye Yuan 1, 2 , Yanni Cheng 1 , Daan Fu 1, 2 , Zhongyin Chen 1 , Yang Wang 1 , Lifang Zhang 1 , Chundong Yao 1 , Lin Shi 1 , Mingyi Li 1 , Cheng Zhou 1, 2 , Meizhen Zou 3 , Guobin Wang 2 , Lin Wang 1, 3 , Zheng Wang 1, 2
Affiliation
|
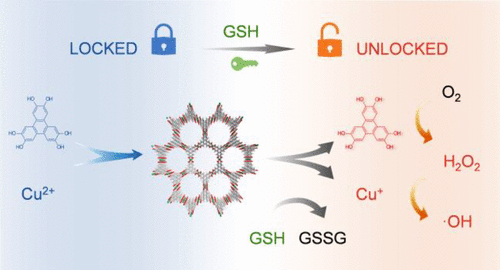
化疗耐药是肿瘤复发的主要原因。鉴于化学药物耐药性的机制复杂性,分子抑制剂和靶向药物通常无法消除耐药癌细胞,有时甚至通过激活替代途径来促进化学耐药性。在这里,通过利用耐药癌细胞中高水平但动态平衡的细胞氧化还原稳态的生化脆弱性,我们设计了一种纳米铜/儿茶酚基金属有机框架 (CuHPT),它有效地扰乱了这种平衡,使平衡向氧化应激倾斜. 在耐药细胞内,CuHPT 开始分解,这是由细胞谷胱甘肽 (GSH) 的持续消耗触发的。CuHPT 解体同时释放两种结构元素:儿茶酚配体和还原性铜离子(Cu+ )。它们两者协同作用,通过自氧化和通过耗尽 GSH 的类芬顿反应来放大细胞内自由基氧化物质 (ROS) 的产生。通过显着提高细胞氧化应激,CuHPT 对多种耐药癌细胞表现出选择性和有效的细胞毒性。重要的是,CuHPT 可有效抑制体内耐药性肿瘤的生长,并使荷瘤小鼠的存活时间加倍。因此,除了 CuHPT 良好的生物相容性外,我们的生化、细胞生物学、临床前动物模型数据提供了令人信服的证据,支持这种基于铜的 MOF 是一种预先设计的智能疗法,可通过精确解构其氧化还原稳态来对抗耐药性癌症。

"点击查看英文标题和摘要"
更新日期:2022-02-22

"点击查看英文标题和摘要"











































 京公网安备 11010802027423号
京公网安备 11010802027423号