当前位置:
X-MOL 学术
›
J. Am. Chem. Soc.
›
论文详情
Our official English website, www.x-mol.net, welcomes your feedback! (Note: you will need to create a separate account there.)
Chemical Protein Synthesis Using a Second-GenerationN-Acylurea Linker for the Preparation of Peptide-Thioester Precursors
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2015-06-02 , DOI: 10.1021/jacs.5b03504 Juan B. Blanco-Canosa , Brunello Nardone 1 , Fernando Albericio 2 , Philip E. Dawson 3
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2015-06-02 , DOI: 10.1021/jacs.5b03504 Juan B. Blanco-Canosa , Brunello Nardone 1 , Fernando Albericio 2 , Philip E. Dawson 3
Affiliation
|
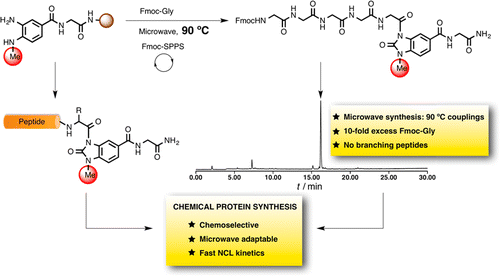
The broad utility of native chemical ligation (NCL) in protein synthesis has fostered a search for methods that enable the efficient synthesis of C-terminal peptide-thioesters, key intermediates in NCL. We have developed an N-acylurea (Nbz) approach for the synthesis of thioester peptide precursors that efficiently undergo thiol exchange yielding thioester peptides and subsequently NCL reaction. However, the synthesis of some glycine-rich sequences revealed limitations, such as diacylated products that can not be converted into N-acylurea peptides. Here, we introduce a new N-acylurea linker bearing an o-amino(methyl)aniline (MeDbz) moiety that enables in a more robust peptide chain assembly. The generality of the approach is illustrated by the synthesis of a pentaglycine sequence under different coupling conditions including microwave heating at coupling temperatures up to 90 C, affording the unique and desired N-acyl-N'-methylacylurea (MeNbz) product. Further extension of the method allowed the synthesis of all 20 natural amino acids and their NCL reactions. The kinetic analysis of the ligations using model peptides shows the MeNbz peptide rapidly converts to arylthioesters that are efficient at NCL. Finally, we show that the new MeDbz linker can be applied to the synthesis of cysteine-rich proteins such the cyclotides Kalata B1 and MCoTI-II through a one cyclization/folding step in the ligation/folding buffer.
中文翻译:

使用第二代 N-酰基脲接头制备肽-硫酯前体的化学蛋白质合成
天然化学连接 (NCL) 在蛋白质合成中的广泛应用促进了对能够有效合成 C 端肽硫酯(NCL 中的关键中间体)的方法的探索。我们开发了一种 N-酰基脲 (Nbz) 方法,用于合成硫酯肽前体,该方法有效地进行硫醇交换,产生硫酯肽,随后发生 NCL 反应。然而,一些富含甘氨酸的序列的合成显示出局限性,例如不能转化为 N-酰基脲肽的二酰化产物。在这里,我们引入了一种带有邻氨基(甲基)苯胺 (MeDbz) 部分的新 N-酰基脲链接器,可实现更强大的肽链组装。该方法的通用性通过在不同偶联条件下合成五甘氨酸序列来说明,包括在偶联温度高达 90°C 的微波加热,提供独特且所需的 N-酰基-N'-甲基酰脲 (MeNbz) 产品。该方法的进一步扩展允许合成所有 20 种天然氨基酸及其 NCL 反应。使用模型肽对连接进行的动力学分析显示 MeNbz 肽快速转化为在 NCL 中有效的芳硫酯。最后,我们表明新的 MeDbz 接头可以通过连接/折叠缓冲液中的一个环化/折叠步骤应用于富含半胱氨酸的蛋白质的合成,例如环肽 Kalata B1 和 MCoTI-II。该方法的进一步扩展允许合成所有 20 种天然氨基酸及其 NCL 反应。使用模型肽对连接进行的动力学分析显示 MeNbz 肽快速转化为在 NCL 中有效的芳硫酯。最后,我们表明新的 MeDbz 接头可以通过连接/折叠缓冲液中的一个环化/折叠步骤应用于富含半胱氨酸的蛋白质的合成,例如环肽 Kalata B1 和 MCoTI-II。该方法的进一步扩展允许合成所有 20 种天然氨基酸及其 NCL 反应。使用模型肽对连接进行的动力学分析显示 MeNbz 肽快速转化为在 NCL 中有效的芳硫酯。最后,我们表明新的 MeDbz 接头可以通过连接/折叠缓冲液中的一个环化/折叠步骤应用于富含半胱氨酸的蛋白质的合成,例如环肽 Kalata B1 和 MCoTI-II。
更新日期:2015-06-02
中文翻译:

使用第二代 N-酰基脲接头制备肽-硫酯前体的化学蛋白质合成
天然化学连接 (NCL) 在蛋白质合成中的广泛应用促进了对能够有效合成 C 端肽硫酯(NCL 中的关键中间体)的方法的探索。我们开发了一种 N-酰基脲 (Nbz) 方法,用于合成硫酯肽前体,该方法有效地进行硫醇交换,产生硫酯肽,随后发生 NCL 反应。然而,一些富含甘氨酸的序列的合成显示出局限性,例如不能转化为 N-酰基脲肽的二酰化产物。在这里,我们引入了一种带有邻氨基(甲基)苯胺 (MeDbz) 部分的新 N-酰基脲链接器,可实现更强大的肽链组装。该方法的通用性通过在不同偶联条件下合成五甘氨酸序列来说明,包括在偶联温度高达 90°C 的微波加热,提供独特且所需的 N-酰基-N'-甲基酰脲 (MeNbz) 产品。该方法的进一步扩展允许合成所有 20 种天然氨基酸及其 NCL 反应。使用模型肽对连接进行的动力学分析显示 MeNbz 肽快速转化为在 NCL 中有效的芳硫酯。最后,我们表明新的 MeDbz 接头可以通过连接/折叠缓冲液中的一个环化/折叠步骤应用于富含半胱氨酸的蛋白质的合成,例如环肽 Kalata B1 和 MCoTI-II。该方法的进一步扩展允许合成所有 20 种天然氨基酸及其 NCL 反应。使用模型肽对连接进行的动力学分析显示 MeNbz 肽快速转化为在 NCL 中有效的芳硫酯。最后,我们表明新的 MeDbz 接头可以通过连接/折叠缓冲液中的一个环化/折叠步骤应用于富含半胱氨酸的蛋白质的合成,例如环肽 Kalata B1 和 MCoTI-II。该方法的进一步扩展允许合成所有 20 种天然氨基酸及其 NCL 反应。使用模型肽对连接进行的动力学分析显示 MeNbz 肽快速转化为在 NCL 中有效的芳硫酯。最后,我们表明新的 MeDbz 接头可以通过连接/折叠缓冲液中的一个环化/折叠步骤应用于富含半胱氨酸的蛋白质的合成,例如环肽 Kalata B1 和 MCoTI-II。















































 京公网安备 11010802027423号
京公网安备 11010802027423号