当前位置:
X-MOL 学术
›
J. Neurochem.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
大鼠纹状体放射性标记乙酰胆碱合成和释放的评价
Journal of Neurochemistry ( IF 4.2 ) Pub Date : 2021-12-08 , DOI: 10.1111/jnc.15556 Ikunobu Muramatsu 1 , Junsuke Uwada 1 , Kazuyasu Chihara 2 , Kiyonao Sada 2 , Mao-Hsien Wang 2 , Takashi Yazawa 3 , Takanobu Taniguchi 3 , Takaharu Ishibashi 1 , Takayoshi Masuoka 1
Journal of Neurochemistry ( IF 4.2 ) Pub Date : 2021-12-08 , DOI: 10.1111/jnc.15556 Ikunobu Muramatsu 1 , Junsuke Uwada 1 , Kazuyasu Chihara 2 , Kiyonao Sada 2 , Mao-Hsien Wang 2 , Takashi Yazawa 3 , Takanobu Taniguchi 3 , Takaharu Ishibashi 1 , Takayoshi Masuoka 1
Affiliation
|
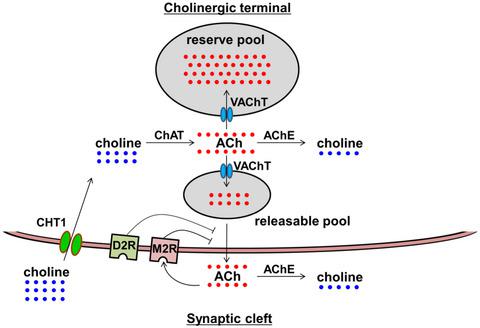
胆碱能传递是认知和运动等高级大脑功能的基础。为了阐明在中枢神经系统中维持和调节乙酰胆碱 (ACh) 释放的过程,研究了大鼠纹状体节段中 [ 3 H] 胆碱的摄取以及 [ 3 H] ACh 的随后合成和释放。与 [ 3 H] 胆碱一起孵育可通过高亲和力胆碱转运蛋白 1 引发有效吸收,从而导致 [ 3 H] 胆碱和 [ 3 H]ACh 的积累。然而,在抑制 ACh 酯酶 (AChE) 后,与 [ 3 H] 胆碱孵育主要导致 [ 3H]乙酰胆碱。电刺激和 KCl 去极化选择性地释放 [ 3 H]ACh 而不是 [ 3 H]胆碱。[ 3 H]ACh 释放在重复刺激后逐渐下降,而在 AChE 抑制下释放可重现。[ 3 H]ACh 释放在用 vesamicol(一种囊泡 ACh 转运蛋白抑制剂)处理后被消除。这些结果表明,可释放的乙酰胆碱不断从细胞质中补充到可释放的胆碱能囊泡池中,以维持胆碱能传递。河豚毒素消除了电刺激引起的[ 3 H]ACh释放,而KCl诱导的[ 3 H]ACh释放在很大程度上具有抗性。ACh 释放量为 Ca 2+依赖于两种刺激之间的对 N 型和 P 型 Ca 2+通道毒素(分别为 ω-芋螺毒素 GVIA 和 ω-agatoxin IVA)的敏感性并表现出略微不同的敏感性。[ 3 H]ACh 释放受 M2 毒蕈碱和 D2 多巴胺能受体的负调控。目前的结果表明,抑制胆碱能神经元内的 AChE 和抑制 ACh 释放的突触前负调节有助于维持和促进胆碱能传递,为胆碱能功能障碍相关疾病的治疗开发提供潜在有用的线索,除了抑制突触间隙 AChE。

"点击查看英文标题和摘要"
更新日期:2022-01-20

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号