当前位置:
X-MOL 学术
›
Nano Lett.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
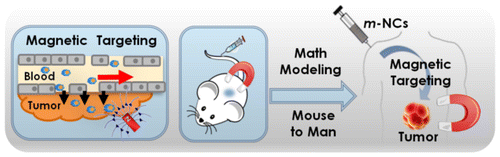
磁性药物靶向:临床前体内研究、数学建模以及对人类的外推
Nano Letters ( IF 9.6 ) Pub Date : 2016-08-19 00:00:00 , DOI: 10.1021/acs.nanolett.6b02261
Khuloud T Al-Jamal , Jie Bai , Julie Tzu-Wen Wang , Andrea Protti 1 , Paul Southern 2 , Lara Bogart 2 , Hamed Heidari 3 , Xinjia Li , Andrew Cakebread , Dan Asker , Wafa T Al-Jamal 4 , Ajay Shah 1 , Sara Bals 3 , Jane Sosabowski , Quentin A Pankhurst 2
Affiliation
|
设计能够在静脉注射后在体内进行磁性捕获的磁性纳米载体的合理理论基础可以帮助阐明体内磁性肿瘤靶向所需的参数。在这项工作中,我们利用长循环聚合物磁性纳米载体,将越来越多的超顺磁性氧化铁纳米粒子(SPION)封装在生物相容性油载体中,以研究 SPION 负载和施加的磁场强度对 CT26 中磁性肿瘤靶向的影响荷瘤小鼠。在受控条件下,对体内磁靶向进行了量化,发现其与 SPION 负载和磁场强度成正比。然而,最高的 SPION 负载会导致血液循环时间减少和磁性靶向趋于稳定。根据 Nacev-Shapiro 结构,采用数学模型来计算作用在纳米胶囊 (NC) 上的体内磁力、粘弹性力、对流力和扩散力,然后将其用于推断人类的预期行为。该模型预测,在后一种情况下,此处应用的数控和磁力足以成功实现对人类的靶向。最后,使用多西他赛 (DTX) 封装的 NC 进行体内小鼠肿瘤生长延迟研究。研究发现,与被动靶向药物剂量相比,磁靶向可提供增强的治疗效果并提高小鼠的存活率。 5–8 毫克 DTX/kg。据我们所知,这是第一项真正弥合磁性药物靶向领域临床前实验和临床转化之间差距的研究。

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号