当前位置:
X-MOL 学术
›
Eur. J. Med. Chem.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
2-acetamido-2-deoxy-d-glucono-1,5-lactonesemicarbazone 衍生物对人 OGA 的纳摩尔抑制
European Journal of Medicinal Chemistry ( IF 6.0 ) Pub Date : 2021-06-15 , DOI: 10.1016/j.ejmech.2021.113649 Mariann Kiss 1 , Erna Szabó 2 , Boglárka Bocska 1 , Luu Thanh Sinh 2 , Conceicao Piedade Fernandes 3 , István Timári 1 , Joseph M Hayes 3 , László Somsák 1 , Teréz Barna 2

"点击查看英文标题和摘要"
更新日期:2021-06-28
European Journal of Medicinal Chemistry ( IF 6.0 ) Pub Date : 2021-06-15 , DOI: 10.1016/j.ejmech.2021.113649 Mariann Kiss 1 , Erna Szabó 2 , Boglárka Bocska 1 , Luu Thanh Sinh 2 , Conceicao Piedade Fernandes 3 , István Timári 1 , Joseph M Hayes 3 , László Somsák 1 , Teréz Barna 2
Affiliation
|
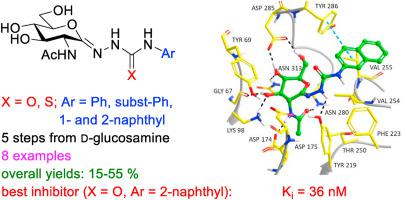
Ó -GlcNAcylation是通过介导的动态翻译后修饰ø -连接的β- Ñ乙酰氨基葡萄糖转移酶(OGT)和Ô -GlcNAc水解酶(OGA),即添加或删除单个β- Ñ乙酰氨基葡萄糖(GlcNAc的)部分或分别来自核细胞溶质和线粒体蛋白的丝氨酸/苏氨酸残基。O- GlcNAc 循环的扰动稳态导致几种病理状况。人类 OGA 是治疗异常低水平O- GlcNAc疾病的有希望的治疗靶点,例如阿尔茨海默病中的 tau 蛋白病。一类新的强效 OGA 抑制剂,2-acetamido-2-deoxy- d-glucono-1,5-lactone (thio)semicarbazones,已被鉴定。从d-葡糖胺开始,分五个步骤设计和合成了八种抑制剂,总产率为 15-55%。具有菌株选择和分离功能的异源 OGA 表达方案已经过优化,可产生稳定、活跃和全长的人类 OGA (hOGA) 同种型。hOGA 的热变性动力学揭示了影响 hOGA 稳定性的环境因素。从动力学实验来看,合成的化合物被证明是 hOGA 的有效竞争性抑制剂,K i -s 范围约为 30-250 nM,对溶酶体 β-氨基己糖苷酶具有中等选择性。电脑模拟由总理蛋白配体细化的研究,QM / MM优化和QM / MM-PBSA结合自由能计算透露的因素支配的观察效力,并导致设计最有力的模拟2-乙酰氨基-2-脱氧的d - glucono-1,5-lactone 4-(2-naphthyl)-semicarbazone 6g ( K i = 36 nM)。所采用的协议在未来针对 OGA 的基于结构的抑制剂设计中具有应用。

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号