当前位置:
X-MOL 学术
›
Inorg. Chem.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
通过点击化学合成后修饰 Curcumin@N3-bio-MOF-100 靶向药物递送系统的乳腺癌
Inorganic Chemistry ( IF 4.3 ) Pub Date : 2021-06-08 , DOI: 10.1021/acs.inorgchem.1c00538 Renata C Alves 1 , Zachary M Schulte 2 , Marcela T Luiz 3 , Patrícia Bento da Silva 4 , Regina C G Frem 5 , Nathaniel L Rosi 2 , Marlus Chorilli 1
Inorganic Chemistry ( IF 4.3 ) Pub Date : 2021-06-08 , DOI: 10.1021/acs.inorgchem.1c00538 Renata C Alves 1 , Zachary M Schulte 2 , Marcela T Luiz 3 , Patrícia Bento da Silva 4 , Regina C G Frem 5 , Nathaniel L Rosi 2 , Marlus Chorilli 1
Affiliation
|
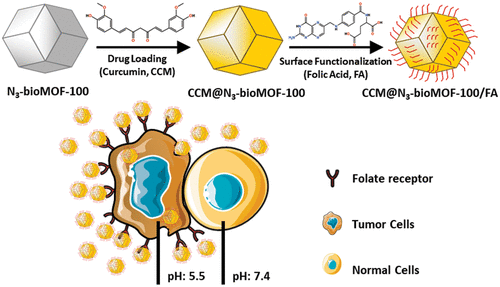
金属有机框架 (MOF) 为生物学和医学领域的应用提供了许多机会。它们广泛的化学成分使毒理学可接受的制剂成为可能,并且它们的高水平功能性使它们成为可能的应用作为治疗剂的递送系统。表面修饰已用于药物递送系统,以最大限度地减少它们与本体的相互作用,提高它们作为靶向载体的特异性。在此,我们讨论了一种使用“点击”化学将功能性叶酸 (FA) 分子锚定在 N 3 -bio-MOF-100表面上以实现靶向肿瘤的载药 MOF 的策略。使用姜黄素 (CCM) 作为抗癌药物,我们观察到浸泡 N 3后的载药封装效率 (DLE) 分别为 24.02 和 25.64%-bio-MOF-100 在 CCM 溶液中分别使用 1 天和 3 天。1 H NMR 光谱、傅里叶变换红外光谱 (FTIR) 和液相色谱-质谱 (LC-MS)证实了 FA 合成后修饰的成功。刺激响应性药物释放研究表明,在酸性微环境下释放的 CCM 增加。此外,在 CCM@N 3 -bio-MOF-100 和 CCM@N 3 -bio-MOF-100/FA 载体存在的情况下,对 4T1(乳腺癌)细胞系进行了细胞活力测定,以确认其生物相容性. 此外,还进行了细胞摄取研究以评估肿瘤细胞的靶向性。

"点击查看英文标题和摘要"
更新日期:2021-08-16

"点击查看英文标题和摘要"


















































 京公网安备 11010802027423号
京公网安备 11010802027423号