当前位置:
X-MOL 学术
›
ACS Appl. Mater. Interfaces
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
缺氧介导的 ROS 扩增通过 PD-L1/ROS 响应、双靶向、载药硫缩酮纳米颗粒触发线粒体介导的细胞凋亡
ACS Applied Materials & Interfaces ( IF 8.3 ) Pub Date : 2021-05-10 , DOI: 10.1021/acsami.1c03594
Asmita Banstola 1 , Kishwor Poudel 2 , Shiva Pathak 3 , Prakash Shrestha 2 , Jong Oh Kim 2 , Jee-Heon Jeong 2 , Simmyung Yook 1
ACS Applied Materials & Interfaces ( IF 8.3 ) Pub Date : 2021-05-10 , DOI: 10.1021/acsami.1c03594
Asmita Banstola 1 , Kishwor Poudel 2 , Shiva Pathak 3 , Prakash Shrestha 2 , Jong Oh Kim 2 , Jee-Heon Jeong 2 , Simmyung Yook 1
Affiliation
|
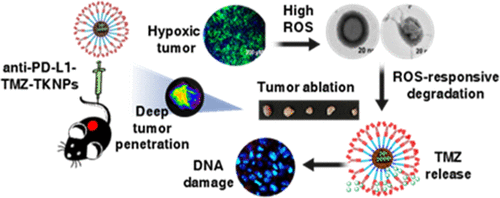
由于纳米粒子的高肿瘤特异性,活性氧 (ROS) 响应刺激与纳米粒子的合并引起了相当大的兴趣。缺氧在加速细胞内 ROS 产生中起关键作用。在此,我们报告了癌细胞 (PD-L1) 和 ROS 响应、双靶向、替莫唑胺 (TMZ) 负载纳米系统的构建,该纳米系统在缺氧肿瘤微环境中提供更好的抗癌效果。双靶向系统促进了癌细胞的渗透。提高高 ROS 水平的缺氧条件加速了原位TMZ 从抗 PD-L1-TKNPs 中释放。TMZ 产生的超积累 ROS 引起氧化损伤,导致线粒体介导的细胞凋亡。在多功能纳米系统(抗PD-L1-TMZ-TKNPs)中制造的TMZ在体内条件下提供了极好的肿瘤积累和延缓肿瘤生长。在用抗 PD-L1-TMZ-TKNPs 治疗后,随着凋亡标记物、DNA 双链断裂标记物的激活和肿瘤组织中血管生成标记物的下调,细胞凋亡效应的增强发挥了强大的抗癌作用。总的来说,纳米结构提供了深入的肿瘤渗透和高药物释放,并拓宽了 ROS 响应纳米系统的应用,以取得成功的抗癌效果。

"点击查看英文标题和摘要"
更新日期:2021-05-19

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号