当前位置:
X-MOL 学术
›
J. Am. Chem. Soc.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Labeling Preferences of Diazirines with Protein Biomolecules
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2021-04-20 , DOI: 10.1021/jacs.1c02509 Alexander V West 1 , Giovanni Muncipinto 2 , Hung-Yi Wu 1 , Andrew C Huang 1 , Matthew T Labenski 2 , Lyn H Jones 3 , Christina M Woo 1
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2021-04-20 , DOI: 10.1021/jacs.1c02509 Alexander V West 1 , Giovanni Muncipinto 2 , Hung-Yi Wu 1 , Andrew C Huang 1 , Matthew T Labenski 2 , Lyn H Jones 3 , Christina M Woo 1
Affiliation
|
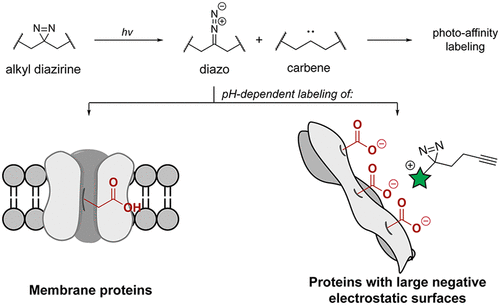
Diazirines are widely used in photoaffinity labeling (PAL) to trap noncovalent interactions with biomolecules. However, design and interpretation of PAL experiments is challenging without a molecular understanding of the reactivity of diazirines with protein biomolecules. Herein, we report a systematic evaluation of the labeling preferences of alkyl and aryl diazirines with individual amino acids, single proteins, and in the whole cell proteome. We find that alkyl diazirines exhibit preferential labeling of acidic amino acids in a pH-dependent manner that is characteristic of a reactive alkyl diazo intermediate, while the aryl-fluorodiazirine labeling pattern reflects reaction primarily through a carbene intermediate. From a survey of 32 alkyl diazirine probes, we use this reactivity profile to rationalize why alkyl diazirine probes preferentially enrich highly acidic proteins or those embedded in membranes and why probes with a net positive charge tend to produce higher labeling yields in cells and in vitro. These results indicate that alkyl diazirines are an especially effective chemistry for surveying the membrane proteome and will facilitate design and interpretation of biomolecular labeling experiments with diazirines.
中文翻译:

用蛋白质生物分子标记二氮嗪的偏好
二氮嗪广泛用于光亲和标记 (PAL) 以捕获与生物分子的非共价相互作用。然而,如果没有对二氮嗪与蛋白质生物分子的反应性的分子理解,PAL 实验的设计和解释是具有挑战性的。在此,我们报告了对具有单个氨基酸、单个蛋白质和整个细胞蛋白质组的烷基和芳基二氮嗪的标记偏好的系统评估。我们发现烷基二氮丙啶以 pH 依赖性方式优先标记酸性氨基酸,这是反应性烷基重氮中间体的特征,而芳基氟二氮丙啶标记模式主要通过卡宾中间体反映反应。从对 32 种烷基二氮嗪探针的调查中,我们使用这种反应性特征来解释为什么烷基二氮嗪探针优先富集高酸性蛋白质或嵌入膜中的蛋白质,以及为什么带有净正电荷的探针倾向于在细胞和体外产生更高的标记产率。这些结果表明烷基二氮丙啶是一种特别有效的化学物质,可用于研究膜蛋白质组,并将促进二氮丙啶生物分子标记实验的设计和解释。
更新日期:2021-05-05
中文翻译:

用蛋白质生物分子标记二氮嗪的偏好
二氮嗪广泛用于光亲和标记 (PAL) 以捕获与生物分子的非共价相互作用。然而,如果没有对二氮嗪与蛋白质生物分子的反应性的分子理解,PAL 实验的设计和解释是具有挑战性的。在此,我们报告了对具有单个氨基酸、单个蛋白质和整个细胞蛋白质组的烷基和芳基二氮嗪的标记偏好的系统评估。我们发现烷基二氮丙啶以 pH 依赖性方式优先标记酸性氨基酸,这是反应性烷基重氮中间体的特征,而芳基氟二氮丙啶标记模式主要通过卡宾中间体反映反应。从对 32 种烷基二氮嗪探针的调查中,我们使用这种反应性特征来解释为什么烷基二氮嗪探针优先富集高酸性蛋白质或嵌入膜中的蛋白质,以及为什么带有净正电荷的探针倾向于在细胞和体外产生更高的标记产率。这些结果表明烷基二氮丙啶是一种特别有效的化学物质,可用于研究膜蛋白质组,并将促进二氮丙啶生物分子标记实验的设计和解释。






























 京公网安备 11010802027423号
京公网安备 11010802027423号