当前位置:
X-MOL 学术
›
Free Radical Bio. Med.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Nrf2 抑制通过抑制 DNA 修复使乳腺癌干细胞对电离辐射敏感
Free Radical Biology and Medicine ( IF 7.1 ) Pub Date : 2021-04-20 , DOI: 10.1016/j.freeradbiomed.2021.04.006 Shenghui Qin 1 , Xiaoyuan He 2 , Houmin Lin 3 , Bradley A Schulte 3 , Mingfeng Zhao 4 , Kenneth D Tew 5 , Gavin Y Wang 6

"点击查看英文标题和摘要"
更新日期:2021-04-26
Free Radical Biology and Medicine ( IF 7.1 ) Pub Date : 2021-04-20 , DOI: 10.1016/j.freeradbiomed.2021.04.006 Shenghui Qin 1 , Xiaoyuan He 2 , Houmin Lin 3 , Bradley A Schulte 3 , Mingfeng Zhao 4 , Kenneth D Tew 5 , Gavin Y Wang 6
Affiliation
|
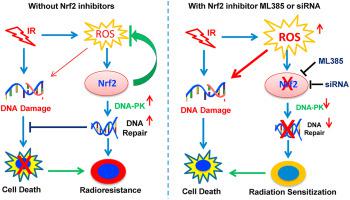
放射线广泛用于癌症治疗,但癌症干细胞(CSC)的放射抗性对癌症治疗的成功提出了重大挑战。核因子红细胞 2 相关因子 2 (Nrf2) 已成为细胞抗氧化反应的重要调节因子,其过度激活与癌细胞的耐药性相关。然而,Nrf2 信号在调节 CSC 对辐射反应中的作用尚未明确。在这里,我们发现三阴性乳腺癌(TNBC)细胞暴露于电离辐射(IR)会上调Nrf2表达并以活性氧(ROS)依赖性方式促进其核转位。Nrf2 的异位过度表达会减弱,而 Nrf2 的敲除会增强 IR 诱导的 TNBC CSC 杀伤作用。从机制上讲,我们发现 Nrf2 敲低会增加 IR 诱导的 ROS 产生,并至少部分通过抑制 DNA-PK 来阻碍 DNA 修复。此外,萝卜硫素对 Nrf2 的激活减弱,而 ML385 对 Nrf2 的抑制增强了 IR 诱导的 TNBC CSC 杀伤作用。总的来说,这些结果表明,红外线诱导的 ROS 产生可以激活 Nrf2 信号传导,从而抵消辐射的杀伤作用。因此,ML385 对 IR 诱导的 Nrf2 激活的药理学抑制可能是一种使治疗抵抗性 CSC 对放射治疗敏感的新治疗方法。

"点击查看英文标题和摘要"


















































 京公网安备 11010802027423号
京公网安备 11010802027423号