当前位置:
X-MOL 学术
›
Mol. Ther. Methods Clin. Dev.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
在Kabuki综合征小鼠模型中,抑制KDM1A活性可恢复成年神经发生并改善海马记忆
Molecular Therapy - Methods & Clinical Development ( IF 4.6 ) Pub Date : 2021-02-18 , DOI: 10.1016/j.omtm.2021.02.011 Li Zhang , Genay Pilarowski , Emilio Merlo Pich , Atsushi Nakatani , John Dunlop , Rina Baba , Satoru Matsuda , Masaki Daini , Yasushi Hattori , Shigemitsu Matsumoto , Mitsuhiro Ito , Haruhide Kimura , Hans Tomas Bjornsson

"点击查看英文标题和摘要"
更新日期:2021-03-07
Molecular Therapy - Methods & Clinical Development ( IF 4.6 ) Pub Date : 2021-02-18 , DOI: 10.1016/j.omtm.2021.02.011 Li Zhang , Genay Pilarowski , Emilio Merlo Pich , Atsushi Nakatani , John Dunlop , Rina Baba , Satoru Matsuda , Masaki Daini , Yasushi Hattori , Shigemitsu Matsumoto , Mitsuhiro Ito , Haruhide Kimura , Hans Tomas Bjornsson
|
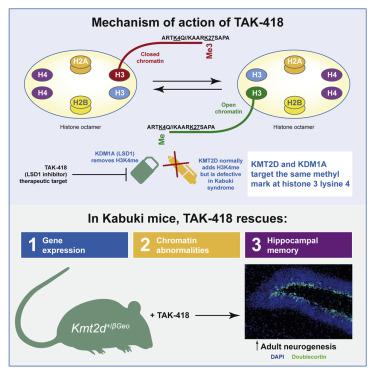
歌舞uki综合症(KS)是智力障碍的罕见原因,主要由赖氨酸特异性甲基转移酶2D(KMT2D)的功能丧失突变引起,该突变通常会在组蛋白3的赖氨酸4上添加甲基标记。先前的研究表明,小鼠KS模型(Kmt2d + /βGeo)证明了成人神经发生和海马记忆的破坏。原理验证研究表明,在促进染色质开放的治疗之后,神经功能障碍的产后挽救得到了缓解。然而,这些策略是非特异性的,不能直接解决组蛋白甲基化的主要缺陷。由于赖氨酸特异性脱甲基酶1A(LSD1 / KDM1A)通常会去除KMT2D添加的H3K4甲基标记,因此我们假设抑制KDM1A脱甲基酶活性可能会改善由于KMT2D丢失引起的分子和表型缺陷。为了验证这一假设,我们在Kmt2d + /βGeo小鼠中评估了最近开发的KDM1A抑制剂(TAK-418)。我们发现口服TAK-418会增加新生双皮质素(DCX)+海马中的细胞和过程呈剂量依赖性。我们还观察到通过蛋白质印迹和染色质免疫沉淀测序(ChIP-seq)的海马中TAK-418依赖的组蛋白修饰缺陷的挽救。治疗挽救了基因表达异常,包括立即早期基因的异常,例如FBJ骨肉瘤癌基因(Fos)和FBJ骨肉瘤癌基因同源物B(Fosb)。经过TAK-418 2周后,Kmt2d + /βGeo小鼠表现出海马记忆缺陷的正常化。总之,我们的数据表明,KDM1A抑制是KS的一种可行治疗策略,并支持以下假设:继KMT2D功能障碍之后的表观遗传失调在KS的产后神经疾病表型中起主要作用。

"点击查看英文标题和摘要"


















































 京公网安备 11010802027423号
京公网安备 11010802027423号