当前位置:
X-MOL 学术
›
Ann. N. Y. Acad. Sci.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
The NO–cGMP–PKG pathway in skeletal remodeling
Annals of the New York Academy of Sciences ( IF 4.1 ) Pub Date : 2020-08-28 , DOI: 10.1111/nyas.14486
Se-Min Kim 1 , Tony Yuen 1 , Jameel Iqbal 1 , Mishaela R Rubin 2 , Mone Zaidi 1
Annals of the New York Academy of Sciences ( IF 4.1 ) Pub Date : 2020-08-28 , DOI: 10.1111/nyas.14486
Se-Min Kim 1 , Tony Yuen 1 , Jameel Iqbal 1 , Mishaela R Rubin 2 , Mone Zaidi 1
Affiliation
|
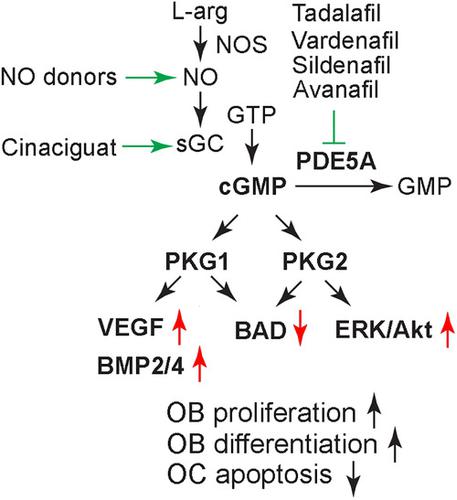
The nitric oxide (NO)-cyclic guanosine monophosphate (cGMP)-protein kinase G (PKG) pathway plays a critical role in skeletal homeostasis. Preclinical data using NO and its donors and genetically modified mice demonstrated that NO was required in bone remodeling and partly mediated the anabolic effects of mechanical stimuli and estrogen. However, the off-target effects and tachyphylaxis of NO limit its long-term use, and previous clinical trials using organic nitrates for osteoporosis have been disappointing. Among the other components in the downstream pathway, targeting cGMP-specific phosphodiesterase to promote the NO-cGMP-PKG signal is a viable option. There are growing in vitro and in vivo data that, among many other PDE families, PDE5A is highly expressed in skeletal tissue, and inhibiting PDE5A using currently available PDE5A inhibitors might increase the osteoanabolic signal and protect the skeleton. These preclinical data open the possibility of repurposing PDE5A inhibitors for treating osteoporosis. Further research is needed to address the primary target bone cell of PDE5A inhibition, the contribution of direct and indirect effects of PDE5A inhibition, and the pathophysiological changes in skeletal PDE5A expression in aging and hypogonadal animal models.
中文翻译:

骨骼重塑中的 NO-cGMP-PKG 途径
一氧化氮 (NO)-环磷酸鸟苷 (cGMP)-蛋白激酶 G (PKG) 通路在骨骼稳态中发挥着关键作用。使用NO及其供体和转基因小鼠的临床前数据表明,NO是骨重塑所必需的,并且部分介导机械刺激和雌激素的合成代谢作用。然而,NO的脱靶效应和快速耐受限制了其长期使用,之前使用有机硝酸盐治疗骨质疏松症的临床试验令人失望。在下游途径的其他成分中,针对 cGMP 特异性磷酸二酯酶来促进 NO-cGMP-PKG 信号是一个可行的选择。越来越多的体外和体内数据表明,在许多其他 PDE 家族中,PDE5A 在骨骼组织中高表达,使用现有的 PDE5A 抑制剂抑制 PDE5A 可能会增加骨合成代谢信号并保护骨骼。这些临床前数据开启了重新利用 PDE5A 抑制剂治疗骨质疏松症的可能性。需要进一步研究来解决 PDE5A 抑制的主要靶骨细胞、PDE5A 抑制的直接和间接作用的贡献,以及衰老和性腺功能减退动物模型中骨骼 PDE5A 表达的病理生理变化。
更新日期:2020-08-28
中文翻译:

骨骼重塑中的 NO-cGMP-PKG 途径
一氧化氮 (NO)-环磷酸鸟苷 (cGMP)-蛋白激酶 G (PKG) 通路在骨骼稳态中发挥着关键作用。使用NO及其供体和转基因小鼠的临床前数据表明,NO是骨重塑所必需的,并且部分介导机械刺激和雌激素的合成代谢作用。然而,NO的脱靶效应和快速耐受限制了其长期使用,之前使用有机硝酸盐治疗骨质疏松症的临床试验令人失望。在下游途径的其他成分中,针对 cGMP 特异性磷酸二酯酶来促进 NO-cGMP-PKG 信号是一个可行的选择。越来越多的体外和体内数据表明,在许多其他 PDE 家族中,PDE5A 在骨骼组织中高表达,使用现有的 PDE5A 抑制剂抑制 PDE5A 可能会增加骨合成代谢信号并保护骨骼。这些临床前数据开启了重新利用 PDE5A 抑制剂治疗骨质疏松症的可能性。需要进一步研究来解决 PDE5A 抑制的主要靶骨细胞、PDE5A 抑制的直接和间接作用的贡献,以及衰老和性腺功能减退动物模型中骨骼 PDE5A 表达的病理生理变化。

































 京公网安备 11010802027423号
京公网安备 11010802027423号