当前位置:
X-MOL 学术
›
Cell. Signal.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
辣椒素通过 TRPV1 介导的线粒体钙超载诱导未分化甲状腺癌细胞的线粒体功能障碍和细胞凋亡。
Cellular Signalling ( IF 4.4 ) Pub Date : 2020-08-06 , DOI: 10.1016/j.cellsig.2020.109733
Shichen Xu 1 , Xian Cheng 1 , Liying Wu 2 , Jiangxia Zheng 2 , Xiaowen Wang 2 , Jing Wu 1 , Huixin Yu 1 , Jiandong Bao 1 , Li Zhang 3

"点击查看英文标题和摘要"
更新日期:2020-08-11
Cellular Signalling ( IF 4.4 ) Pub Date : 2020-08-06 , DOI: 10.1016/j.cellsig.2020.109733
Shichen Xu 1 , Xian Cheng 1 , Liying Wu 2 , Jiangxia Zheng 2 , Xiaowen Wang 2 , Jing Wu 1 , Huixin Yu 1 , Jiandong Bao 1 , Li Zhang 3
Affiliation
|
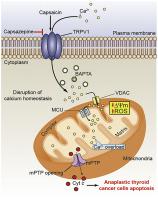
甲状腺未分化癌 (ATC) 是一种罕见的恶性肿瘤,由于其侵袭性行为和对治疗的抵抗力,预后较差。钙 (Ca 2+ ) 作为无处不在的细胞第二信使并影响多种肿瘤行为。因此,Ca 2+调节有望成为癌症的新治疗靶点。然而,Ca 2+调节在ATC治疗中是否有效仍然未知。在这项研究中,我们报道了辣椒素 (CAP) 是一种瞬时受体电位香草素类型 1 (TRPV1) 激动剂,可抑制间变性甲状腺癌细胞的活力。辣椒素处理通过 TRPV1 激活触发 Ca 2+流入,导致细胞内钙稳态失衡。快速增加的胞质 Ca2+浓度反映在线粒体中,并导致 ATC 细胞中线粒体钙超载的严重状况。此外,辣椒素引起线粒体钙稳态的破坏导致 ATC 细胞线粒体功能障碍,如线粒体活性氧 (ROS) 的产生、线粒体膜电位 (ΔΨm) 的去极化和线粒体通透性转换孔的开放(mPTP)。接下来,由此产生的 cyt c释放到细胞质中引发了凋亡体组装以及随后的半胱天冬酶激活和凋亡。值得注意的是,TRPV1 拮抗剂(capsazepine)和钙螯合剂(BAPTA)都可以减弱异常的 Ca 2+辣椒素治疗诱导的体内平衡、线粒体功能障碍和细胞凋亡。因此,我们的研究表明,辣椒素通过 TRPV1 介导的途径在 ATC 细胞中诱导线粒体钙超载和细胞凋亡。更好地了解钙调节的抗癌机制为 ATC 治疗提供了一个潜在的目标。

"点击查看英文标题和摘要"


































 京公网安备 11010802027423号
京公网安备 11010802027423号