当前位置:
X-MOL 学术
›
Appl. Clay. Sci.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
用于环丙沙星口服控释的蒙脱石/环丙沙星/TiO2多孔结构的合成与表征
Applied Clay Science ( IF 5.3 ) Pub Date : 2020-11-01 , DOI: 10.1016/j.clay.2020.105768 Buket Gulen , Pelin Demircivi
Applied Clay Science ( IF 5.3 ) Pub Date : 2020-11-01 , DOI: 10.1016/j.clay.2020.105768 Buket Gulen , Pelin Demircivi
|
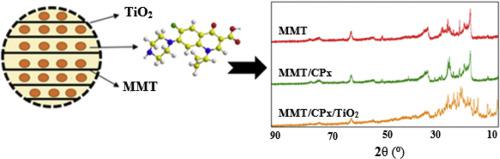
摘要 基于蒙脱石粘土和 TiO2 的生物纳米复合材料被布置为用于口服环丙沙星 (CPx) 的受控给药系统。为此,选择了最小量的商业 CPx,并延长了制备的多孔结构的释放期。为了确定药物递送过程中使用的 MMT 量,CPx 在 MMT 上的吸附在批处理系统中进行。发现 0.1 g MMT 足以吸附 250 mg CPx,吸附效率为 99.2%。在其他模型中,Temkin 等温线模型(R2 = 0.96)最好地描述了 CPx 吸附,这表明吸附热的线性减少。合成的 MMT/CPx 纳米复合材料,包括 0.1 g MMT,涂有不同量的 TiO2(10-100% wt%)以获得 MMT/CPx/TiO2 多孔结构。MMT/CPx/TiO2 (10%) 纳米复合材料在模拟胃液中24 小时内达到100% 释放,而MMT/CPx 和商业CPx 在胃液中分别在15 小时和8 小时内完成释放。MMT/CPx/TiO2 (30%) 在模拟血液中的最长 CPx 释放时间为 69 小时。CPx分子与结构之间的静电吸引力是影响药物传递机制的主要原因。Zeta 电位测量值、FTIR 和 XRD 结果也支持实验数据。CPx 释放曲线与 Korsmeyer-Peppas 动力学模型非常吻合,发现 n 值高于 0.89,这表明 Super Case II 释放机制。MMT/CPx/TiO2 (30%) 在模拟血液中的最长 CPx 释放时间为 69 小时。CPx分子与结构之间的静电吸引力是影响药物传递机制的主要原因。Zeta 电位测量值、FTIR 和 XRD 结果也支持实验数据。CPx 释放曲线与 Korsmeyer-Peppas 动力学模型非常吻合,发现 n 值高于 0.89,这表明 Super Case II 释放机制。MMT/CPx/TiO2 (30%) 在模拟血液中的最长 CPx 释放时间为 69 小时。CPx分子与结构之间的静电吸引力是影响药物传递机制的主要原因。Zeta 电位测量值、FTIR 和 XRD 结果也支持实验数据。CPx 释放曲线与 Korsmeyer-Peppas 动力学模型非常吻合,发现 n 值高于 0.89,这表明 Super Case II 释放机制。

"点击查看英文标题和摘要"
更新日期:2020-11-01

"点击查看英文标题和摘要"




















































 京公网安备 11010802027423号
京公网安备 11010802027423号