当前位置:
X-MOL 学术
›
Biotechnol. Bioeng.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Current technologies to endotoxin detection and removal for biopharmaceutical purification.
Biotechnology and Bioengineering ( IF 3.5 ) Pub Date : 2020-04-25 , DOI: 10.1002/bit.27362 Mason Schneier 1 , Sidharth Razdan 1 , Allison M Miller 1 , Maria E Briceno 1 , Sutapa Barua 1
Biotechnology and Bioengineering ( IF 3.5 ) Pub Date : 2020-04-25 , DOI: 10.1002/bit.27362 Mason Schneier 1 , Sidharth Razdan 1 , Allison M Miller 1 , Maria E Briceno 1 , Sutapa Barua 1
Affiliation
|
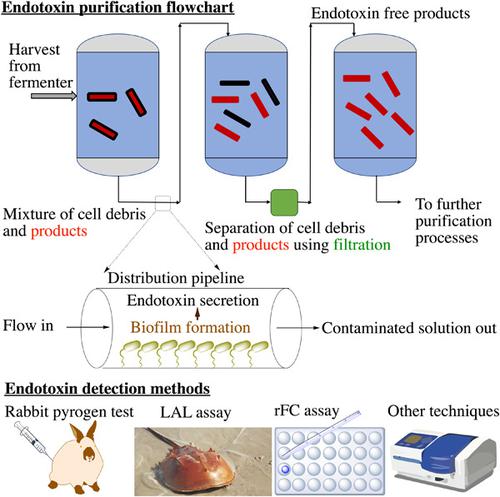
Endotoxins are the major contributors to the pyrogenic response caused by contaminated pharmaceutical products, formulation ingredients, and medical devices. Recombinant biopharmaceutical products are manufactured using living organisms, including Gram‐negative bacteria. Upon the death of a Gram‐negative bacterium, endotoxins (also known as lipopolysaccharides) in the outer cell membrane are released into the lysate where they can interact with and form bonds with biomolecules, including target therapeutic compounds. Endotoxin contamination of biologic products may also occur through water, raw materials such as excipients, media, additives, sera, equipment, containers closure systems, and expression systems used in manufacturing. The manufacturing process is, therefore, in critical need of methods to reduce and remove endotoxins by monitoring raw materials and in‐process intermediates at critical steps, in addition to final drug product release testing. This review paper highlights a discussion on three major topics about endotoxin detection techniques, upstream processes for the production of therapeutic molecules, and downstream processes to eliminate endotoxins during product purification. Finally, we have evaluated the effectiveness of endotoxin removal processes from a perspective of high purity and low cost.
中文翻译:

用于生物制药纯化的内毒素检测和去除的当前技术。
内毒素是由受污染的医药产品、制剂成分和医疗器械引起的热原反应的主要原因。重组生物制药产品是使用活生物体制造的,包括革兰氏阴性菌。革兰氏阴性细菌死亡后,外细胞膜中的内毒素(也称为脂多糖)被释放到裂解物中,在那里它们可以与生物分子(包括目标治疗化合物)相互作用并形成键。生物制品的内毒素污染也可能通过水、原材料(如赋形剂、培养基、添加剂、血清、设备、容器密封系统和制造中使用的表达系统)发生。因此,制造过程是 除了最终药物产品放行测试外,迫切需要通过在关键步骤监测原材料和中间体来减少和去除内毒素的方法。这篇综述文章重点讨论了关于内毒素检测技术、治疗分子生产的上游过程以及在产品纯化过程中消除内毒素的下游过程的三个主要主题。最后,我们从高纯度和低成本的角度评估了内毒素去除工艺的有效性。在产品纯化过程中消除内毒素的下游工艺。最后,我们从高纯度和低成本的角度评估了内毒素去除工艺的有效性。在产品纯化过程中消除内毒素的下游工艺。最后,我们从高纯度和低成本的角度评估了内毒素去除工艺的有效性。
更新日期:2020-04-25
中文翻译:

用于生物制药纯化的内毒素检测和去除的当前技术。
内毒素是由受污染的医药产品、制剂成分和医疗器械引起的热原反应的主要原因。重组生物制药产品是使用活生物体制造的,包括革兰氏阴性菌。革兰氏阴性细菌死亡后,外细胞膜中的内毒素(也称为脂多糖)被释放到裂解物中,在那里它们可以与生物分子(包括目标治疗化合物)相互作用并形成键。生物制品的内毒素污染也可能通过水、原材料(如赋形剂、培养基、添加剂、血清、设备、容器密封系统和制造中使用的表达系统)发生。因此,制造过程是 除了最终药物产品放行测试外,迫切需要通过在关键步骤监测原材料和中间体来减少和去除内毒素的方法。这篇综述文章重点讨论了关于内毒素检测技术、治疗分子生产的上游过程以及在产品纯化过程中消除内毒素的下游过程的三个主要主题。最后,我们从高纯度和低成本的角度评估了内毒素去除工艺的有效性。在产品纯化过程中消除内毒素的下游工艺。最后,我们从高纯度和低成本的角度评估了内毒素去除工艺的有效性。在产品纯化过程中消除内毒素的下游工艺。最后,我们从高纯度和低成本的角度评估了内毒素去除工艺的有效性。






























 京公网安备 11010802027423号
京公网安备 11010802027423号