当前位置:
X-MOL 学术
›
Bioconjugate Chem.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Polydopamine Coated PB-MnO2 Nanoparticles as an Oxygen Generator Nanosystem for Imaging-Guided Single-NIR-Laser Triggered Synergistic Photodynamic/Photothermal Therapy.
Bioconjugate Chemistry ( IF 4.0 ) Pub Date : 2020-04-14 , DOI: 10.1021/acs.bioconjchem.0c00165 Atheer Hameid Odda 1, 2 , Hailiang Li 3 , Naveen Kumar 4 , Naseeb Ullah 1 , Malik Ihsanullah Khan 1 , Gang Wang 1 , Kuang Liang 1 , Tan Liu 1 , Yue-Yin Pan 1 , An-Wu Xu 1
Bioconjugate Chemistry ( IF 4.0 ) Pub Date : 2020-04-14 , DOI: 10.1021/acs.bioconjchem.0c00165 Atheer Hameid Odda 1, 2 , Hailiang Li 3 , Naveen Kumar 4 , Naseeb Ullah 1 , Malik Ihsanullah Khan 1 , Gang Wang 1 , Kuang Liang 1 , Tan Liu 1 , Yue-Yin Pan 1 , An-Wu Xu 1
Affiliation
|
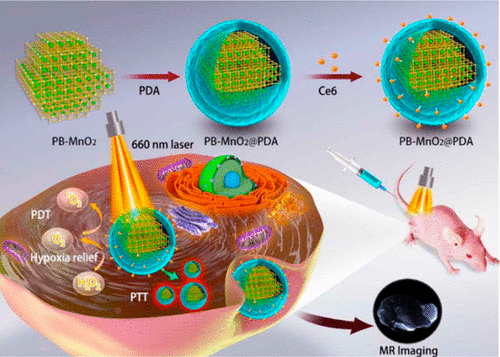
Exploring a combined phototherapeutic strategy to overcome the limitations of a single mode therapy and inducing high anticancer efficiency is highly promising for precision cancer nanomedicine. However, a single-wavelength laser activates dual photothermal/photodynamic therapy (PTT/PDT) treatment is still a formidable challenge. Herein, we strategically design and fabricate a multifunctional theranostic nanosystem based on chlorin e6-functionalized polydopamine (PDA) coated prussian blue/manganese dioxide nanoparticles (PB-MnO2@PDA-Ce6 NPs). Interestingly, the obtained PB-MnO2@PDA NPs not only offer an effective delivery system for Ce6 but also provide strong optical absorption in the near-infrared range, endowing high antitumor efficacy of PTT. More importantly, the as-prepared PB-MnO2@PDA-Ce6 nanoagents exhibit an effective oxygen generation, superior reactive oxygen species (ROS), and outstanding photothermal conversion ability to greatly improve PTT and PDT treatments. As a result, both in vitro and in vivo treatments guided by MR imaging on liver cancer cells reveal the complete cell/tumor eradication under a single wavelength of 660 nm laser irradiation, implying the simultaneous synergistic PDT/PTT effects triggered by PB-MnO2@PDA-Ce6 nanoplatform, which are much higher than individual treatment. Taken together, our phototherapeutic nanoagents exhibit an excellent therapeutic performance, which may act as a nanoplatform to find safe and clinically translatable routes to accelerate cancer therapeutics.
中文翻译:

聚多巴胺涂层的PB-MnO2纳米粒子作为制氧指导的单近红外激光触发的协同光动力/光热疗法的制氧纳米系统。
对于精确的癌症纳米药物,探索一种组合的光疗策略以克服单模治疗的局限性并诱导高抗癌效率是非常有前途的。然而,单波长激光激活双重光热/光动力疗法(PTT / PDT)治疗仍然是一个巨大的挑战。在这里,我们策略性地设计和制造基于二氢卟酚e6官能化的聚多巴胺(PDA)涂层的普鲁士蓝/二氧化锰纳米颗粒(PB-MnO2 @ PDA-Ce6 NPs)的多功能神经治疗纳米系统。有趣的是,所得的PB-MnO2 @ PDA NPs不仅为Ce6提供了有效的递送系统,而且在近红外范围内提供了强大的光吸收,赋予了PTT高抗肿瘤功效。更重要的是,所制备的PB-MnO2 @ PDA-Ce6纳米剂表现出有效的氧气生成,优异的活性氧(ROS)和出色的光热转化能力,可大大改善PTT和PDT处理。结果,在肝癌细胞上通过MR成像指导的体外和体内治疗均显示在660 nm激光照射的单个波长下完全清除了细胞/肿瘤,这暗示着PB-MnO2 @引发的同时PDT / PTT协同效应。 PDA-Ce6纳米平台,比单独治疗要高得多。综上所述,我们的光疗纳米剂具有出色的治疗性能,可以作为纳米平台来寻找安全且可临床翻译的途径来加速癌症治疗。MR成像在肝癌细胞上进行的体外和体内治疗均显示在660 nm激光照射的单个波长下完全清除了细胞/肿瘤,这意味着PB-MnO2 @ PDA-Ce6纳米平台同时触发了PDT / PTT协同作用,比个别治疗要高得多。综上所述,我们的光疗纳米剂具有出色的治疗性能,可以作为纳米平台来寻找安全且可临床翻译的途径来加速癌症治疗。MR成像在肝癌细胞上进行的体外和体内治疗均显示在660 nm激光照射的单个波长下完全清除了细胞/肿瘤,这意味着PB-MnO2 @ PDA-Ce6纳米平台同时触发了PDT / PTT协同作用,比个别治疗要高得多。综上所述,我们的光疗纳米剂具有出色的治疗性能,可以作为纳米平台来寻找安全且可临床翻译的途径来加速癌症治疗。
更新日期:2020-04-14
中文翻译:

聚多巴胺涂层的PB-MnO2纳米粒子作为制氧指导的单近红外激光触发的协同光动力/光热疗法的制氧纳米系统。
对于精确的癌症纳米药物,探索一种组合的光疗策略以克服单模治疗的局限性并诱导高抗癌效率是非常有前途的。然而,单波长激光激活双重光热/光动力疗法(PTT / PDT)治疗仍然是一个巨大的挑战。在这里,我们策略性地设计和制造基于二氢卟酚e6官能化的聚多巴胺(PDA)涂层的普鲁士蓝/二氧化锰纳米颗粒(PB-MnO2 @ PDA-Ce6 NPs)的多功能神经治疗纳米系统。有趣的是,所得的PB-MnO2 @ PDA NPs不仅为Ce6提供了有效的递送系统,而且在近红外范围内提供了强大的光吸收,赋予了PTT高抗肿瘤功效。更重要的是,所制备的PB-MnO2 @ PDA-Ce6纳米剂表现出有效的氧气生成,优异的活性氧(ROS)和出色的光热转化能力,可大大改善PTT和PDT处理。结果,在肝癌细胞上通过MR成像指导的体外和体内治疗均显示在660 nm激光照射的单个波长下完全清除了细胞/肿瘤,这暗示着PB-MnO2 @引发的同时PDT / PTT协同效应。 PDA-Ce6纳米平台,比单独治疗要高得多。综上所述,我们的光疗纳米剂具有出色的治疗性能,可以作为纳米平台来寻找安全且可临床翻译的途径来加速癌症治疗。MR成像在肝癌细胞上进行的体外和体内治疗均显示在660 nm激光照射的单个波长下完全清除了细胞/肿瘤,这意味着PB-MnO2 @ PDA-Ce6纳米平台同时触发了PDT / PTT协同作用,比个别治疗要高得多。综上所述,我们的光疗纳米剂具有出色的治疗性能,可以作为纳米平台来寻找安全且可临床翻译的途径来加速癌症治疗。MR成像在肝癌细胞上进行的体外和体内治疗均显示在660 nm激光照射的单个波长下完全清除了细胞/肿瘤,这意味着PB-MnO2 @ PDA-Ce6纳米平台同时触发了PDT / PTT协同作用,比个别治疗要高得多。综上所述,我们的光疗纳米剂具有出色的治疗性能,可以作为纳米平台来寻找安全且可临床翻译的途径来加速癌症治疗。


















































 京公网安备 11010802027423号
京公网安备 11010802027423号