Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Guselkumab用于患有活动性银屑病关节炎的患者,如果是初生或曾接受过TNFα抑制剂治疗(DISCOVER-1),则为双盲,随机,安慰剂对照的3期临床试验。
The Lancet ( IF 98.4 ) Pub Date : 2020-03-13 , DOI: 10.1016/s0140-6736(20)30265-8
Atul Deodhar 1 , Philip S Helliwell 2 , Wolf-Henning Boehncke 3 , Alexa P Kollmeier 4 , Elizabeth C Hsia 5 , Ramanand A Subramanian 6 , Xie L Xu 4 , Shihong Sheng 7 , Prasheen Agarwal 7 , Bei Zhou 7 , Yanli Zhuang 8 , Christopher T Ritchlin 9 ,

"点击查看英文标题和摘要"
更新日期:2020-04-03
The Lancet ( IF 98.4 ) Pub Date : 2020-03-13 , DOI: 10.1016/s0140-6736(20)30265-8
Atul Deodhar 1 , Philip S Helliwell 2 , Wolf-Henning Boehncke 3 , Alexa P Kollmeier 4 , Elizabeth C Hsia 5 , Ramanand A Subramanian 6 , Xie L Xu 4 , Shihong Sheng 7 , Prasheen Agarwal 7 , Bei Zhou 7 , Yanli Zhuang 8 , Christopher T Ritchlin 9 ,
Affiliation
|
背景
许多银屑病关节炎患者对肿瘤坏死因子(TNF)抑制剂的反应不足。Guselkumab是通过IL-23 p19亚基结合的白介素23(IL-23)的特异性抑制剂,在2期试验中以可接受的安全性显着改善了银屑病关节炎的体征和症状。方法
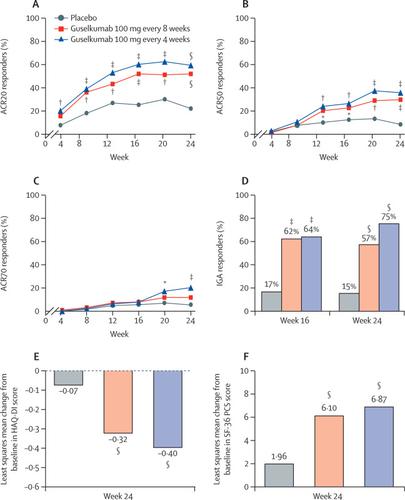
这项多中心,双盲,随机,安慰剂对照的3期临床试验在亚洲,澳大拉西亚,欧洲和北美的13个国家/地区的86个地点进行,并招募了患有活动性银屑病关节炎的成人(至少三个肿胀和三个压痛关节)尽管采用标准疗法,但C反应蛋白仍≥0·3 mg / dL)。资格标准包括对标准治疗的反应不足或不耐受,包括至少4个月的前体药物,至少3个月的非生物疾病改良抗风湿药(DMARD)或至少4周的非甾体类抗炎药对于银屑病关节炎。大约30%的研究参与者以前可能曾接受过一种或两种TNF抑制剂。患者被随机分配(1:1:1,计算机生成的排列区块;通过基线DMARD和先前使用的TNF抑制剂进行分层),每4周皮下注射Guselkumab 100 mg; guselkumab 100 mg在第0、4周,然后每8周一次;或匹配的安慰剂。主要终点是在每个分配的治疗组中,使用无反应者插补的所有患者在第24周时美国风湿病学会改善20%(ACR20)。评估接受治疗的所有患者的安全性。该试用版的注册网址为,(处于活动状态,而非正在招募中)。发现
从2017年8月28日至2018年8月17日,我们筛选了624名患者,其中381名患者被随机分配并每4周(n = 128),每8周(n = 127)进行guselkumab或安慰剂(n = 126)。362名患者继续接受研究治疗,直至第24周。达到了主要终点:每4周组中的guselkumab患者比例显着提高(在第48周中有76 [59%],在128 [95%CI 50-68]中达到了ACR20) ])和每8周组(127 [43–61]中的66 [52%])比安慰剂组(126 [15-30]中的28 [22%]),与安慰剂的百分比差异为37%(每4周组95%CI 26-48),每8周组30%(19-41)(均p <0·0001)。直到第24周,没有发生每4周接受guselkumab的患者的严重不良事件,每8周接受过guselkumab的患者有四(3%)位,五(4%)名接受安慰剂的患者。直到第24周,安慰剂组的一名患者死于心力衰竭,两名严重感染;没有接受古塞珠单抗治疗的患者死亡或受到严重感染。解释
Guselkumab表现出良好的获益-风险特征,对于活动性银屑病关节炎患者可能是一种有效的治疗选择。资金
Janssen研究与开发。
"点击查看英文标题和摘要"







































 京公网安备 11010802027423号
京公网安备 11010802027423号