Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
ROR1通过调节药物外排泵ABCB1来调节乳腺癌的化学耐药性。
Scientific Reports ( IF 3.8 ) Pub Date : 2020-02-04 , DOI: 10.1038/s41598-020-58864-0
Norman Fultang 1 , Abhinav Illendula 1 , Jianhuang Lin 2 , Manoj K Pandey 3 , Zachary Klase 1 , Bela Peethambaran 1
Scientific Reports ( IF 3.8 ) Pub Date : 2020-02-04 , DOI: 10.1038/s41598-020-58864-0
Norman Fultang 1 , Abhinav Illendula 1 , Jianhuang Lin 2 , Manoj K Pandey 3 , Zachary Klase 1 , Bela Peethambaran 1
Affiliation
|
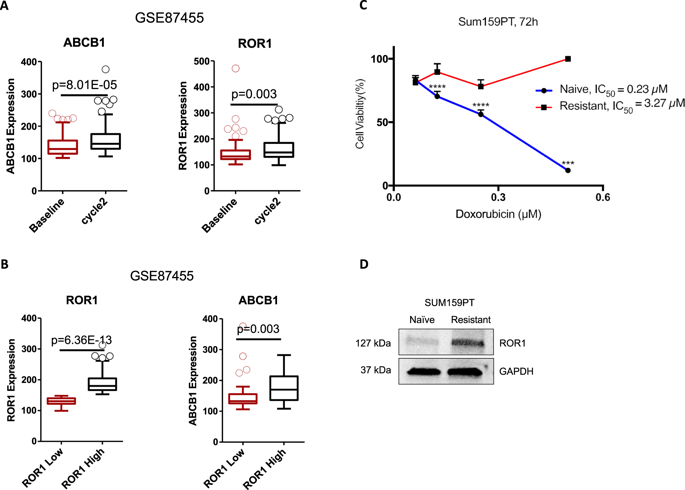
化学抗性是乳腺癌(BC)死亡的主要原因之一。为了对抗BC的化学抗性,了解调节化学抗性的分子至关重要。药物外排泵ABCB1在耐化学性肿瘤中过表达,在那里它从细胞中排出各种化学治疗剂。由于它在正常细胞和癌细胞中均表达,因此直接靶向ABCB1的尝试由于低特异性和正常组织的破坏而失败。提议的抑制ABCB1的方法是针对其癌症特异性上游调节剂,以减轻对正常组织的损害。很少有这类癌症特异性上游调节剂被描述。在这里,我们将ROR1表征为ABCB1的上游调节剂。ROR1在发育过程中高表达,但在正常成人组织中不表达。然而,它在几种癌症中高度表达。ROR1在耐化学性BC中过表达,与不良的治疗反应和肿瘤复发相关。我们的数据表明,ROR1抑制使BC细胞对化学药物敏感。我们还显示ROR1通过MAPK / ERK和p53调节ABCB1稳定性和转录。验证我们的总体发现,ROR1的抑制与化学药物从细胞中流出的减少直接相关。总体而言,我们的结果突出了ROR1作为多药耐药性恶性肿瘤治疗靶点的潜力。验证我们的总体发现,ROR1的抑制与化学药物从细胞中流出的减少直接相关。总体而言,我们的结果突出了ROR1作为多药耐药性恶性肿瘤治疗靶点的潜力。验证我们的总体发现,ROR1的抑制与化学药物从细胞中流出的减少直接相关。总体而言,我们的结果突出了ROR1作为多药耐药性恶性肿瘤治疗靶点的潜力。

"点击查看英文标题和摘要"
更新日期:2020-02-04

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号