当前位置:
X-MOL 学术
›
Aging Cell
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
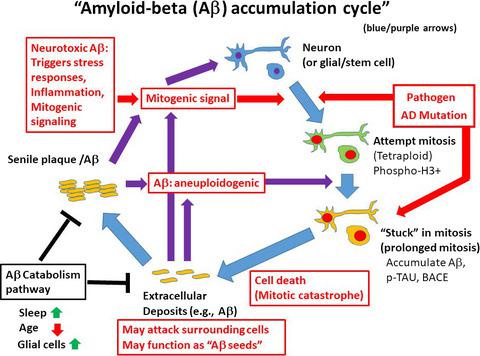
"Amyloid-beta accumulation cycle" as a prevention and/or therapy target for Alzheimer's disease.
Aging Cell ( IF 8.0 ) Pub Date : 2020-01-25 , DOI: 10.1111/acel.13109 Chinthalapally V Rao 1 , Adam S Asch 2 , Daniel J J Carr 3 , Hiroshi Y Yamada 1
Aging Cell ( IF 8.0 ) Pub Date : 2020-01-25 , DOI: 10.1111/acel.13109 Chinthalapally V Rao 1 , Adam S Asch 2 , Daniel J J Carr 3 , Hiroshi Y Yamada 1
Affiliation
|
The cell cycle and its regulators are validated targets for cancer drugs. Reagents that target cells in a specific cell cycle phase (e.g., antimitotics or DNA synthesis inhibitors/replication stress inducers) have demonstrated success as broad‐spectrum anticancer drugs. Cyclin‐dependent kinases (CDKs) are drivers of cell cycle transitions. A CDK inhibitor, flavopiridol/alvocidib, is an FDA‐approved drug for acute myeloid leukemia. Alzheimer's disease (AD) is another serious issue in contemporary medicine. The cause of AD remains elusive, although a critical role of latent amyloid‐beta accumulation has emerged. Existing AD drug research and development targets include amyloid, amyloid metabolism/catabolism, tau, inflammation, cholesterol, the cholinergic system, and other neurotransmitters. However, none have been validated as therapeutically effective targets. Recent reports from AD‐omics and preclinical animal models provided data supporting the long‐standing notion that cell cycle progression and/or mitosis may be a valid target for AD prevention and/or therapy. This review will summarize the recent developments in AD research: (a) Mitotic re‐entry, leading to the “amyloid‐beta accumulation cycle,” may be a prerequisite for amyloid‐beta accumulation and AD pathology development; (b) AD‐associated pathogens can cause cell cycle errors; (c) thirteen among 37 human AD genetic risk genes may be functionally involved in the cell cycle and/or mitosis; and (d) preclinical AD mouse models treated with CDK inhibitor showed improvements in cognitive/behavioral symptoms. If the “amyloid‐beta accumulation cycle is an AD drug target” concept is proven, repurposing of cancer drugs may emerge as a new, fast‐track approach for AD management in the clinic setting.
中文翻译:

“淀粉样蛋白-β积累周期”作为阿尔茨海默病的预防和/或治疗目标。
细胞周期及其调节因子是抗癌药物的有效靶点。针对特定细胞周期阶段的细胞的试剂(例如抗有丝分裂剂或 DNA 合成抑制剂/复制应激诱导剂)已被证明是成功的广谱抗癌药物。细胞周期蛋白依赖性激酶 (CDK) 是细胞周期转变的驱动因素。 CDK 抑制剂,flavopiridol/alvocidib,是 FDA 批准的治疗急性髓系白血病的药物。阿尔茨海默病(AD)是当代医学中的另一个严重问题。尽管潜在的β-淀粉样蛋白积累的关键作用已经被发现,但 AD 的病因仍然难以捉摸。现有的 AD 药物研发目标包括淀粉样蛋白、淀粉样蛋白代谢/分解代谢、tau、炎症、胆固醇、胆碱能系统和其他神经递质。然而,没有一个被验证为治疗有效的靶点。 AD 组学和临床前动物模型的最新报告提供的数据支持了长期存在的观点,即细胞周期进展和/或有丝分裂可能是 AD 预防和/或治疗的有效目标。本综述将总结 AD 研究的最新进展: (a) 有丝分裂再进入导致“β-淀粉样蛋白积累循环”,可能是β-淀粉样蛋白积累和 AD 病理学发展的先决条件; (b) AD 相关病原体可导致细胞周期错误; (c) 37 个人类 AD 遗传风险基因中有 13 个可能在功能上参与细胞周期和/或有丝分裂; (d) 用 CDK 抑制剂治疗的临床前 AD 小鼠模型显示认知/行为症状有所改善。如果“β-淀粉样蛋白积累周期是 AD 药物靶标”的概念得到证实,癌症药物的重新利用可能会成为临床环境中 AD 管理的一种新的快速方法。
更新日期:2020-01-25
中文翻译:

“淀粉样蛋白-β积累周期”作为阿尔茨海默病的预防和/或治疗目标。
细胞周期及其调节因子是抗癌药物的有效靶点。针对特定细胞周期阶段的细胞的试剂(例如抗有丝分裂剂或 DNA 合成抑制剂/复制应激诱导剂)已被证明是成功的广谱抗癌药物。细胞周期蛋白依赖性激酶 (CDK) 是细胞周期转变的驱动因素。 CDK 抑制剂,flavopiridol/alvocidib,是 FDA 批准的治疗急性髓系白血病的药物。阿尔茨海默病(AD)是当代医学中的另一个严重问题。尽管潜在的β-淀粉样蛋白积累的关键作用已经被发现,但 AD 的病因仍然难以捉摸。现有的 AD 药物研发目标包括淀粉样蛋白、淀粉样蛋白代谢/分解代谢、tau、炎症、胆固醇、胆碱能系统和其他神经递质。然而,没有一个被验证为治疗有效的靶点。 AD 组学和临床前动物模型的最新报告提供的数据支持了长期存在的观点,即细胞周期进展和/或有丝分裂可能是 AD 预防和/或治疗的有效目标。本综述将总结 AD 研究的最新进展: (a) 有丝分裂再进入导致“β-淀粉样蛋白积累循环”,可能是β-淀粉样蛋白积累和 AD 病理学发展的先决条件; (b) AD 相关病原体可导致细胞周期错误; (c) 37 个人类 AD 遗传风险基因中有 13 个可能在功能上参与细胞周期和/或有丝分裂; (d) 用 CDK 抑制剂治疗的临床前 AD 小鼠模型显示认知/行为症状有所改善。如果“β-淀粉样蛋白积累周期是 AD 药物靶标”的概念得到证实,癌症药物的重新利用可能会成为临床环境中 AD 管理的一种新的快速方法。































 京公网安备 11010802027423号
京公网安备 11010802027423号