当前位置:
X-MOL 学术
›
Org. Lett.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Traceless and Chemoselective Amine Bioconjugation via Phthalimidine Formation in Native Protein Modification
Organic Letters ( IF 4.9 ) Pub Date : 2016-05-18 00:00:00 , DOI: 10.1021/acs.orglett.6b00983
Chun Ling Tung 1 , Clarence T T Wong 1 , Eva Yi Man Fung 1 , Xuechen Li 1
Organic Letters ( IF 4.9 ) Pub Date : 2016-05-18 00:00:00 , DOI: 10.1021/acs.orglett.6b00983
Chun Ling Tung 1 , Clarence T T Wong 1 , Eva Yi Man Fung 1 , Xuechen Li 1
Affiliation
|
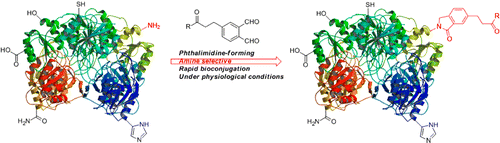
ortho-Phthalaldehyde (OPA) and its derivatives are found to react chemoselectively with amino groups on peptides and proteins rapidly and tracelessly under the physiological condition via formation of phthalimidines, which provides a novel and promising approach when performing bioconjugation on native proteins. The notable advantages of this method over the existing native protein lysine-labeling approaches include a traceless process, a self-reacting, specific and fast reaction, ease of operation, and the ability to use nonhydrolyzable reagents. Its applications have been effectively demonstrated including conjugation of peptides and proteins, and generation of an active PEGlyated l-asparaginase.
中文翻译:

天然蛋白质修饰中通过邻苯二脒形成的无痕化学选择性胺生物共轭
邻苯二甲醛(OPA)及其衍生物被发现在生理条件下与肽和蛋白质上的氨基发生化学选择性反应,通过形成邻苯二甲酰亚胺,快速、无痕迹地发生反应,这为天然蛋白质的生物缀合提供了一种新颖且有前景的方法。与现有的天然蛋白质赖氨酸标记方法相比,该方法的显着优点包括无痕过程、自反应、特异且快速的反应、易于操作以及能够使用不可水解试剂。其应用已得到有效证明,包括肽和蛋白质的缀合以及活性聚乙二醇化L-天冬酰胺酶的生成。
更新日期:2016-05-18
中文翻译:

天然蛋白质修饰中通过邻苯二脒形成的无痕化学选择性胺生物共轭
邻苯二甲醛(OPA)及其衍生物被发现在生理条件下与肽和蛋白质上的氨基发生化学选择性反应,通过形成邻苯二甲酰亚胺,快速、无痕迹地发生反应,这为天然蛋白质的生物缀合提供了一种新颖且有前景的方法。与现有的天然蛋白质赖氨酸标记方法相比,该方法的显着优点包括无痕过程、自反应、特异且快速的反应、易于操作以及能够使用不可水解试剂。其应用已得到有效证明,包括肽和蛋白质的缀合以及活性聚乙二醇化L-天冬酰胺酶的生成。

































 京公网安备 11010802027423号
京公网安备 11010802027423号