西南交大孟涛团队CEJ:液-液相分离调控复杂反应
通讯作者:苑昊、孟涛(西南交通大学生命科学与工程学院)
作者:Junqiu Ma(马君秋), Kaihui Xu(徐开慧), Chenlong Guo(郭晨龙), Sicheng Chen(陈思成), Wen Xie(谢雯), Xingyuan Fang(方兴元), Ting Guo(郭婷), Hao Yuan*(苑昊), Tao Meng*(孟涛)
数百万年来,细胞通过自然选择进化出一种特殊策略——液-液相分离(LLPS),以此来精确控制细胞内部的物质和功能。自从2009年LLPS首次提出以来,充分研究其反应动力学、热力学以及分子机制已经成为了一项前沿科学挑战。为了更深入地理解LLPS的反应特性,科学家们构建了体外LLPS系统,例如凝聚体和双水相系统(ATPS),这些系统能够隔离催化剂,从而揭示LLPS在细胞过程中的关键作用。通过这些研究能够了解到LLPS通过熵驱动效应、多价大分子相互作用等方式,形成了一个独特的微环境,这个环境可以调节酶和核酸等生物分子的活性,并且通过半透性界面动态调节微环境的成分。在此基础上,科学家们还基于细胞内LLPS的原理,设计了仿生微反应器,这些反应器具有隔室化和高效物质传输的特点,显著提高了生化过程的反应速率,比如级联催化反应、核酶切割反应和RNA催化,从而给生物催化领域带来了革命性的变化。因此,对LLPS的深入研究不仅能够加深我们对生命系统工作机制的理解,也能为生物技术的发展提供新的视角。尽管如此,目前对LLPS的认识仍然有限,大部分研究仅局限于一到两个催化步骤的简单模型反应,而细胞内的各类生化反应往往复杂且具有多个步骤,这大大限制了LLPS作为生物反应器在更广泛领域的应用。
近日,西南交通大学孟涛教授(点击查看介绍)团通过构建和筛选一个定制的LLPS系统,并以复杂的核酸扩增反应为例,发现 LLPS 可以在稀释环境中富集必要的反应物,从而维持和加速复杂的反应,其富集程度比普通水相系统高出 13 倍。更重要的是,与均匀加速的简单反应不同,LLPS 对复杂反应的加速取决于每个反应阶段的动力学和反应物浓度,揭示了细胞内核酸复制的内在机制。此外,通过加入 LLPS 及其阶段特异性因子,展示了基于 LLPS 的分子诊断工具的发展,与传统方法相比,它具有更短的检测时间、更高的效率和灵敏度,拓展了 LLPS 作为高效生物反应器在诊断方面的应用。
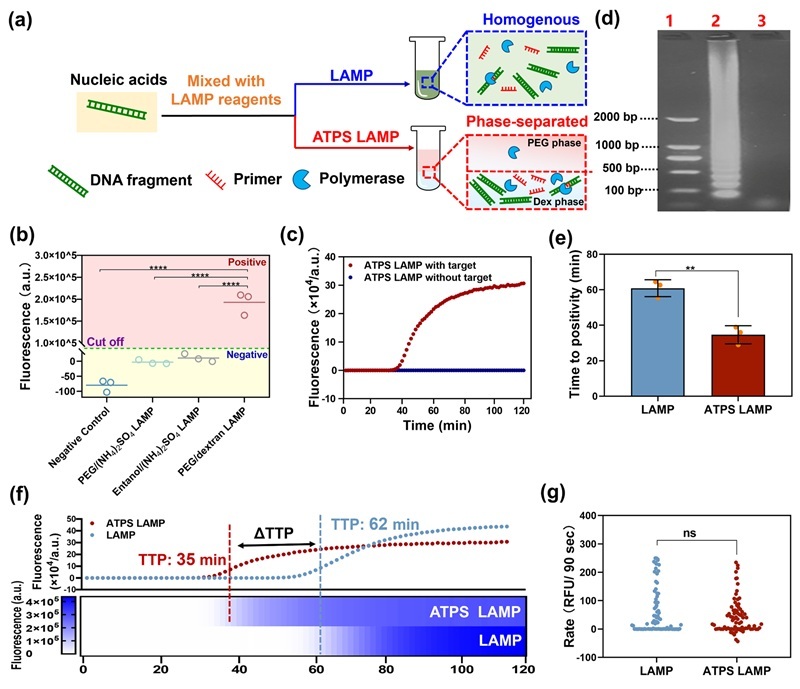
图1. 在LLPS中进行复杂有序的顺序反应及相应动力学分析
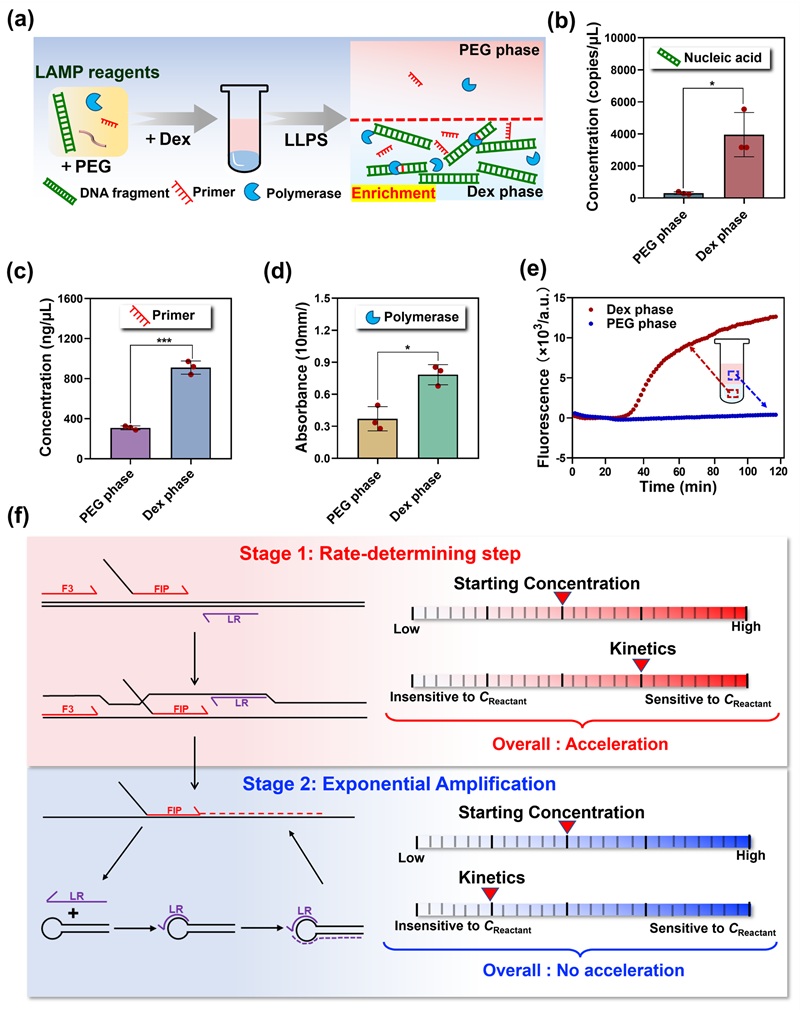
图2. LLPS调控复杂反应的机制
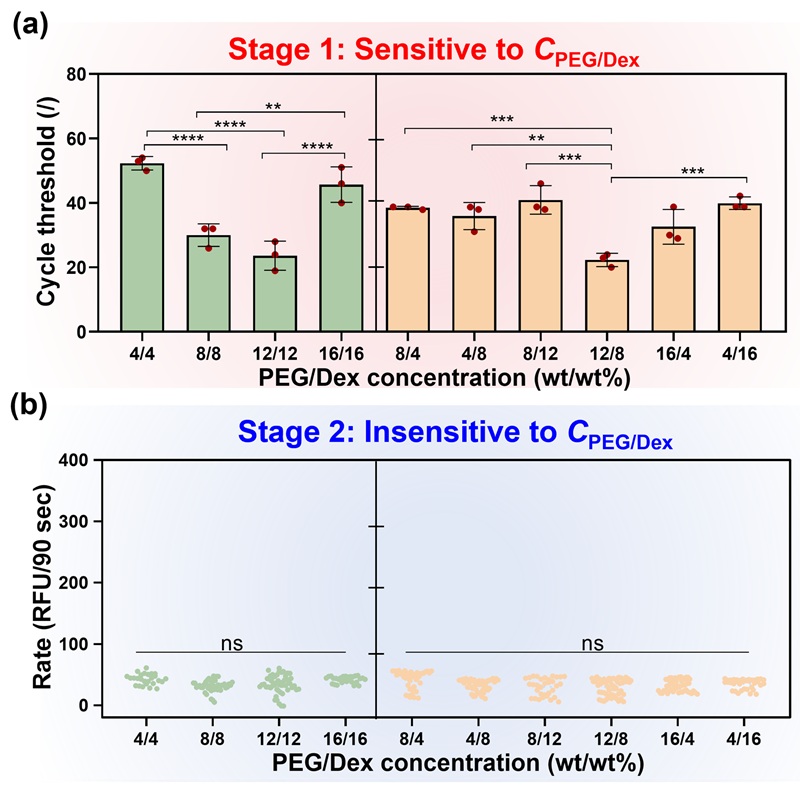
图3. ATPS的性质对复杂反应不同阶段加速效果的影响
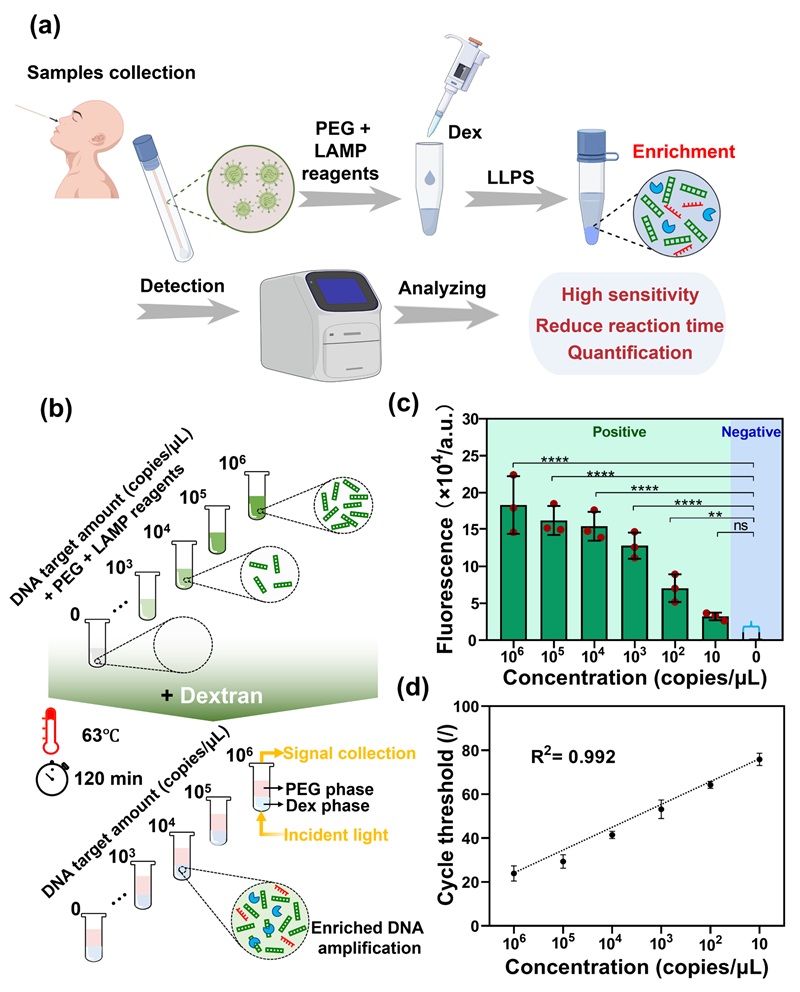
图4. LLPS作为病原体和疾病检测的诊断工具
总结/展望
本研究揭示了 LLPS 介导的复杂反应的复杂性,并能创造出更准确、更可靠的诊断工具,为诊断学的进步铺平了道路,并为进一步利用 LLPS 拓展了可能性。该研究得到国家自然科学基金项目(22204130, 22378336, 21776230),四川省科技厅重点研发项目(2021YFN0129, 2022NSFSC1211),中央高校基础研究基金((2682024ZTPY001, 2682023ZTPY048, 2682021ZTPY031)的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

The stage- and kinetics-dependent regulation of highly ordered sequential reactions by liquid-liquid phase separation
Junqiu Ma, Kaihui Xu, Chenlong Guo, Sicheng Chen, Wen Xie, Xingyuan Fang, Ting Guo, Hao Yuan *, Tao Meng *
Chem. Eng. J., 2024, DOI: 10.1016/j.cej.2024.155610
导师介绍
孟涛
https://www.x-mol.com/university/faculty/186043
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
核内“液-液相分离”对染色质结构的感知与重塑 2018-12-12
-
Angew. Chem.:液-液相分离介导的肽超分子组装成核-生长新机制 2019-10-31
-
磷光金属钌配合物DNA分子光开关用于活细胞DNA相分离诱导与示踪 2021-08-13
-
Liquid-liquid phase separation in hair cell stereocilia development and maintenanceComputational and Structural Biotechnology Journal (IF 4.4) Pub Date : 2023-02-24 ,DOI:10.1016/j.csbj.2023.02.040Jianchao Li
-
The Regulatory Mechanism of Transthyretin Irreversible Aggregation through Liquid-to-Solid Phase Transition.International Journal of Molecular Sciences (IF 4.9) Pub Date : 2023-02-13 ,DOI:10.3390/ijms24043729Guangfei Duan,Yanqin Li,Meimei Ye,Hexin Liu,Ning Wang,Shizhong Luo








































 京公网安备 11010802027423号
京公网安备 11010802027423号