福州大学郑寿添/李新雄/高瑜Angew:具有类芬顿反应活性和高生物相容性的多钨氧酸盐用于高效肿瘤化学动力治疗
癌症是一个普遍存在和威胁生命健康的严峻问题,对当代生物医学研究提出了重大挑战。将芬顿化学和纳米医学融入到癌症治疗中极大地推动了肿瘤的化学动力疗法(CDT)的发展。多金属氧酸盐(POMs)是一类由高价的前过渡金属(Mo、W、V、Nb、Ta)与氧形成的多核金属氧簇化合物,因其结构的多样性和性质的可调性在越来越多领域受到广泛而持续的关注。POMs也被誉为“电子海绵”,其具有独特的接受或释放电子的能力,并可以在不发生明显结构变化的情况下进行快速可逆的多电子氧化还原反应。这些特性使得POMs有望作为CDT药物通过催化类芬顿反应将肿瘤微环境(TME)中过表达的H2O2催化分解成高毒性的活性氧,进而抑制肿瘤的生长。然而,由于缺乏兼具优异的类芬顿催化活性、溶解性、生物相容性和安全性的POMs,采用POMs材料通过CDT治疗癌症的研究仍然尚待发展且富有挑战性。
近日,福州大学郑寿添/李新雄/高瑜教授通过简易的“一锅法”溶剂热反应,以克级高产率合成了一种尺寸约为1.0 × 1.0 × 1.9 nm3的胶囊状新型锑钨酸纳米簇合物{Dy2Sb2W7O23(OH) (DMF)2(SbW9O33)2}(1)。化合物1不仅具有良好的水溶性、稳定性和生物安全性,而且展现出优异的类芬顿催化活性,其能够利用TME中过表达的H2O2和谷胱甘肽(GSH)通过类芬顿反应高效催化H2O2分解生成高氧化性的羟基自由基(•OH),从而杀死肿瘤细胞和抑制肿瘤的生长。体外实验证明1可以诱导细胞凋亡和促进脂质过氧化,对B16-F10小鼠黑色素瘤癌细胞表现出很高的细胞毒性和选择性。同时,1在小鼠体内实验中也表现出优异的CDT抗肿瘤效果和良好的体内安全性,证明了1是一种潜在的强效CDT治疗癌症的候选药物。这项研究工作不仅首次证明了晶态锑钨酸盐在CDT药物开发中的巨大潜力,而且为新型抗癌药物的开发提供了新的见解和方法。
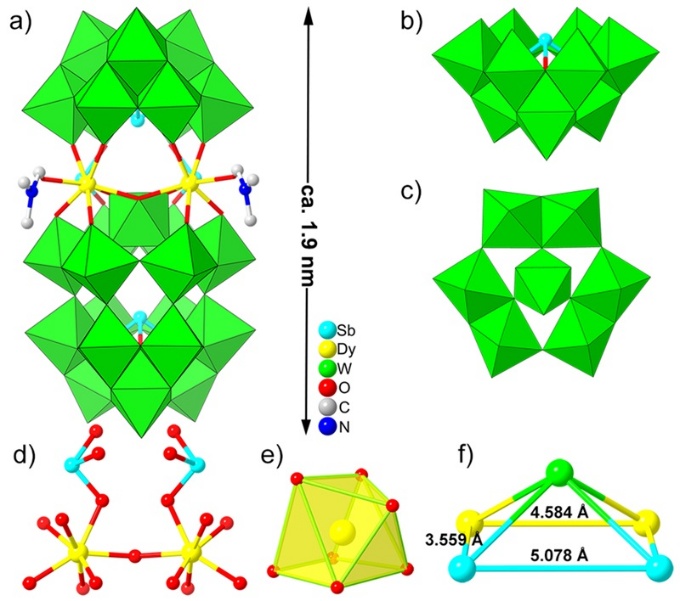
图1. 化合物1的晶体结构及其构筑基元
本项工作中,研究人员将具有抗肿瘤活性的Sb元素引入到POMs中,通过简易的“一锅法”溶剂热反应,以克级高产率合成了一种尺寸约为1.0×1.0×1.9 nm3的胶囊状新型锑钨酸纳米簇合物。图1展示了化合物1的晶体结构,其由两个三缺位的{B-α-SbW9O33}单元共同夹心一个七核同钨多酸簇块{W7O29(OH)}和一个四核Sb-Dy异金属簇{Sb2Dy2O10(DMF)2}组成。化合物1具有非常出色的水溶性,图2中电喷雾电离质谱表明其在水溶液中能够以完整簇的形式稳定存在。此外,高角度环形暗场扫描透射电子显微镜和动态光散射测试结果表明,化合物1可以均匀地分散在水溶液中,平均粒径约为2.0 nm,与单晶结构分析测定的尺寸接近。有趣的是,化合物1展现出优异的类芬顿催化活性,共聚焦激光扫描显微镜(CLSM)显示化合物1可以利用肿瘤细胞中过多的H2O2和GSH促进•OH的生成,使其有望用于CDT癌症治疗。
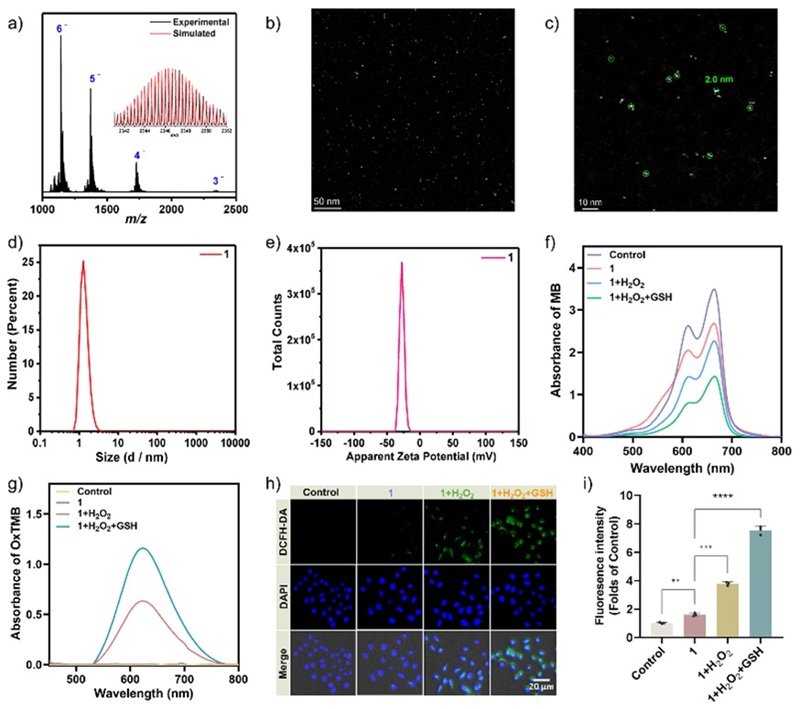
图2. 化合物1在溶液中的稳定性、分散性及类芬顿催化活性
表1中体外细胞毒性测试结果表明,化合物1对多种癌细胞表现出广谱的抗肿瘤活性,其中对B16-F10小鼠黑素瘤癌细胞表现出高细胞毒性,在72小时处理后,IC50值为4.75 μM,而对L929正常小鼠成纤维细胞的细胞毒性较弱,表明1对肿瘤细胞具有较高的特异性。相比之下,起始原料Na2WO4, Dy(NO3)3•6H2O和{SbW9O33}前驱体对B16-F10细胞几乎没有细胞毒性,进一步说明1的独特结构有助于其抗肿瘤活性的提升。随后,对化合物1的抗肿瘤作用机制进行探究,线粒体膜电位和流式细胞术分析等测试结果表明(图3),化合物1通过催化类芬顿反应产生活性氧破坏线粒体膜电位、诱导细胞凋亡和促进细胞膜的脂质过氧化来消除肿瘤细胞。
表1. 化合物1对不同癌细胞系和正常细胞的抑增殖活性
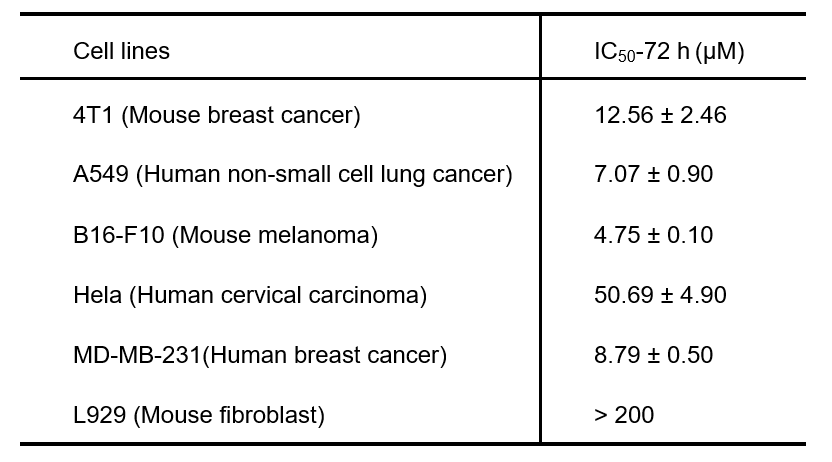
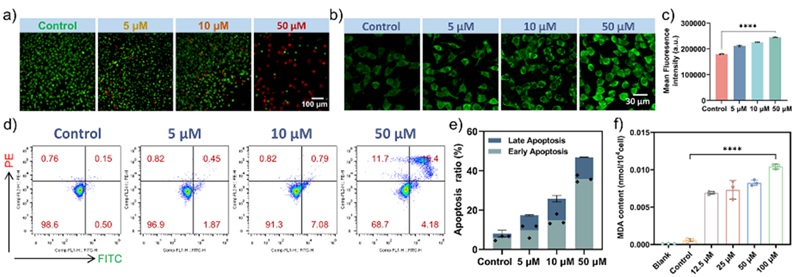
图3. 化合物1对B16-F10细胞的抗肿瘤作用机制探究
最后,研究人员在B16-F10荷瘤小鼠模型中进一步研究了化合物1在体内的CDT肿瘤治疗效果。图4结果显示,与对照组相比,低剂量组的肿瘤体积缩小了近3.2倍,肿瘤重量减轻了43.4%;高剂量组中肿瘤体积缩小了近5.2倍,肿瘤重量减轻了76.0%,说明化合物1在体内具有高效的抗肿瘤活性。此外,各组小鼠均未观察到体重减轻或行为异常,且在正常组织(心脏、肝脏、脾脏、肺和肾脏)中未观察到明显的组织损伤和炎症反应,而用化合物1处理的肿瘤细胞的细胞核和细胞质则受到明显损伤。值得注意的是,CLSM显示在化合物1处理的肿瘤组织中可以观察到强烈的•OH信号,说明化合物1的是抗肿瘤活性归因于类芬顿反应产生的活性氧,凸显了化合物1作为一种安全高效的CDT候选药物用于癌症治疗的巨大潜力。

图4. 化合物1的小鼠体内抑瘤实验
相关工作近期发表在Angew. Chem. Int. Ed.上,福州大学化学学院郑寿添教授、李新雄研究员和高瑜教授为论文的共同通讯作者,福州大学化学学院博士研究生肖慧萍和硕士研究生杜曼宜为论文的共同第一作者。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Highly Biocompatible Polyoxotungstate with Fenton-like Reaction Activity for Potent Chemodynamic Therapy of Tumors
Hui-Ping Xiao, Man-Yi Du, Xian-Bin Sun, Ruo-Fei Xu, Dong-Miao Li, Sheng-Nan Yue, Ping-Wei Cai, Rong-Zhi Sun, Zi-Zhong Zhang, Xing Huang, Xin-Xiong Li, Yu Gao, Shou-Tian Zheng
Angew. Chem. Int. Ed., 2024, DOI: 10.1002/anie.202422949
导师介绍
郑寿添
https://www.x-mol.com/university/faculty/9549
高瑜
https://www.x-mol.com/university/faculty/9576
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号