Nano Res.[生物]│四川大学孙逊团队:共载抗原和唑来膦酸的铝盐纳米粒显著增强细胞免疫应答
本篇文章版权为 孙逊课题组等所有,未经授权禁止转载。

背景介绍 亚单位疫苗由纯化后的病原体抗原制备而成,具有安全性高、易于制备和储存的优点。然而,亚单位疫苗免疫原性较低且淋巴结靶向效率差,难以激活CD8+ T细胞免疫应答,因此对于癌症患者的临床效果有限。联用佐剂和使用疫苗递送系统可显著提高亚单位疫苗的免疫刺激效率。 唑来膦酸(Zoledronte, ZOL)是第三代含氮双膦酸盐,可以通过抑制甲羟戊酸通路中的法尼基焦磷酸合酶影响下游产物Rab GTPases的异戊二烯化修饰,进而延缓吞噬体与溶酶体的融合,促进抗原的交叉呈递。因此,唑来膦酸可作为一种潜在的疫苗佐剂以减少抗原降解和诱导细胞免疫反应。 成果简介 本研究构建了一种共载亚单位抗原和唑来膦酸的氢氧化铝纳米疫苗,以增强亚单位抗原的CD8+ T细胞应答(图1)。研究者利用带正电荷的氢氧化铝内核吸附带负电荷的蛋白抗原, 利用内核上的-OH基团与唑来膦酸的-PO4-基团的配位交换作用实现唑来膦酸的包载。同时,通过使用PEG衍生物(PEGn-ploy(AGE-Suc)m(PpAS))来控制氢氧化铝内核聚集,采用简便的两相混合法即可得到共载抗原和ZOL佐剂的铝盐纳米粒(APN-OVA-ZOL)。 实验结果显示,APN-OVA-ZOL能有效靶向淋巴结,并被淋巴结内的树突状细胞摄取。APN-OVA-ZOL成功干扰了树突状细胞内抗原转运过程,增强了抗原的交叉呈递能力。在荷瘤小鼠模型中,APN-OVA-ZOL显著增强了细胞免疫应答,有效抑制了EG7-OVA肿瘤生长,并延长了小鼠的生存期。此项研究表明,调节抗原呈递细胞的抗原处理过程是一种极具潜力的策略,用于提高癌症免疫治疗的效果。 作者简介 孙逊,四川大学华西药学院教授、药剂学系主任、国家杰出青年基金获得者,英国皇家学会牛顿高级学者,中国药学会药剂专业委员会副主任委员,四川省药学会副秘书长。研究方向为生物大分子药物高效递释系统和靶向药物传递系统,获国家科技进步二等奖,四川省科技进步一等奖,树兰医学青年奖等荣誉。担任美国基因和细胞治疗协会(ASGCT)官方杂志Molecular Therapy和药剂学排名第一的SCI期刊J. Controlled Release副主编,在Nature Communication、Science Advances、Advanced Materials等权威期刊发表SCI论文100余篇,累计获授权专利20余项。 文章信息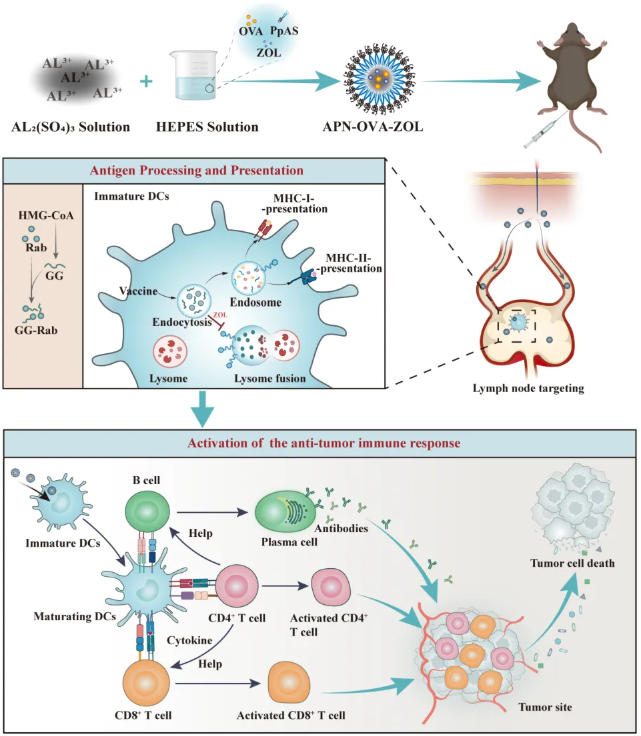


如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!































 京公网安备 11010802027423号
京公网安备 11010802027423号