Nature:开环复分解,芳香族来也
芳香族化合物稳定且分子形状明确,具有多种多样的构环策略,广泛应用于化学和材料科学领域。芳香族化合物虽能够参与多种取代反应,但其去芳构化仍然是个具有挑战性的课题。目前,化学家发展的去芳构化策略包括:1)Birch 还原、芳烃氢化、各种环加成和氧化反应;2)芳香族化合物的扩环反应(图1a),即Buchner等人通过卡宾/氮宾/phosphinidene与芳香族化合物发生(6+1)环加成以及对旋6π电环化开环反应来制备七元环;3)芳香族化合物与亲芳烃体进行环加成、环氧化和环扩张(图1b),但由于芳香族C=C键的高键解离能导致裂解芳香环的方法明显较少。另一方面,自然界利用酶氧化(杂)芳烃实现去芳构化,例如:细菌利用双加氧酶先将芳烃转化为cis-二氢二醇,再经酶促裂解获得粘康酸衍生物(图1c),而真核生物通常利用单加氧酶形成芳烃氧化物作为氧化开环的第一步。近来,化学家利用铜催化实现了非酶裂解官能团化芳烃并获相应的烯基腈(图1d)。对非芳香性的结构来说,过渡金属亚烷基配合物催化的烯烃/炔烃复分解形成和断裂C-C键的通用策略(图1e),三位化学家也因在烯烃复分解反应研究与应用领域的贡献而获得了2005年诺贝尔化学奖,但是,要想通过复分解反应让芳香族化合物开环却并非易事。
考虑到过渡金属亚烷基衍生物在复分解反应中的作用,瑞士巴塞尔大学的Christof Sparr教授课题组设想能否借助合适的内源性驱动力来开发一种高效的催化体系,进而从动力学和热力学上解决芳环的开环问题?近日,Christof Sparr教授课题组利用Schrock-Hoveyda型钼催化剂成功地实现了芳香族化合物(包括:苯并蒽、萘、吲哚、苯并呋喃和菲)的开环复分解反应(aromatic ring-opening metathesis, ArROM,图1f),每种环体系的反应都通过独特的亚烷基中间体进行。值得注意的是,该方法不仅能通过催化剂的调控实现立体选择性芳族开环复分解,而且无需任何试剂或光激发即可进行各种芳香族化合物的催化转化和相互转化。相关文章发表于Nature 上。

图1. 研究背景和本文工作。图片来源:Nature
首先,作者对ArROM的可行性进行了探索,即[2+2]-环加成与芳烃形成闭环复分解步骤(RCM)串联,以通过常见的金属环中间体促进芳环断裂(图2a)。初步研究表明苯并蒽1在市售钼催化剂C1(10 mol%)的作用下于65℃反应18 h后,能以82%的产率获得所需产物2。与1相比,2的形成在热力学上是有利的,并且其总体的芳香稳定性更高。随后,作者探索了萘基底物3的ArROM反应(图2b),即将ArROM与双重RCM结合,成功地实现了3的裂解并以74%的产率获得稠二萘4。类似地,五元杂环(如:吲哚底物 5a和苯并呋喃底物 5b)也可通过ArROM和双重关环复分解转化为相应的萘并吲哚6a(产率:98%)和菲并呋喃6b(产率:92%,图2c)。如图2d所示,作者还利用双重ArROM和双重RCM策略双向合成了可拓展的多环芳烃(PAHs),其中底物7a和 7b进行反应时获得了芳基化benzo[k]tetraphene(8a-8b,产率:56%-67%),而区域异构体7c则获得了具有另一特征几何结构的benzo[m]-tetraphene(8c,产率:63%)。此外,该方法也可获得具有拓展性多芳烃且高度不稳定的dibenzo[a,j]tetracene(8d),尽管产率较低(31%)。
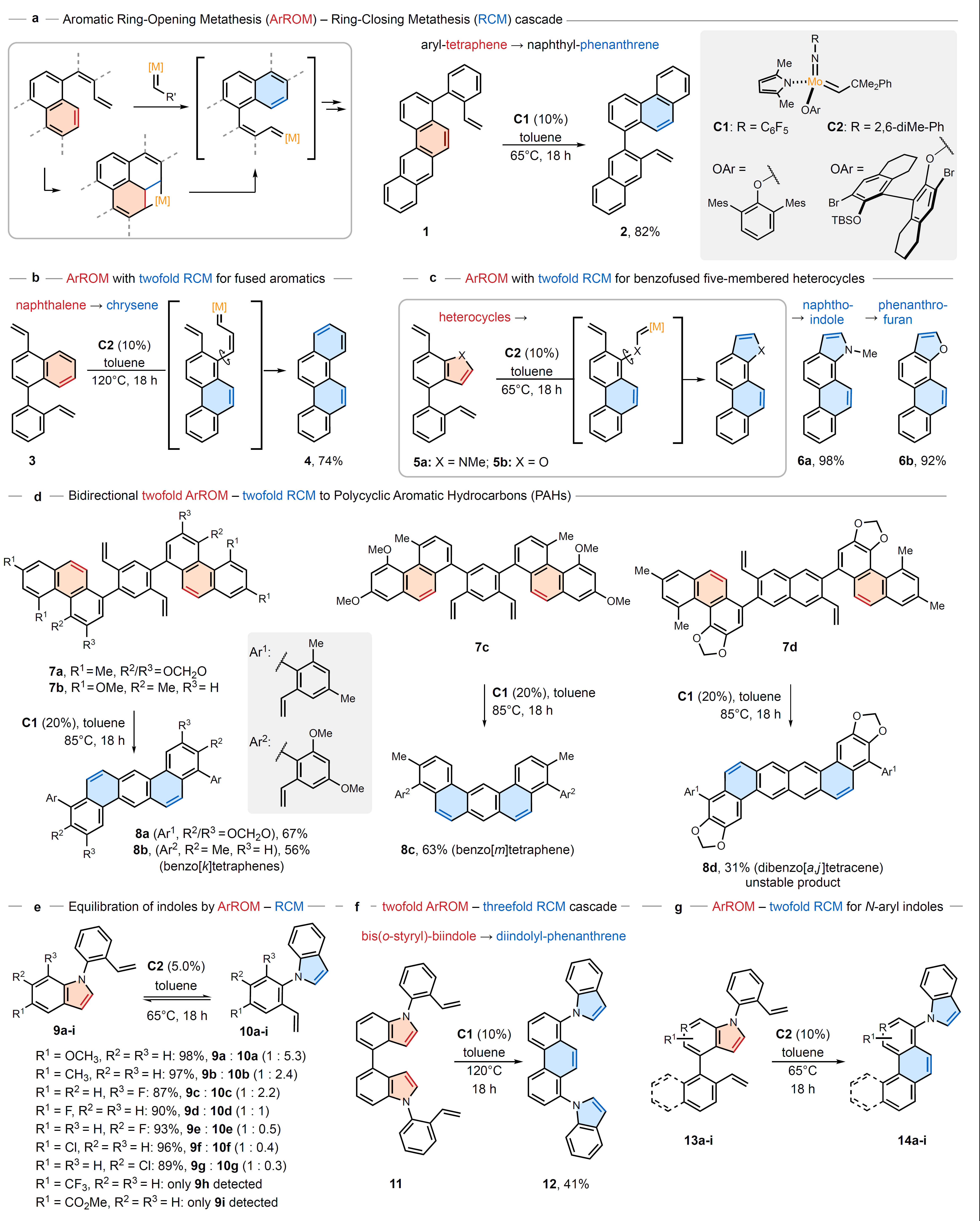
图2. 芳族开环复分解(ArROM)反应。图片来源:Nature
接下来,作者对吲哚裂解反应的可能性进行了研究(图2e),结果显示底物(9a-i)在ArROM条件下进行反应时生成了另一种N-o-苯乙烯基吲哚,并且该过程是可逆的,从而使得通过ArROM-RCM平衡吲哚成为可能。此外,作者还根据实验产生的取代吲哚(9a-i)及其相应构造异构体(10a-i)的平衡混合物对其稳定性进行了研究,结果表明:1)9d和10d在混合物中的比例为1:1,这说明氟取代基对二者相对的稳定性影响不大;2)含有供电子基团的吲哚(9a、9b)使得比例向其相应异构体(10a、10b)移动;3)吸电子基团取代的吲哚底物(9f-i)导致了相反的行为,同时底物(9c-e)的平衡揭示了取代模式的影响,这些结果表明吲哚底物参与的异构化机制与芳香族结构的异构化机制不同。如图2f所示,作者还探索了涉及多个芳香环开环和关环复分解步骤的复杂级联反应,即双-(邻苯乙烯基)-联吲哚11在C1(10 mol%)的催化下于120℃反应18 h后,能以41%的产率获得所需的二吲哚基菲12,该过程涉及双重ArROM和三重RCM。类似地,另一类吲哚底物也可实现ArROM与双重RCM级联反应(图2g),其中钌基Hoveyda-Grubbs II(HG-II)催化剂能以47%的产率获得所需产物14a,而钼催化剂C2则以优异的产率(96-98%)获得相应产物,同时该过程能实现112 mg规模制备(产率:97%)且C2的负载量低至2.0 mol%。值得一提的是,该方法对于带有供电子(14c)和吸电子基团(14b、d-f)的底物同样有效,即使是具有大位阻和氮杂吲哚核心的底物也可以顺利转化为相应产物14g和14h,尽管产率较低。
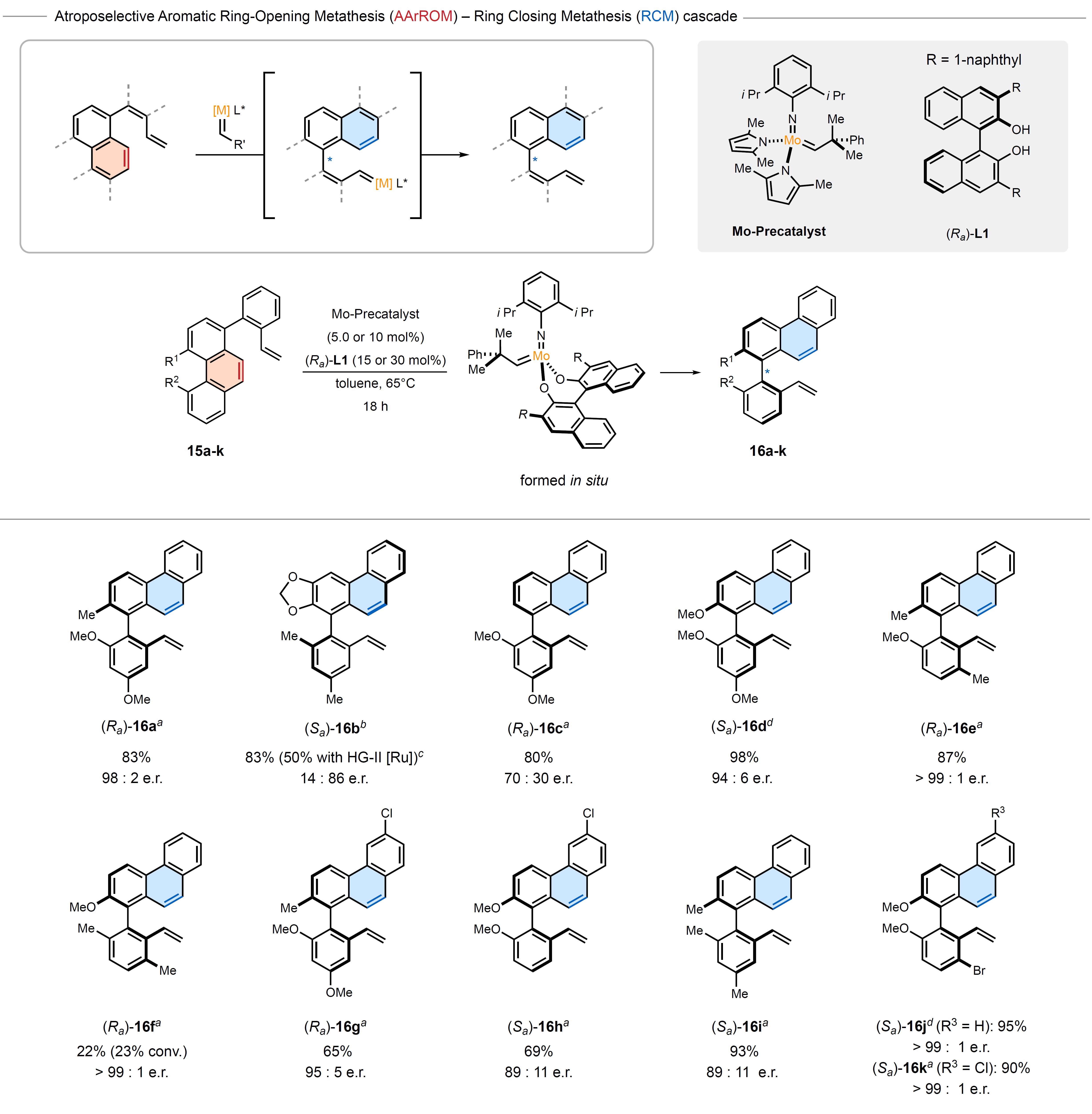
图3. 阻转选择性芳族开环复分解。图片来源:Nature
受立体选择性烯烃复分解开环反应的启发,作者尝试通过芳烃的阻转选择性芳族开环复分解(AArROM)反应来构建新型轴手性。具体而言:菲底物在手性催化剂的作用下控制立体轴的构型,并经芳烃开环反应产生极具挑战性的四邻位取代的芳香开环异构体。如图3所示,Mo-二吡咯前体与(Ra)-L1配体原位生成的手性催化剂能够有效催化菲底物15a的AArROM反应,并以98:2 e.r.值和83%的产率获得所需产物(Ra)-16a。类似地,一系列不同基团取代的菲底物均能兼容该反应,以中等至优异的阻转选择性(高达>99:1 e.r.)和产率(高达98%)获得相应产物(16b-k),尽管三取代菲的阻转异构体(Ra)-16c的选择性略有降低。值得一提的是,该方法对缺乏任何潜在配位取代基的底物15i也是有效的。

图4. 阻转选择性芳族开环复分解。图片来源:Nature
最后,作者研究了芳族体系的AArROM与双重RCM级联反应(图4a),发现一系列不同基团取代的菲底物(17a-i)均能以优异的阻转选择性(>99:1 e.r.)和良好至优异的产率(高达98%)转化为所需产物(18a-i),特别是产物(Sa)-18a(产率:97%、e.r.值:>99:1)还能以111 mg规模进行制备并且仅需5.0 mol%预催化剂(10 mol%(Ra)-L1)。另外,作者还通过产物(Sa)-18f的X-射线衍射分析确定其绝对构型。其次,该方法对于杂芳族体系的阻转选择性ArROM同样有效(图4b),具体而言:1)吲哚底物19a经ArROM进行动力学拆分后,以87:13 e.r.值和41%的产率获得所需产物20a,同时起始原料19a的对映体富集度仍为18:82 e.r.(s=15);2)通过动态动力学拆分(DKR),立体动力学底物19c和19d获得了明显较高的对映选择性(97:3 e.r.和96:4 e.r.)和产率(93%和91%),同时还通过化合物(Sa)-20d的微晶电子衍射(microED)分析确定其绝对构型。
总结
Christof Sparr教授课题组利用Schrock-Hoveyda型钼催化剂成功地实现了多种芳香族化合物(如:苯并蒽、萘、吲哚、苯并呋喃和菲)的开环复分解反应,包括不同的串联反应、杂环平衡、动力学拆分、多环芳烃 (PAH) 的双向合成、动态动力学拆分和由手性 Schrock-Hoveyda 钼亚烷基催化剂控制的高度阻转选择性转化。此外,该方法不仅拓展了过渡金属亚烷基催化剂的功能,而且芳族开环复分解反应为创造多种复杂多环芳烃开辟了新的途径。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Aromatic ring-opening metathesis
Valeriia Hutskalova, Christof Sparr
Nature, 2024, DOI: 10.1038/s41586-024-08472-z
(本文由吡哆醛供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
“出双入对”的妙处:Al(III)离子对催化的羰基-烯烃关环复分解反应 2020-10-14
-
Nat. Catal.:催化剂控制六重立体选择性 2021-06-15
-
北京大学焦宁团队Nature:芳环开环裂解制备烯基腈 2021-07-25
-
北京大学JACS:卡宾助力芳环开环 2024-05-11
-
Ring-Opening Metathesis Polymerization and Related Olefin Metathesis Reactions in Benzotrifluoride as an Environmentally Advantageous Medium.International Journal of Molecular Sciences (IF 4.9) Pub Date : 2022-12-30 ,DOI:10.3390/ijms24010671Ervin Kovács,Bence Balterer,Nguyen Anh Duc,Györgyi Szarka,Michael C Owen,Attila Domján,Béla Iván









































 京公网安备 11010802027423号
京公网安备 11010802027423号