南京大学郭子建院士/何卫江教授/陈韵聪教授团队CBMI | 通过亲脂性调控磺酰胺苯并噁二唑类荧光团实现内质网自靶向
英文原题:Tuning SBDs as Endoplasmic Reticulum Self-Targeting Fluorophores and Its Application for Zn2+ Tracking in ER Stress

通讯作者:郭子建,南京大学;何卫江,南京大学;陈韵聪,南京大学
作者:Ming-Feng Li (李明凤),Hao Yuan (袁昊), Shan-Kun Yao (姚善昆)
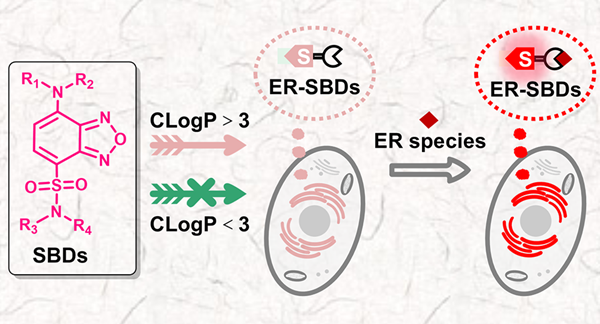
背景介绍
内质网(ER)的原位动态成像技术对于深入揭示与ER相关的病理生理机制及相互作用系统具有重要意义。然而,当前ER靶向成像策略尚不完善,且已开发的ER靶向探针大多依赖于小分子靶向基团。这些基团本身缺乏荧光特性,通常需要外接荧光团以实现可视化,从而在设计上多采用三模块构建策略(图1c)。相比之下,若荧光团本身具备内质网自靶向(ERST)能力,则可通过简单整合传感部分,构建出用于检测ER特定物种的探针(图1b)。这种双模块构建策略相较于三模块策略更为简洁高效,展现出广阔的应用前景。目前,仅有氟化罗丹明和苯并试卤灵被报道具有作为ERST荧光团的潜力(图1a)。然而,在实际应用中,这两种荧光团的传感部分常会对整个分子的ER靶向效果产生不利影响。因此,开发新型ERST荧光团策略显得尤为重要。本研究不仅揭示了磺酰胺苯并噁二唑(SBD)荧光母体作为ERST荧光团的巨大潜力(图1d),还提出了一种创新策略:通过调节SBD基荧光分子(SBDs)的亲脂性,来设计具有特定ER靶向特性的响应探针。这一策略为开发更高效、更精准的ER靶向成像探针提供了新的思路和方法。
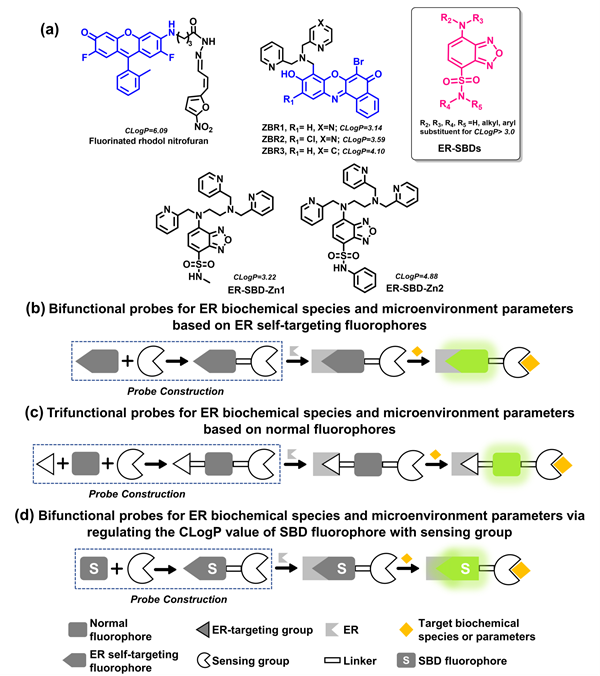
图1. (a)已报道的作为ERST荧光团的氟化罗丹明和苯并试卤灵的探针,以及新型内质网自靶向SBD荧光团(ER-SBDs,CLogP>3.0)和ER中Zn2+的荧光探针ER-SBDZn1和ER-SBDZn2;(b-d)设计用于ER中化学物种和微环境参数的荧光探针的不同策略:(b)基于内质网自我靶向荧光团的双功能策略,(c)基于普通荧光团的三功能策略,以及(d)通过调节带有传感部分的SBD荧光团的CLogP值来实现的双功能策略
文章亮点
近日,南京大学郭子建院士/何卫江教授/陈韵聪教授团队在期刊Chemical & Biomedical Imaging发表了题为“Tuning SBDs as Endoplasmic Reticulum Self-Targeting Fluorophores and Its Application for Zn2+ Tracking in ER Stress”的研究性论文。通过调节SBD母体的4位和7位取代基结构,合成了一系列具有不同CLogP值的SBDs,并研究了它们的ER靶向特性。
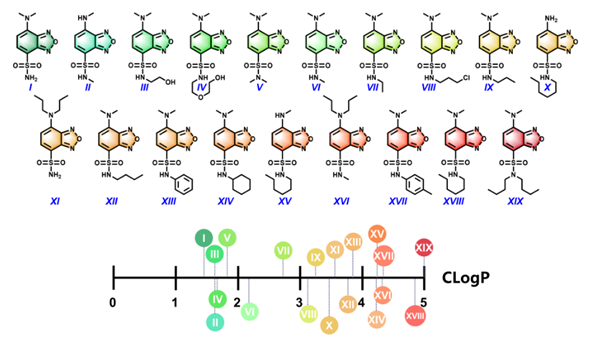
图2. SBDs的分子结构和对应的CLogP值
研究发现,仅当CLogP值大于3.0时,对应的SBDs才展现出ER靶向能力。鉴于CLogP值对SBDs的ER靶向性起着关键调节作用,本研究进一步据此设计了基于SBD的新型ER靶向锌离子探针。具体而言,通过将部分SBDs分子中4位的二甲胺基团替换为锌离子螯合团,成功合成了三例探针。研究结果显示,CLogP值小于3.0的SBD-TPEA探针表现出较差的ER靶向性。相比之下,CLogP值大于3.0的ER-SBD-Zn1和ER-SBD-Zn2探针则呈现出良好的ER靶向特性。这一发现不仅验证了通过调节CLogP值来控制SBDs ER靶向性的策略是切实可行的,而且为开发针对特定细胞器(如内质网)的高效离子探针提供了新的方向和策略。
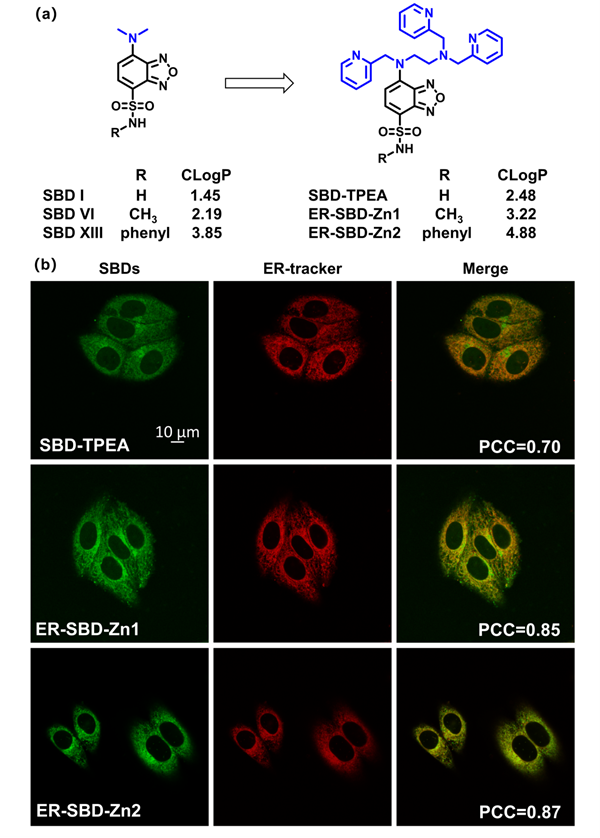
图3. (a)通过在SBD荧光探针上修饰锌离子传感基团来构建具有内质网靶向性的Zn²⁺探针;(b)在HepG2细胞中,ER-SBD-Zn1、ER-SBD-Zn2和SBD-TPEA与ER-Tracker Red的共定位实验
利用具有高灵敏度响应特性的ER靶向锌离子探针ER-SBD-Zn1,本研究深入探索了在衣霉素诱导的内质网应激(ERS)条件下,ER中游离锌离子的动态变化情况。实验结果显示,在遭受强烈的ERS时,ER中的游离锌离子浓度会迅速降低;而在经历轻度的ERS时,则观察到一个先升高后降低的过程。这一发现提示,ER中游离锌离子的初期增加可能代表了细胞对轻度ERS的一种补偿性反应,旨在通过调节锌离子稳态来应对内质网功能的紊乱。这些结果为理解ERS过程中锌离子稳态的调控机制及其在细胞应激响应中的作用提供了新的视角。
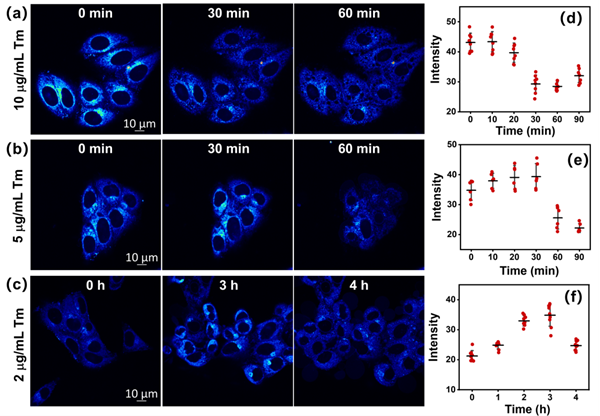
图4. HepG2细胞在不同孵育时间下与10 µg/mL (a)、5 µg/mL (b) 和2 µg/mL (c) 的衣霉素共同孵育的共聚焦图像;(d–f)为(a–c)中细胞的时间荧光特征曲线
总结/展望
基于对具有不同亲脂性的SBDs进行ER靶向性的深入研究,研究团队揭示了通过精细调控SBDs的CLogP值,可以设计出具有高效ER靶向性的SBD基荧光探针。这一发现为ER成像领域开辟了一种新颖的荧光团自靶向策略,为探索ER功能及相关疾病机制提供了一种强有力的辅助工具。在ER研究日益受到重视的今天,这一成果不仅拓宽了经典SBD荧光团的应用范围,更为其赋予了新的生命力和研究价值。
相关论文发表在高质量期刊Chemical & Biomedical Imaging上,南京大学博士研究生李明凤为文章的第一作者, 郭子建院士、何卫江教授和陈韵聪教授为通讯作者。
通讯作者信息
郭子建 教授
1999年获得国家自然科学基金委杰出青年基金资助,2001年被聘为教育部长江学者奖励计划特聘教授,2002年被评为享受国务院特殊津贴专家,2017年当选中国科学院化学部院士。曾任Chem. Soc. Rev., Inorg. Chem., J. Biol. Inorg. Chem., 期刊的编委,目前担任Coord. Chem. Rev., Dalton Trans., J. Inorg. Biochem., 等国际期刊的编委/顾问编委,以及《高等学校化学学报》、《无机化学学报》、Chem. Biomed. Imaging 等刊物的副主编、主编。主要研究领域为金属化学生物学,研究方向包括:无机药物化学、金属-生物大分子相互作用机制以及生物无机物种的荧光识别与检测等。
何卫江 教授
陈韵聪 教授
扫描二维码阅读英文原文,或点此查看原文

Chem. Biomed. Imaging 2024, ASAP
Publication Date: October 16, 2024
https://doi.org/10.1021/cbmi.4c00063
© 2024 The Authors. Co-published by Nanjing University and American Chemical Society
关于
Chemical & Biomedical Imaging


所有的稿件都将经过严格的、公平的、高效的同行评审,我们致力于以期刊的文章质量赢得读者的信任。如有任何疑问,请发送电子邮件至 eic@cbmi.acs.org


如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!









































 京公网安备 11010802027423号
京公网安备 11010802027423号