川大/华西/川农郭俊凌/童吉宇/杜晓:多酚骨架分子诱导多细胞组装用于肿瘤免疫治疗
细胞间相互作用在多细胞生物的生理过程中发挥着举足轻重的作用,涵盖免疫反应、代谢调节及疾病传播等多个方面。近年来,随着细胞表面工程技术的兴起,研究者们致力于精确调控细胞间的相互作用,以期推动细胞治疗与组织工程的蓬勃发展。当前,常见的细胞表面工程技术包括化学反应、代谢标记及电荷相互作用等,这些方法为细胞功能的拓展开辟了新的途径。
四川大学郭俊凌教授团队主要围绕植物多酚(又名单宁)在基础科学和交叉学科领域开展研究,发展了植物多酚高值转化体系(Science 2018; Nat. Nanotechnol. 2016; Matter 2023, 2024; Nat. Commun. 2022; Angew. Chem. 2024, 2023, 2019, 2014; Adv. Mater. 2024, 2023, 2020, 2013等)。近日,郭俊凌教授、华西第二医院童吉宇教授、四川农业大学杜晓教授共同组建了医工结合团队,成功开发了一种全新的细胞自组装策略。该策略通过铁离子FeIII与单宁酸(TA)构建的金属-多酚(MPN)网络,实现了对细胞的功能化修饰,进而构建出细胞1-细胞2组装体(CCA)。这一创新方法有效促进了细胞间的协作,为生物医学领域带来了全新的研究视角。MPN网络凭借其独特的相互作用力,如疏水相互作用、静电吸附、氢键和π-π堆叠等,使得功能化的细胞1(如金黄色葡萄球菌(S. aureus)、大肠杆菌(E. coli)、化脓性链球菌、干酪乳杆菌(L. casei)、白色念珠菌或T细胞)与细胞2(如单核细胞(MOs)、树突状细胞(DC)、NIH3T3和巨噬细胞(Mφ))能够任意组合,形成多种类型的CCA。这种模块化策略的多样性为细胞间相互作用的调节提供了无限可能。在癌症免疫治疗中,该团队通过L. casei@Mφ的组合,成功实现了不同细胞类型之间的多细胞合作,显著增强了癌症免疫治疗效果,对转移性肿瘤产生了强烈的抑制作用。这一研究成果不仅展示了多酚支架策略在调节细胞间相互作用方面的巨大潜力,还为多细胞自组织和基于细胞的疗法研究开辟了新的道路。该研究成果发表于国际纳米材料顶级期刊Small,文章的通讯作者为四川大学郭俊凌教授、童吉宇教授,四川农业大学杜晓教授作为重要合作者参与了该研究。文章的第一作者系四川大学轻工学院龚贵东副研究员(现陆军军医大学第二附属医院副研究员)、四川大学华西第二医院硕士尹啟敏和四川农业大学博士研究生刘琴玲。
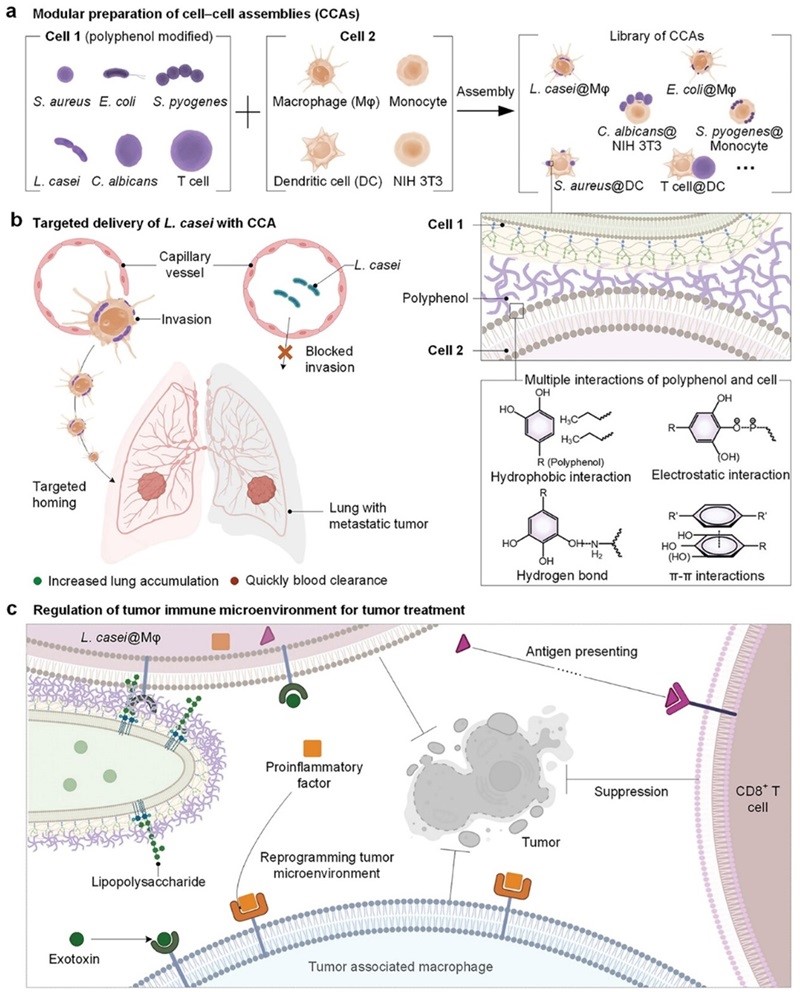
图1. CCA的模块化结构,以增强肺转移免疫治疗的细胞间合作
在这项研究中,该团队首先利用FeIII‐TA修饰细胞1(以L. casei为例),赋予其细胞亲和特性。随后,通过将L. casei与Fe3+处理的巨噬细胞Mφ充分混合,成功制备出L. casei@Mφ细胞组合。团队深入探究了L. casei@Mφ细胞组合的组装配比、表面形貌、肺转移肿瘤的侵袭能力和靶向递送性能。实验结果显示,在1000:1的进料速率下,CCA的组装率超过80%。该策略的一个关键创新点在于多酚(如TA)作为“细胞胶”的应用。多酚能够通过儿茶酚或没食子醇基团与细胞表面的生物大分子形成多种分子间相互作用,从而实现细胞间的紧密连接和协作。
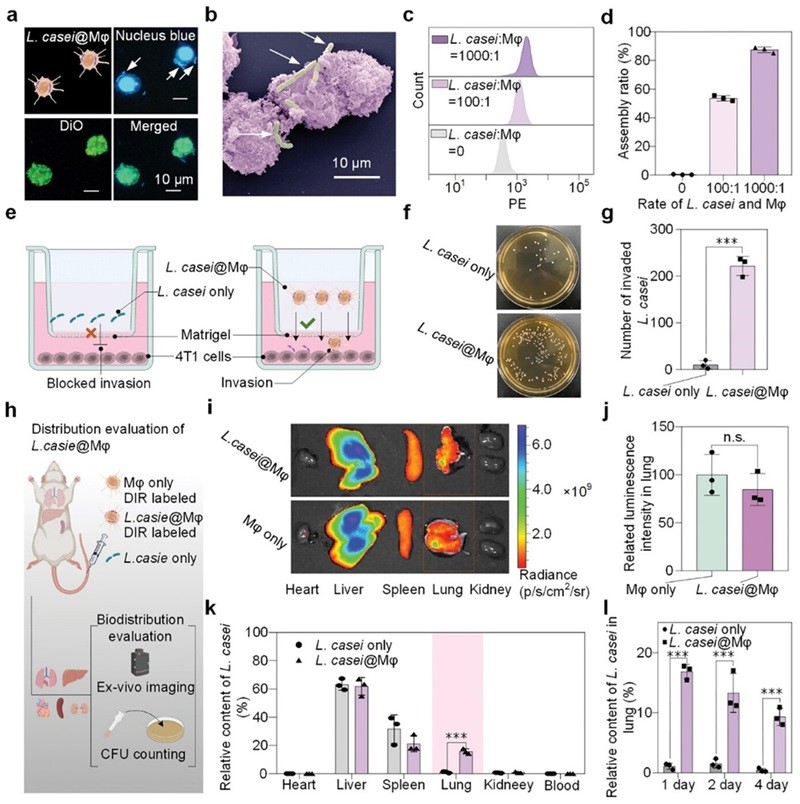
图2. 构建不同组合的CCAs,以及L. casei@Mφ促进了L. casei的肺蓄积
Mφ受细菌等外部因素诱导,可极化为经典激活的M1表型,分泌肿瘤坏死因子-α(TNF-α)等细胞因子。这些细胞因子能够杀灭肿瘤细胞,介导抗体依赖性细胞毒性及吞噬作用,导致血管损伤和肿瘤坏死,是肿瘤免疫治疗的关键。L. casei@Mφ中的干酪乳杆菌能有效诱导Mφ向M1表型极化,有望为多发性恶性肿瘤的治疗带来全新策略(图3)。
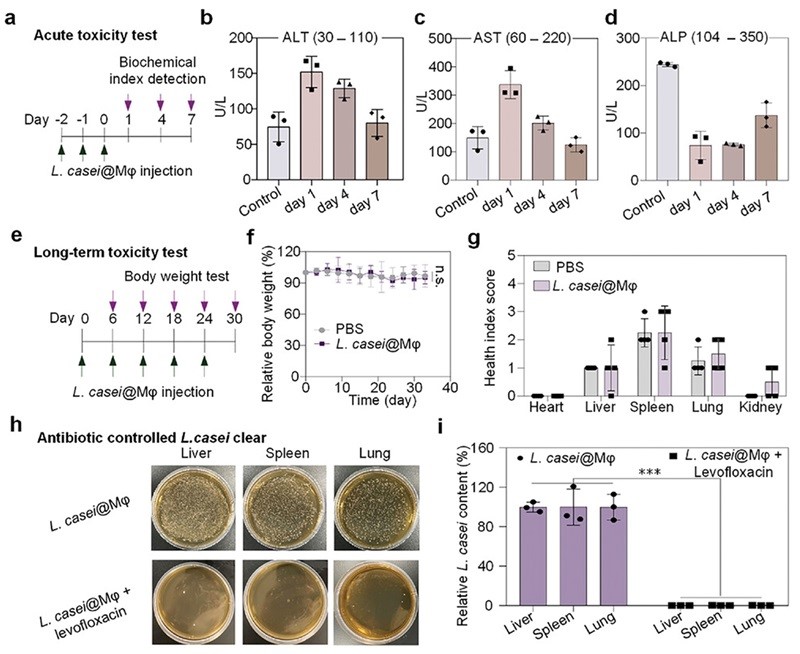
图3. L. casei@Mφ有效诱导内源性肿瘤相关Mφ的M1极化
该团队最终通过4T1转移性肿瘤小鼠模型验证了L. casei@Mφ的抗癌能力。L. casei@Mφ凭借增强肿瘤内M1 Mφ和CD8+ T细胞的浸润,成功将免疫抑制的肿瘤微环境转变为促炎状态,展现出显著的抗肿瘤效果。
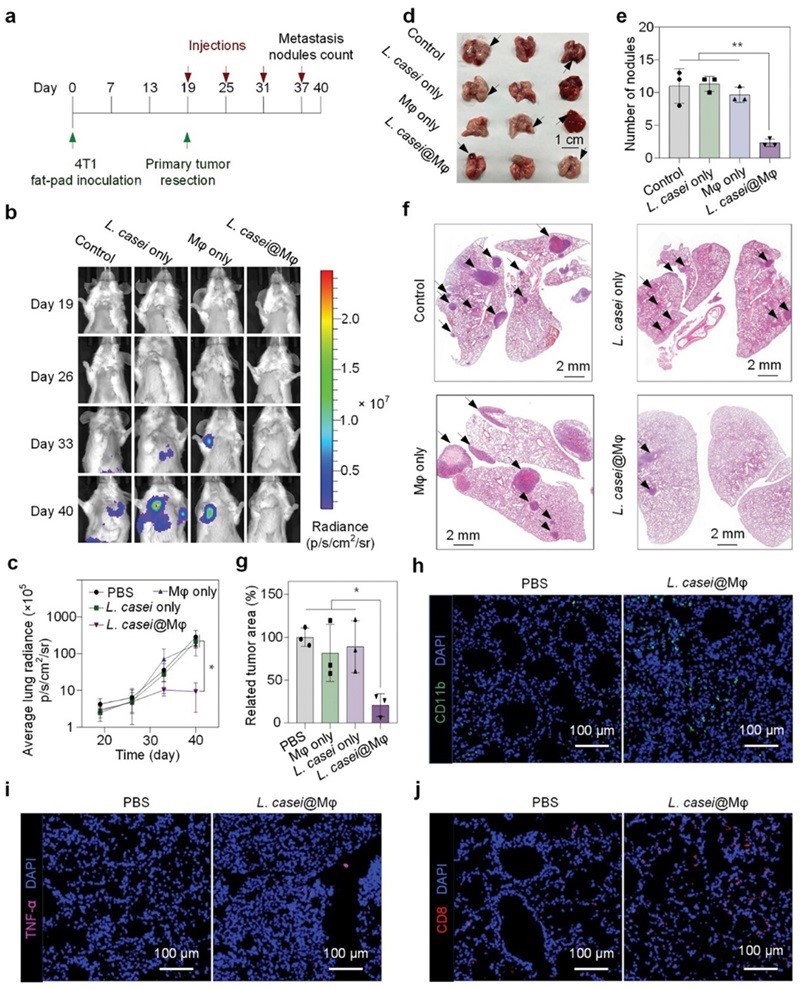
图4. L. casei@Mφ在体内高效激活抗肿瘤免疫,抑制转移性肺癌
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Polyphenol-Scaffolded Modular Assembly of Heterotypic Cell–Cell Assemblies for Potentiating Cancer Immunotherapy
Guidong Gong, Qimin Yin, Qinling Liu, Yajing Zhang, Jinyuan Liu, Mengyuan Dai, Jiawen Li, Xianglian He, Jiezhou Pan, Yunxiang He, Bo Wang, Jiyu Tong, Junling Guo
Small, 2024, DOI: 10.1002/smll.202408746
通讯作者简介

郭俊凌,皮革化学与工程教育部重点实验室副主任,四川大学教授,英属哥伦比亚大学客座教授,博士生导师,任教育部重大奖项/青年长江评委专家、全国学科评估专家、成都市委统战部“欧美同学会”副秘书长、新材料专委会部长、成都市工商联(总商会)专委会专家等。以项目或课题负责人承担国家重点研发计划、国家自然科学基金面上项目、四川省重点研发计划等,获得四川“天府峨眉”领军人才,苏州市/苏州高新区领军人才,成都市“蓉漂计划”领军人才,成都市高新区“产业教授”等。曾毕业于四川大学轻工学院(石碧院士、廖学品教授)、墨尔本大学(英国皇家学会院士、澳大利亚科学院院士Frank Caruso),哈佛大学(美国工程院院士、美国医学院院士Samir Mitragotri)。主要围绕植物多酚高值转化与跨领域应用研究,发展了吸附分离体系、药物精准递送体系、细胞工程化体系,共发表论文180余篇,其中以第一/通讯作者发表在Science、Nat. Nanotechnol.、Sci. Adv.、Nat. Commun.、Chem. Soc. Rev.、Matter、Angew. Chem.、Adv. Mater.、EES等国际顶级期刊,总被引8200余次,H指数46,申请及授权专利39项,关键技术已实现千万级产业转化。
课题组网站:
https://www.x-mol.com/university/faculty/65705

童吉宇,四川大学高层次引进人才、特聘研究员,入选四川省“高层次人才计划青年项目”、四川大学“双百人才B计划”、 四川大学基础法医学院“双十人才B计划”,获2021年 四川大学“学术新人奖”。四川大学华西第二医院、华西基础医学与法医学院表观遗传与免疫学实验室负责人。主要从事“T细胞功能的RNA和表观遗传调控”研究。近年来,已发表SCI论文10余篇;其中以第一或通讯(含共同)作者发表论文6篇,分别发表在Nature、Science Advances、Cell Research等国际权威期刊上,他引1000余次,研究成果入选F1000推荐论文和ESI高被引论文;担任Front Genet等国际知名学术期刊客座主编或编委。主持了包括国家自然科学基金面上、国家自然科学基金青年、四川省“天府峨眉计划”、中国博士后基金重点项目在内的多个国家级、省部级科研项目。
https://www.x-mol.com/university/faculty/353357

杜晓,四川农业大学教授,博士生导师,四川大学工学博士,日本广岛县立大学访问学者。任职中国茶叶学会审评专委会委员,中国茶叶学会审评教师,中国农促会茶叶专家委员会专家,国家乐山茶叶科技园首席专家,省茶业科学与工程重点实验室主任,《四川茶业》和《茶叶科学》编委等。主持部、省级科研2项,主研5项;先后在国外和国内15种公开出版的省部级刊物发表学术论文50余篇;自编教材4部。检索证实其中3个成分为世界上尚无报道的新化合物。申报国家发明专利5项,3项已实现落地转化,现均应用于实际生产。
研究团队:

团队网站:
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号