北化工谢文升/王兴/清华赵凌云Small:工程化自体外泌体纳米激动剂强化黑色素瘤放疗免疫治疗
黑色素瘤起源于黑色素细胞的恶性转化,是一种致命的皮肤癌,目前,治疗黑色素瘤的主要临床策略包括手术、放疗和免疫治疗。然而,由于免疫抑制的肿瘤微环境、免疫细胞的细胞毒性抵抗,以及在抗原处理和呈递过程中的病变,临床治疗过程出现治疗低应答率和不可避免的耐药性,这极大地限制了患者预后的改善。作为免疫原性最强的肿瘤之一,黑色素瘤的内在的可塑性使其能够在放疗过程中逃避免疫监视。因此,本研究设计了一种工程化的自体外泌体纳米激动剂MnExo@cGAMP,联合放疗级联激活cGAS-STING信号通路,阻断黑色素瘤免疫监视逃逸,提升放疗治疗结果。
1. MnExo@cGAMP级联激活cGAS-STING信号通路
MnExo@cGAMP具有高效的药物负载能力、靶向递送性能和出色的生物相容性。一旦被肿瘤细胞内化,释放的 Mn2+ 离子将增强干扰素基因刺激因子(STING)的结合,并使 GMP-AMP (cGAS)对放疗诱导的双链 DNA(dsNDA)敏感,从而在 X 射线照射的同时放大 cGAS-STING 通路的激活。同时,负载的 2′,3′-cGAMP 可作为次级信使直接增强通路的活性。这些 cGAS-STING 通路的级联激活可引发 I 型干扰素的过度表达,促进树突状细胞(DCs)成熟、抗原递呈和 CD8+ T 细胞活化,从而克服黑色素瘤的免疫抑制,达到有效的放射免疫治疗效果。

2. B16F10自体外泌体的制备流程及形貌表征
通过梯度离心、超声、膜挤压法可以连续、批量制备大小均一的MnExo@cGAMP外泌体,利用HRTEM观察到外泌体典型的磷脂双层膜结构,该结构揭示了超声处理后工程化自体外泌体的成功合成和完整的形态。

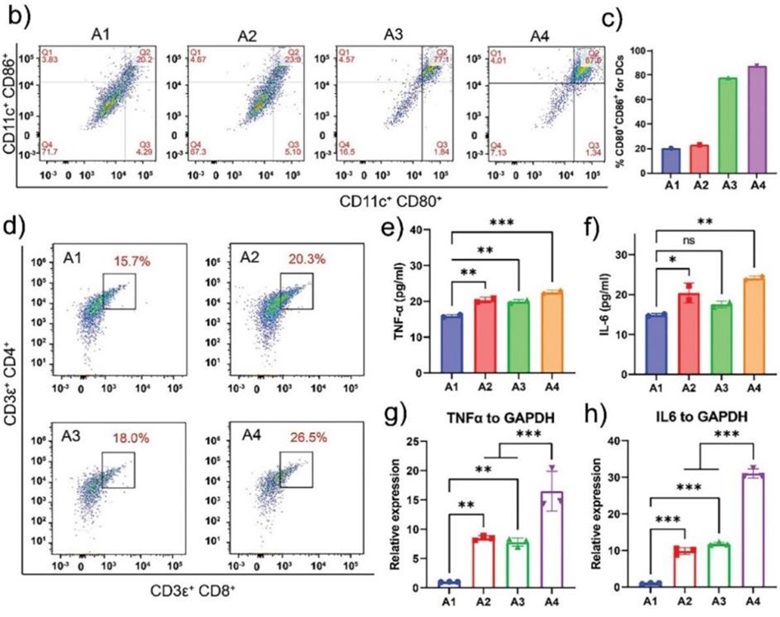
3. MnExo@cGAMP促进DC细胞成熟、抗原递呈以及T细胞的活化
MnExo@cGAMP释放 Mn2+离子将增加 cGAS 对肿瘤细胞的胞质 dsDNA 的敏感性,然后与2',3'-cGAMP 共同激活 cGAS-STING 通路以使DCs细胞成熟。与对照组相比,Mn2+和2',3′-cGAMP的联合处理极大地促进了DCs细胞的成熟,成熟率高达87.6%,高于单一药物处理组,同时联合治疗组CD8+ T细胞的绝对百分比为26.5%,与对照组(15.7%)相比显著升高。以上结果表明,Mn2+离子和/或 2',3′-cGAMP 治疗黑色素瘤可有效促进 DCs 成熟、抗原呈递和 T 细胞活化。
4. MnExo@cGAMP+RT联合治疗缓解黑色素瘤免疫抑制
MnExo@cGAMP联合放疗(RT)能显著促进CRT和HMGB1的释放,表明这种联合疗法对黑色素瘤具有免疫原性。此外,与其他组相比,MnExo@cGAMP联合低剂量X射线照射能增加肿瘤中细胞毒性T淋巴细胞(CTLs)的数量,显示出有效的免疫反应。同时,MnExo@cGAMP联合RT治疗还导致调节性T细胞(Foxp3+ CD4+ T细胞)数量增加,以维持治疗期间的免疫平衡。

小结
本研究展示了一种涉及金属免疫疗法和STING激动剂的靶向治疗方式,通过级联 cGAS-STING 通路激活进行有效的黑色素瘤放射免疫治疗。单独的传统放疗即使可以触发 dsNDA 的产生,也很难诱导免疫反应。然而,在 MnExo@cGAMP 被肿瘤细胞内化后,释放的 Mn2+离子将使 cGAS 对 dsDNA 敏感,并增强 STING 结合,与负载的 2′,3′-cGAMP 一起激活 cGAS-STING 通路。同时,外部辐射可以进一步增强 I 型 IFN 的产生,从而促进 DCs成熟、抗原呈递、T 细胞活化和最终的抗肿瘤免疫。总体而言,这种基于不同靶点的工程化自体外泌体显示出通过金属免疫疗法联合放疗克服黑色素瘤免疫疗法低响应率的独特潜力。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Engineering Autologous Cell-Derived Exosomes to Boost Melanoma-Targeted Radio-Immunotherapy by Cascade cGAS-STING Pathway Activation
Fangming Zhang, Ziyao Zhang, Wanting Yang, Zhuyuan Peng, Juntao Sun, Guofeng Li, Yen Wei, Xing Wang, Lingyun Zhao, Wensheng Xie
Small, 2024, DOI: 10.1002/smll.202408769
通讯作者简介
谢文升,北京化工大学副教授,入选北京化工大学青年后备人才、北京市优秀博士毕业生。主要研究领域为:(1)功能型可降解和全降解纳米材料在肿瘤热疗和动力学治疗中的应用;(2)新型纳米药物递送系统在肿瘤微环境免疫互作机制研究;(3)肿瘤细胞与生物界面的手性识别行为研究。已在Progress of Materials Science、Cell Reports Physical Science、Advanced Functional Materials、 ACS Nano、Advanced Science 等期刊发表第一作者/通讯作者论文20余篇,总被引2000余次,H-index为23,授权发明专利5项。担任中国生物工程学会干细胞与组织工程专业委员会青年委员,NSO和MedMat期刊化学科学青年编委,Materials和IJMS期刊专刊客座编辑。
课题组网站:
http://www.wangxing-lab.com/team_content.aspx?id=17199
https://www.x-mol.com/groups/xie_wensheng
王兴,北京化工大学教授,博士生导师。担任北京化工大学生命科学与技术学院教授科研副院长,北京市科委科技计划项目会评专家,智利国家科学与技术委员会外籍项目函评专家,著名国际期刊AM、NC、AFM、Small、ACS AMI 等30多个期刊的审稿人。主要从事生物医用材料在抗菌、止血和药物递送领域的基础研究与应用,在“立体化学抗菌”领域做出重要贡献。主持国家自然科学基金、北京重点专项(首席科学家)、领域基金、基础研究、外专项目和企业技术开发项目等23项。发表SCI论文80余篇,h指数32。授权发明专利20件,转让2件。
课题组网站:
http://www.wangxing-lab.com/team_content.aspx?id=4694
https://www.x-mol.com/university/faculty/76476
赵凌云,清华大学材料学院副研究员。主要研究领域涉及纳米材料、生物材料、肿瘤综合诊疗、分子自组装等方面。曾获清华大学优秀博士后、中国仪器仪表学会科技成果奖、清华大学刘述礼育才奖、2024年度清华大学优秀班主任一等奖、第八届中国国际“互联网+”大学生创新创业大赛金奖指导教师。作为项目负责人主持各类国家及省部级项目,在Adv. Mater, ACS Nano, Adv. Funct. Mater, Biomaterials 等国际期刊发表论文100余篇,连续七年入选生物医学工程领域Elsevier中国高被引学者。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
具有“独立模块/级联功能”的工程化外泌体,通过多步靶向和多环节干预治疗帕金森病 2022-05-07
-
北化工王兴/谢文升/清华赵凌云ACS AMI:胞内ROS过表达调节药物诱导细胞坏死性凋亡 2024-04-15
-
Epigenetic nanoplatform for synergistic immune activation and immunogenicity restoration enhancing cancer radio-immunotherapyZhenhu He, Xiaopei Peng, Jiong Li, Yaning Zhu, Xuan Zhang, Junhong Duan, Jing Ni, Mengtian Ma, Juan Wang, Zhenguo Liu, Bin Feng, Wenbin Zeng, Chao Liu, Xiaolong Qi, Pengfei Rong
-
Engineering Semiconducting Polymeric Nanoagonists Potentiate cGAS-STING Pathway Activation and Elicit Long Term Memory Against Recurrence in Breast CancerHaitao Yuan, Chong Qiu, Xiaoxian Wang, Peili Wang, Letai Yi, Xin Peng, Xiaolong Xu, Wei Huang, Yunmeng Bai, Jinxi Wei, Jingbo Ma, Yin Kwan Wong, Chunjin Fu, Wei Xiao, Chunbo Chen, Ying Long, Zhijie Li, Jigang Wang
-
Boosting ubiquitin-proteasome system-mediated androgen receptor degradation and cGAS-STING pathway activation for synergistic prostate cancer therapy by engineered zinc-manganese oxide nanoparticlesLinnan Yang, Yi Hu, Hui Peng, Zhengbin Wang, Sixu Chen, Jieying Qian, Yujie Yang, Zhonghua Xu, Jin Wu, Chaozhao Liang, Guilong Zhang, Yunjiao Zhang, Li Zhang



































 京公网安备 11010802027423号
京公网安备 11010802027423号