南开大学等四单位联合JACS:单原子纳米酶轴向氯化工程Fe-N4Cl催化位点用于高效过氧化物酶模拟
纳米酶是一种具有类酶特征的纳米材料,有效地结合了天然酶和纳米材料的优点。然而,纳米酶较低的动力学和催化效率阻碍其进一步应用。因此,开发高效纳米酶并探索其医学应用具有重要意义。近年来,金属单原子位点催化剂表现出优异的催化活性和选择性。然而,对称的金属-N4位点不利于催化过程中对中间体的吸附。此外,金属-N4位点的刚性结构不利于优化催化位点的几何构型和电子分布。因此,打破金属-N4位点的几何对称性有望进一步提高其类酶活性。轴向氯化工程是一种简单、合理、可控的策略,然而其在单原子纳米酶的领域仍处于空白阶段,其结构与类酶活性之间的构效关系尚未研究报道。
近日,南开大学张冀杰副教授、中国科学院生物物理研究所高利增研究员、美国西北大学王翕君博士、首都师范大学陈郑博副教授团队联合在Journal of the America Chemical Society 上发表研究论文,首次提出了Fe-N4Cl催化位点的轴向氯化工程 (Fe-N4Cl/CNCl)。与传统的具有Fe-N4催化位点的Fe-N4/CN单原子纳米酶相比,Fe-N4Cl/CNCl单原子纳米酶对过氧化物酶底物3,3',5,5'-四甲基联苯胺(TMB)具有更强的类过氧化物酶活性,最大反应速度(Vmax)为4.73×10−5 M min−1,催化常数(kcat)为246.4 min−1,比活性为81 U/mg,分别是Fe-N4/CN单原子纳米酶的4.9倍、3.9倍和2.7倍,揭示了轴向氯化工程在提高单原子纳米酶类酶活性方面的显著潜力。与Fe-N4/CN单原子纳米酶相比,Fe-N4Cl/CNCl单原子纳米酶在体外和体内抗肿瘤治疗过程中均显著抑制肿瘤细胞的生长。密度泛函理论(DFT)计算表明,与Fe-N4位点相比,Fe-N4Cl位点能够促进•OH自由基的释放,降低决速步(RDS)的能垒,从而提高反应速率。这项工作揭示了单原子纳米酶的轴向氯化工程在提高其类酶活性方面有巨大的优势,在肿瘤治疗中具有广阔的应用前景。论文第一作者为魏盛杰、孙敏敏、黄娟。

图1. (a) Fe-N4Cl/CNCl单原子纳米酶的合成过程示意图。灰球、蓝球、红球和绿球分别代表C、N、Fe和Cl原子。(b,c) Fe-N4Cl/CNCl单原子纳米酶的HAADF-STEM图像和相应的EDX结果。(d) Fe-N4Cl/CNCl单原子纳米酶的AC-STEM图像。(e,f) Fe-N4/CN单原子纳米酶的HAADF-STEM图像及相应的EDX结果。(g) Fe-N4/CN单原子纳米酶的AC-STEM图像。
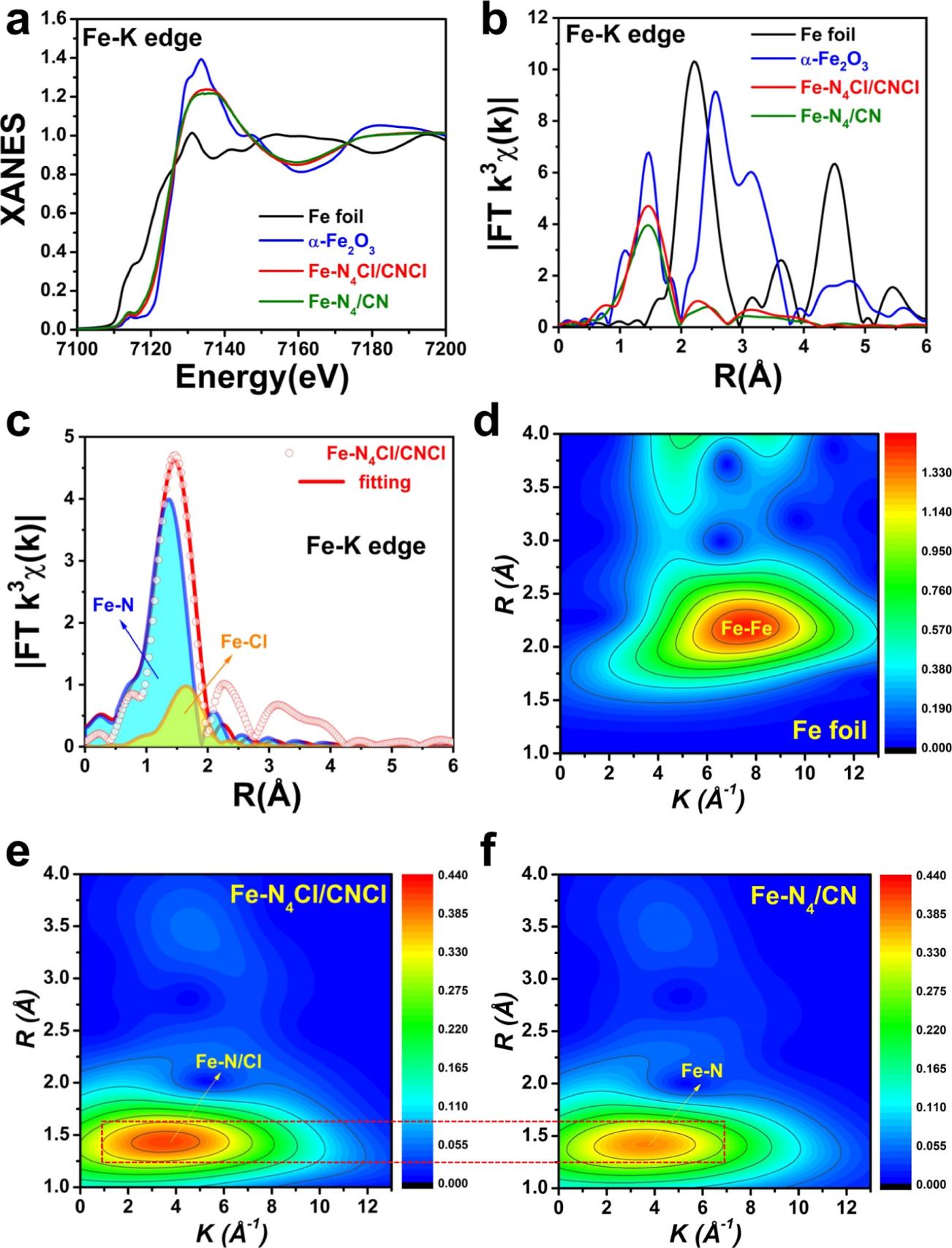
图2. (a,b) Fe-N4Cl /CNCl和Fe-N4/CN单原子纳米酶、Fe箔和α-Fe2O3的XANES光谱和相应的FT-EXAFS结果。(c) Fe-N4Cl/CNCl单原子纳米酶在R空间的拟合结果。(d-f) Fe箔、Fe-N4Cl/CNCl和Fe-N4/CN单原子纳米酶的小波变换分析。
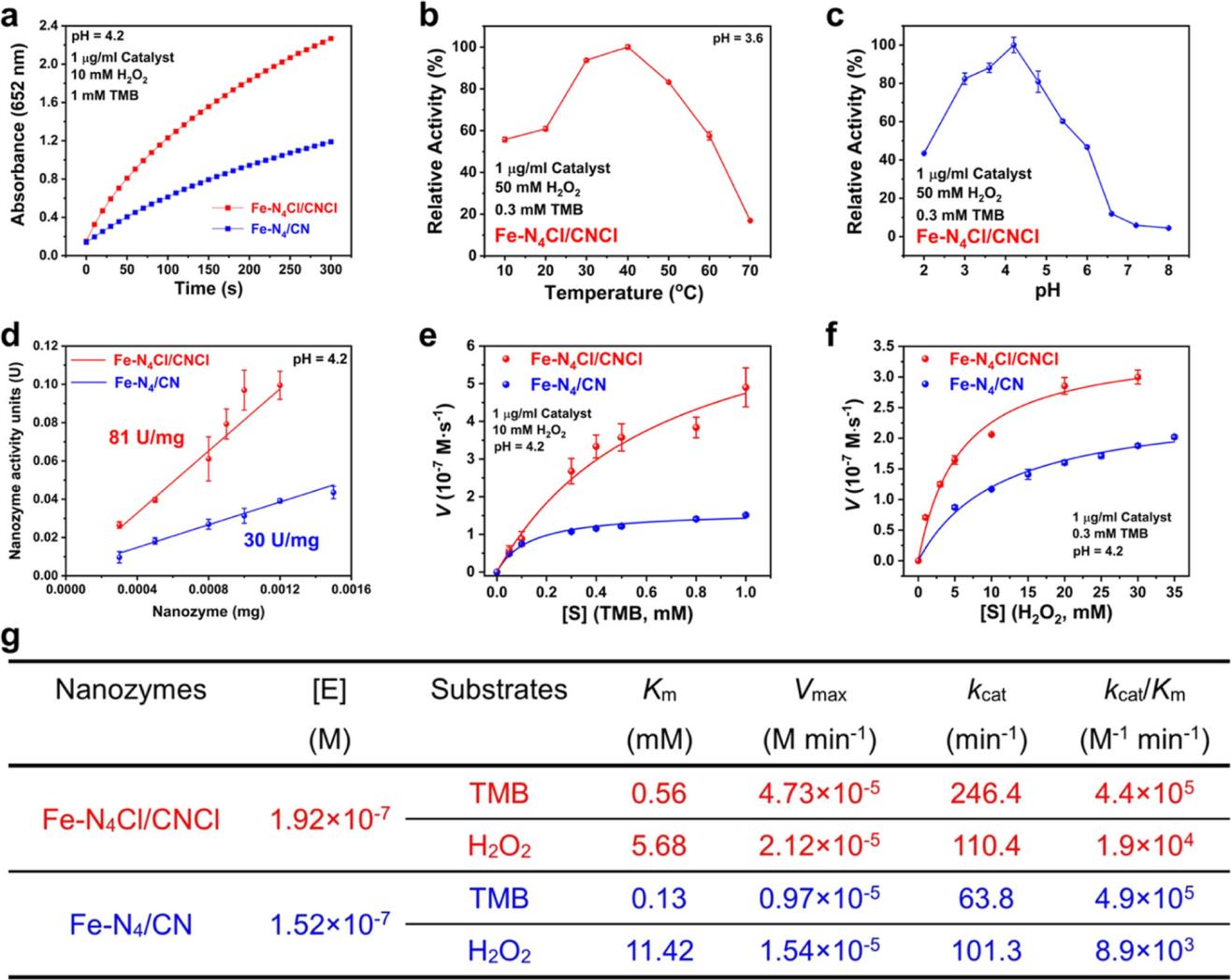
图3. (a) Fe-N4Cl/CNCl和Fe-N4/CN单原子纳米酶催化TMB比色反应的反应时间曲线。(b,c) Fe-N4Cl/CNCl单原子纳米酶催化TMB比色反应中催化温度和pH值的影响。(d) Fe-N4Cl/CNCl和Fe-N4/CN单原子纳米酶的比活性比较。(e,f) 分别用普通最小二乘法拟合不同浓度TMB和H2O2的Michaelis-Menten曲线。(g) Fe-N4Cl/CNCl和Fe-N4/CN单原子纳米酶的Fe活性位点动力学比较。[E]为Fe活性位点的摩尔浓度。Km是Michaelis常数。Vmax是最大反应速度。kcat (kcat = Vmax/[E])为催化常数。kcat/Km值反映了单原子纳米酶的催化效率。
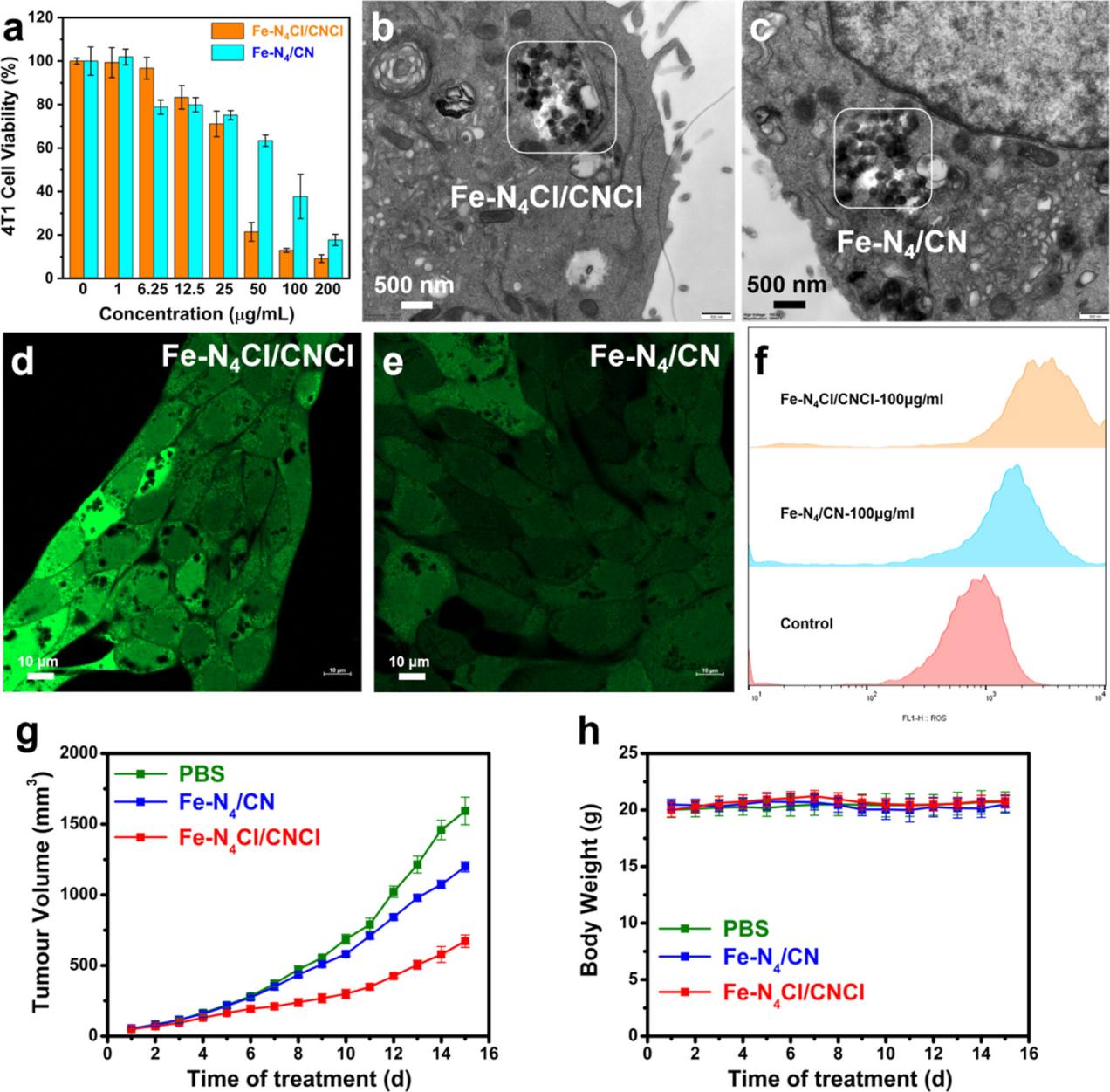
图4. (a) 不同浓度Fe-N4Cl/CNCl和Fe-N4/CN单原子纳米酶培育4T1细胞后的细胞活力。(b,c) Fe-N4Cl/CNCl和Fe-N4/CN单原子纳米酶被吞噬的TEM图像。(d,e) 分别用Fe-N4Cl/CNCl和Fe-N4/CN单原子纳米酶处理4T1细胞后,细胞内的ROS水平。(f) 流式细胞术检测100 μg/mL Fe-N4Cl/CNCl单原子纳米酶、Fe-N4/CN单原子纳米酶处理的4T1细胞及对照组细胞内ROS水平。(g) 4T1荷瘤小鼠治疗15天肿瘤体积变化。(h) 4T1荷瘤小鼠治疗15天期间体重变化。
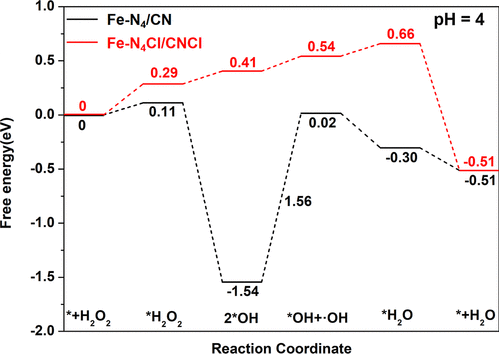
图5. Fe-N4和Fe-N4Cl催化位点催化H2O2活化相应的能量变化。
小结
本文要点在于:(一)首次提出了Fe-N4Cl催化位点的轴向氯化工程(Fe-N4Cl/CNCl),与传统的具有Fe-N4/CN的单原子纳米酶相比,表现出更优越的类过氧化物酶活性。(二)Fe-N4Cl/CNCl单原子纳米酶催化的最大反应速度(4.73×10−5 M min−1),催化常数(246.4 min−1),比活性(81 U/mg)分别是Fe-N4/CN单原子纳米酶的4.9倍,3.9倍,2.7倍,揭示了单原子纳米酶的轴向氯化工程在提高类酶活性上具有巨大优势。(三)Fe-N4Cl/CNCl单原子纳米酶在体内外均表现出增强的抑制肿瘤细胞生长的作用。(四)理论计算结果表明,与Fe-N4催化位点相比,Fe-N4Cl位点更有利于释放•OH自由基,降低决速步能垒,从而加快反应速率。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Axial Chlorination Engineering of Single-Atom Nanozyme: Fe-N4Cl Catalytic Sites for Efficient Peroxidase-Mimicking
Shengjie Wei, Minmin Sun, Juan Huang, Zhengbo Chen*, Xijun Wang*, Lizeng Gao*, Jijie Zhang*
J. Am. Chem. Soc., 2024, DOI: 10.1021/jacs.4c13335
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号