Chem Catal.:级联反应实现C-核苷的生物催化合成
C-核苷作为抗感染药剂以及治疗性核酸的组成砌块,是一类重要的合成目标分子。然而,已报道的C-核苷合成方法面临原料来源受限、产率低、反应范围小等挑战。针对该难题,来自奥地利格拉茨工业大学的Bernd Nidetzky教授研究团队近日在Cell Press细胞出版社旗下期刊Chem Catalysis 上发表研究论文,发展了一种基于磷酸化-缩合的级联反应策略,利用D-核糖(Rib)以及尿嘧啶作为原料制备假尿苷5'-磷酸(Ψ5P)。级联过程包括Rib在偶联激酶催化下于O5位发生磷酸化生成Rib5P中间体,并进一步与等摩尔当量尿嘧啶缩合定量转为Ψ5P。借助于条件优化,该反应可实现Ψ5P的克级别合成,并在多元酶促级联反应用于高效制备C-核苷类似物方面展现出优异的合成兼容性。
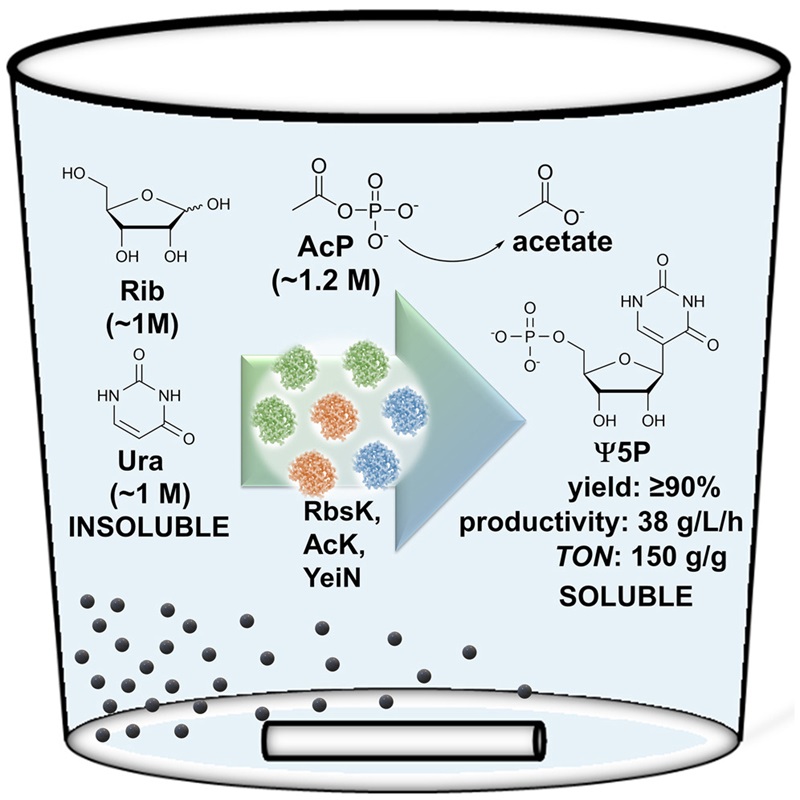
研究亮点
低成本:磷酸化-缩合级联反应合成Ψ5P利用Rib和尿嘧啶原料,来源广泛、成本低廉。
高性能:通过偶联激酶和C-糖苷酶,实现了Ψ5P一锅法合成,产率接近定量,且具有较高的空间和化学选择性。
可放大:结合生物催化和反应工程,优化条件,显著提高了Ψ5P合成效率,实现宏量制备。
可兼容:一锅法将多类五碳糖和尿嘧啶类似物原料合成相应的C-核苷类似物。
研究背景
假尿苷(Ψ)是尿苷(U)的天然C-糖苷异构体,存在于多种RNA类型中(图1A)。Ψ及其1-N-甲基衍生物是合成RNA的构建砌块,可应用于mRNA治疗技术中。RNA治疗技术的发展使得对Ψ的需求不断增长,学界和产业界对其合成的关注也随之增加。尽管已有多种化学合成Ψ的方法,但仍存在立体选择性、效率和步骤经济性等方面的挑战。在水作为溶剂时Ψ5P的合成已实现定量,因而实现Ψ5P合成反应的主要挑战在于高效制备Rib5P底物用于C-糖苷酶的酶促反应(图1B)。尽管目前已有研究关注Rib5P的合成,但多反应步骤互不兼容,难以实现一锅反应;此外合成原料来源受限,经济性堪忧。例如,利用U与α-D-核糖-1-磷酸盐反应得到Rib5P并进一步转化为Ψ5P,优化条件下具有高产率(~100%)、高产物浓度(~320 g/L)、高产量(~40 g/L/h)和产物纯度(≥ 95%)等优点(图1C)。然而,U并非成熟的商业原料。在此背景下,利用方便可得的Rib和Ura作为原料则可降低Ψ5P的生产成本。
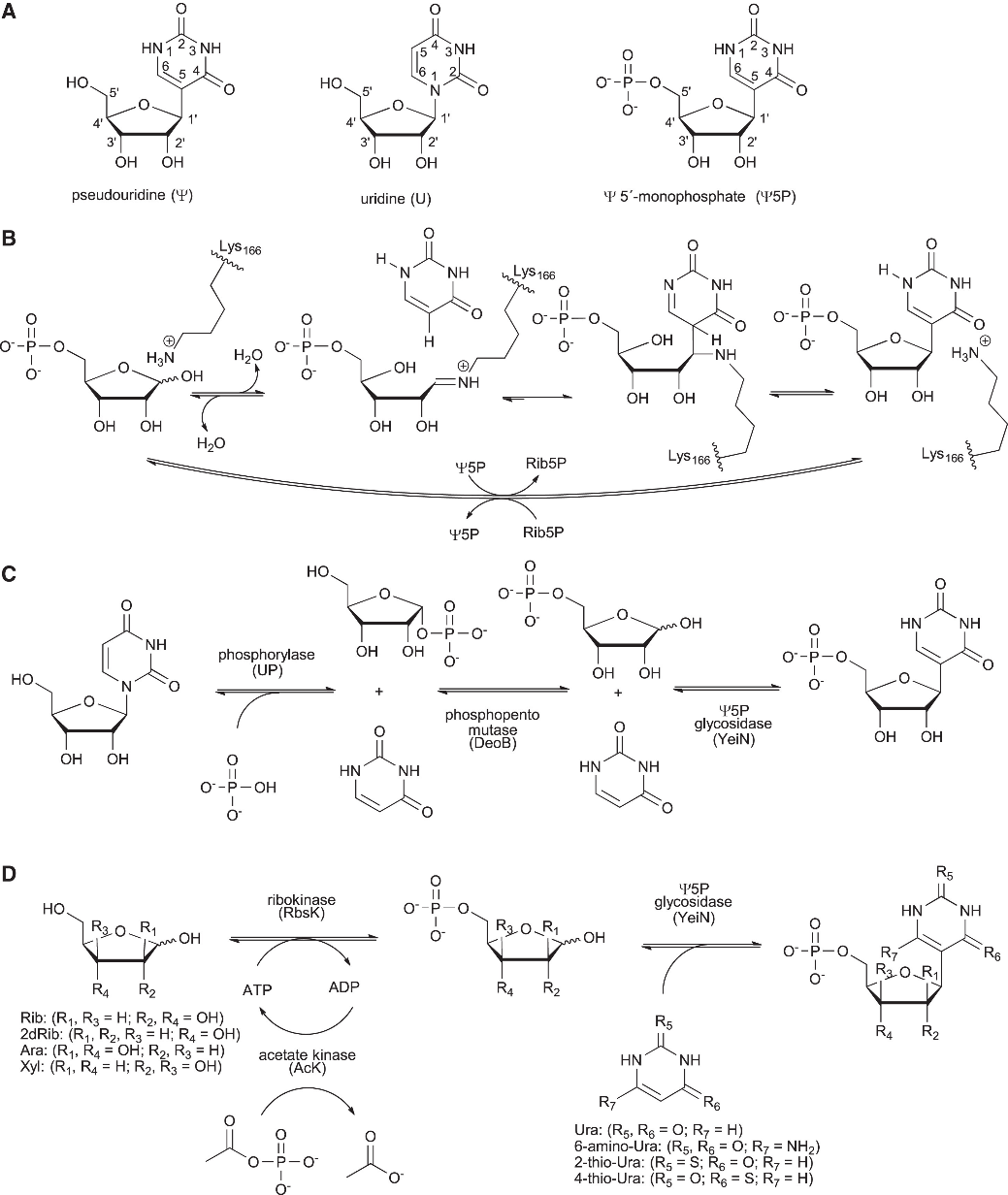
图1. Ψ5P的酶催化合成
基于以上分析,作者系统评估了以五碳糖和尿嘧啶类似物为原料进行磷酸化-缩合级联反应的各个步骤。针对磷酸化反应,考察了磷酸酶和激酶催化的反应,讨论并确认了乙酰磷酸(AcP)作为磷酸供体的有效性。进一步地,通过生物催化与反应工程的结合,将磷酸化反应和缩合反应成功集成,一锅法高效合成Ψ5P。该过程的反应边界远远超出(30倍)了核碱基可溶性底物浓度的极限,并最大限度地利用了AcP供体。除此之外,多种N-核苷也通过磷酸化-缩合级联反应得以合成。
结果与讨论
1. 磷酸化反应合成Rib5P
首先,作者尝试了由磷酸酶催化的磷酸化反应,采用多种生物来源的磷酸酶,借助AcP作为磷酸供体底物进行研究。然而,产物的核磁共振NMR图谱结果显示,当AcP完全转化时,D-核糖-1-磷酸盐与Rib5P的产量相近,表明磷酸酶催化的Rib磷酸化反应不具有选择性,这可能是由于磷酸酶缺乏对Rib的位点选择性(图2A)。随后,作者选取对Rib O5位点具有选择性的RbsK反应合成Rib5P,并偶联AcK反应实现ATP的再生(图1D)。该反应通过激酶催化,在水相pH 7.5和30°C的条件下进行,ATP将Rib磷酸化,以高产率(≥ 90%)得到Rib5,该条件是两种激酶和C-糖苷酶的综合最适条件(图2B)。
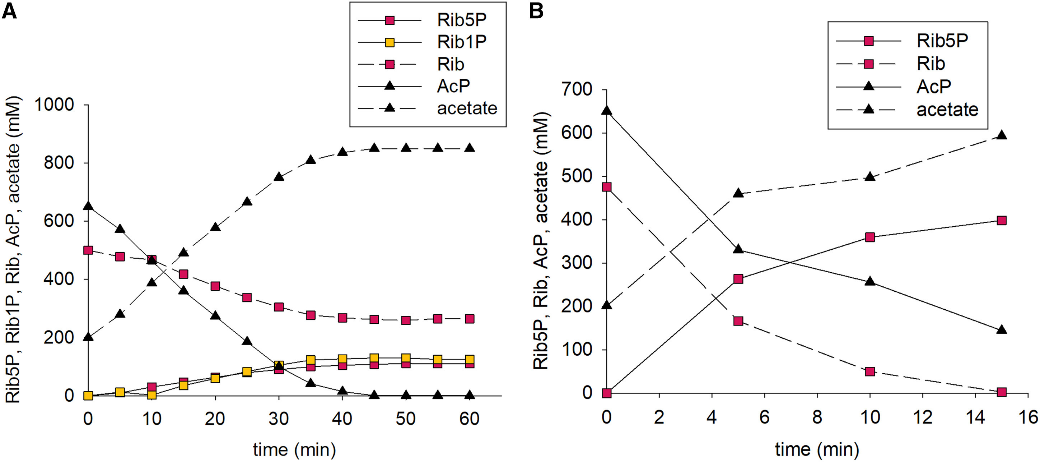
图2. Rib磷酸化反应的筛选:使用磷酸酶或激酶的对应反应效率
在确认偶联激酶反应为实现磷酸化的有效反应类型后,作者进一步通过调整底物浓度以及Mg2+浓度(反应所使用两种激酶的辅因子),将磷酸化反应的效率显著提高。当Rib浓度调整至~ 1M时,其转化率高达约97%(图3A);而当调节Mg2+至接近其饱和浓度(~ 60 mM)时,Rib5P的生成速率提升了约20倍。值得注意的是,尽管AcK和RbsK在反应中逐渐失活,但通过反应的快速转化可最小化酶失活带来的影响。在优化条件下,Rib5P的生产速率可达150 g/L/h,且基于质量的总转化数超过1.5×102 g/g(图3B)。
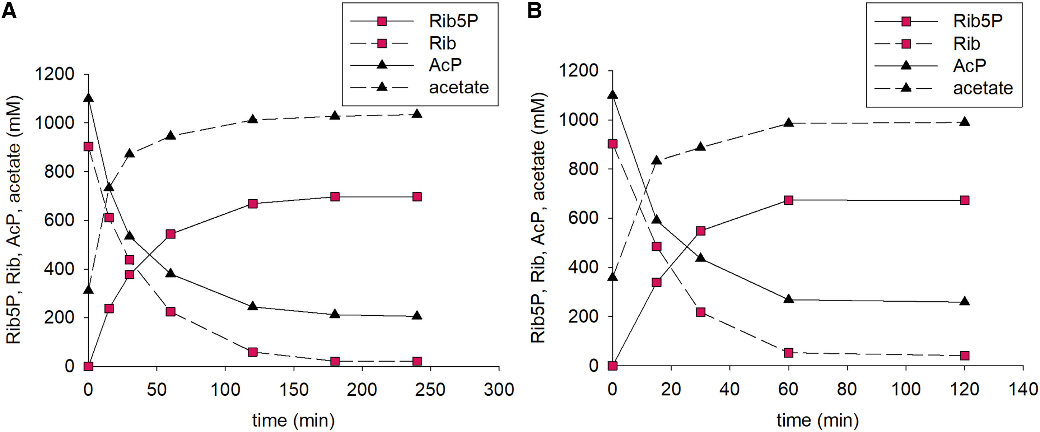
图3. 优化耦合RbsK和AcK反应实现Rib5P高效合成
2. 酶催化C-C缩合实现Ψ5P合成的反应工程
在优化Rib经磷酸化合成Rib5P反应后,作者紧接着对级联反应中涉及的C-C缩合进行系统探究。研究中使用来自于大肠杆菌的C-糖苷酶YeiN,该酶在Rib5P反应体系中可维持其反应活性,无需额外添加Mn2+就可实现Rib5P与Ura的C-C缩合反应。考虑到Ura在水中的溶解度是反应中所使用Rib5P浓度的约1/30,研究人员采取分步加入Ura的投料策略,单次投入量在50-670 mM之间,并施加搅拌以联合克服溶解和传质限制。通过调节使用YeiN酶的浓度,使Ura与Rib5P缩合转化生成Ψ5P的产率超过97%,产量高达52 g/L/h(图4)。
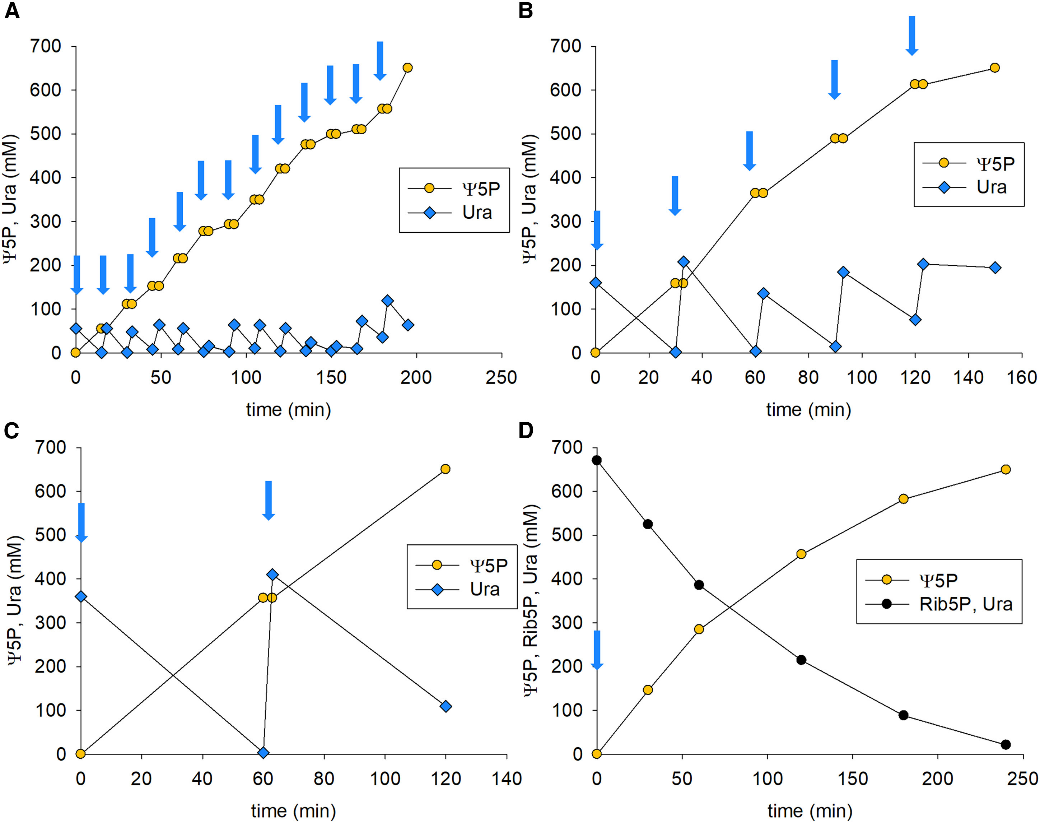
图4. 固体Ura存在条件下对Ψ5P生产的强化
3. 一锅法反应的放大
随后,作者将一锅法反应量级从0.5 mL扩大20倍至10 mL量级(图5),发现无论是顺序反应还是同时反应,级联反应中的磷酸化步骤与缩合步骤均可兼容,但由于同时反应条件下YeiN的活性受到碱性环境的影响使得产率下降约30%(图6)。优化条件下,在10 mL反应体积中可获得约2.2 g的Ψ5P,产量可达到38 g/L/h。
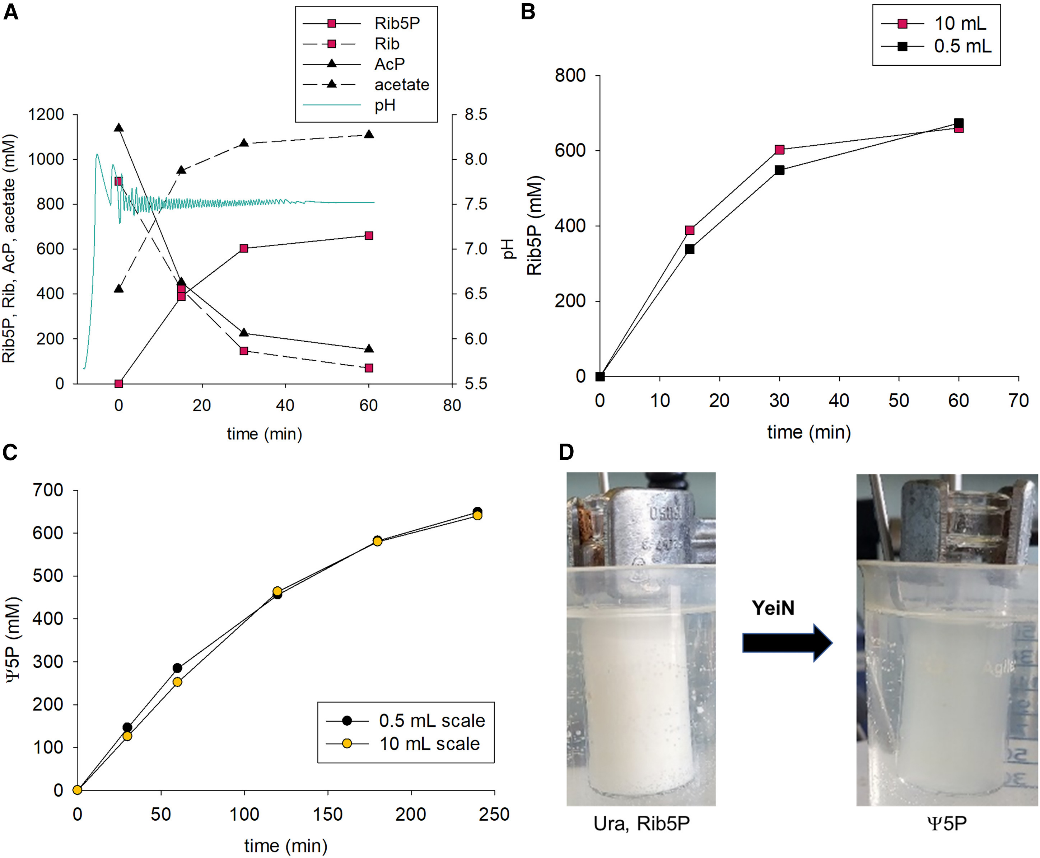
图5. 用于合成Ψ5P的磷酸化-缩合级联反应的放大化
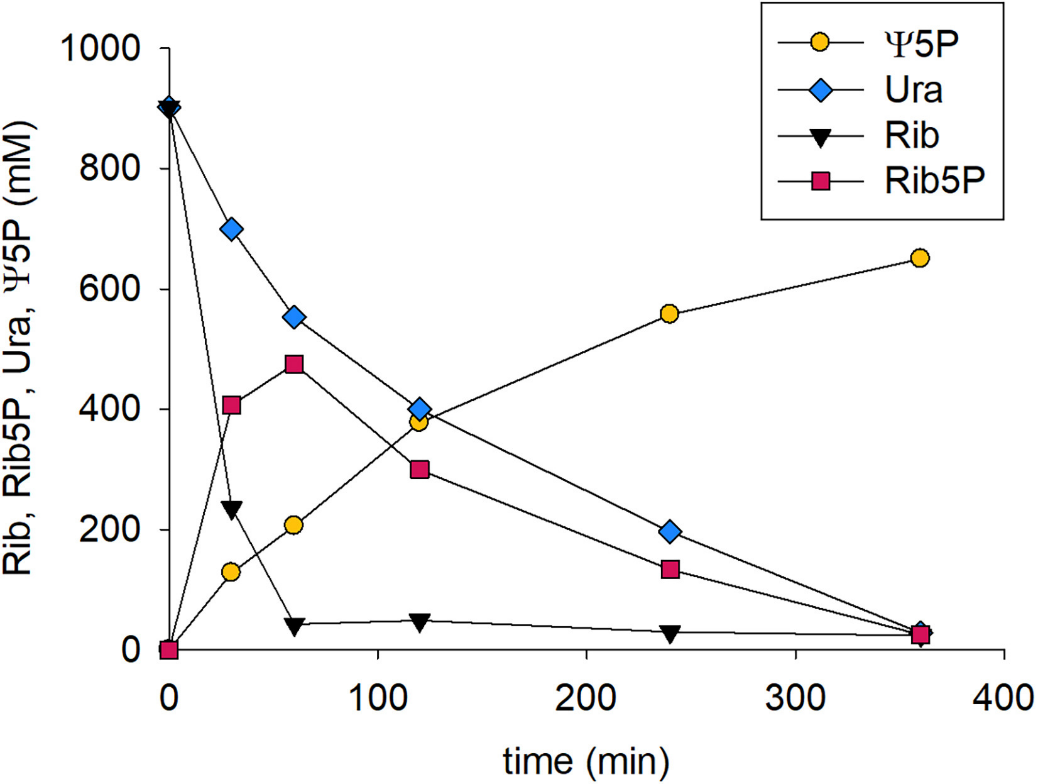
图6. 同时反应模式下Ψ5P生产涉及的磷酸化与缩合反应的反应-时间曲线
4. 级联反应的合成灵活性与实际价值
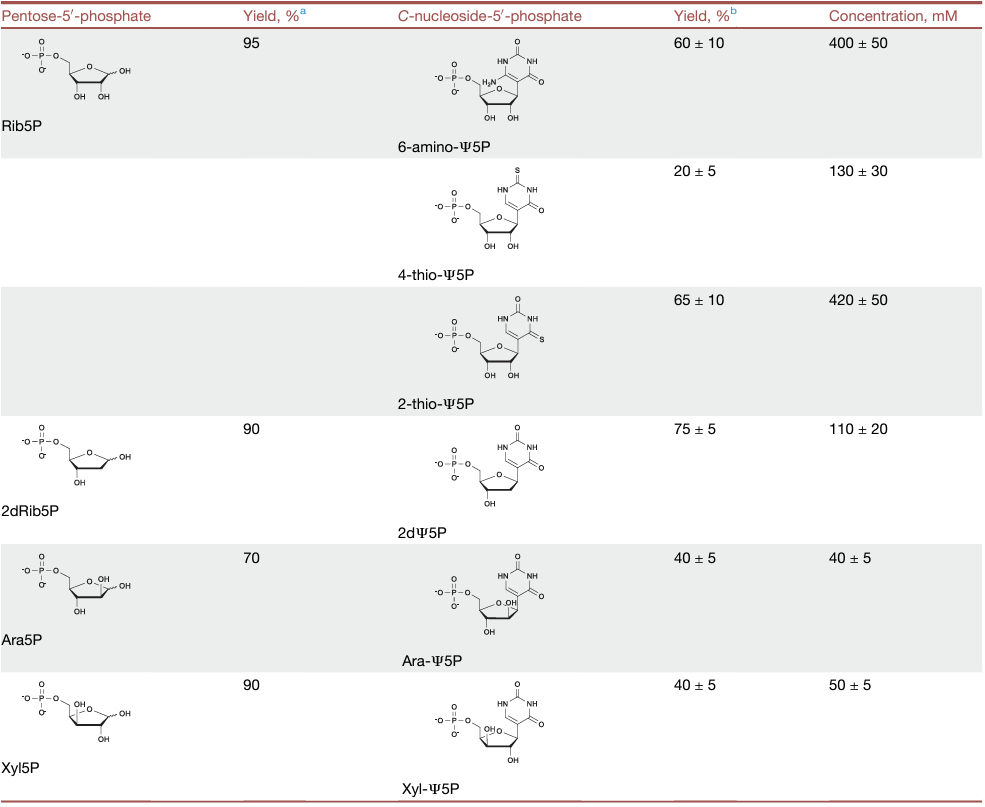
对于各类五碳糖,如D-阿拉伯糖(Ara)、2-脱氧-Rib(2dRib)和D-木糖(Xyl)等,以及尿嘧啶类似物(如6-氨基、2-硫、4-硫等)原料,作者通过优化条件展示了所开发的级联合成反应在通过五碳糖和Ura类似物为原料构筑核苷反应中的合成灵活性。值得注意的是,尽管YeiN酶对五碳糖的结构变化的敏感性较高,但仍然能够在合适的浓度条件下合成具有良好产率的C-核苷酸5'-磷酸类似物(表1)。
表1. 五碳糖磷酸化反应以及C-核苷酸5'-磷酸类似物合成反应性能总结
5. 生物催化级联反应的比较
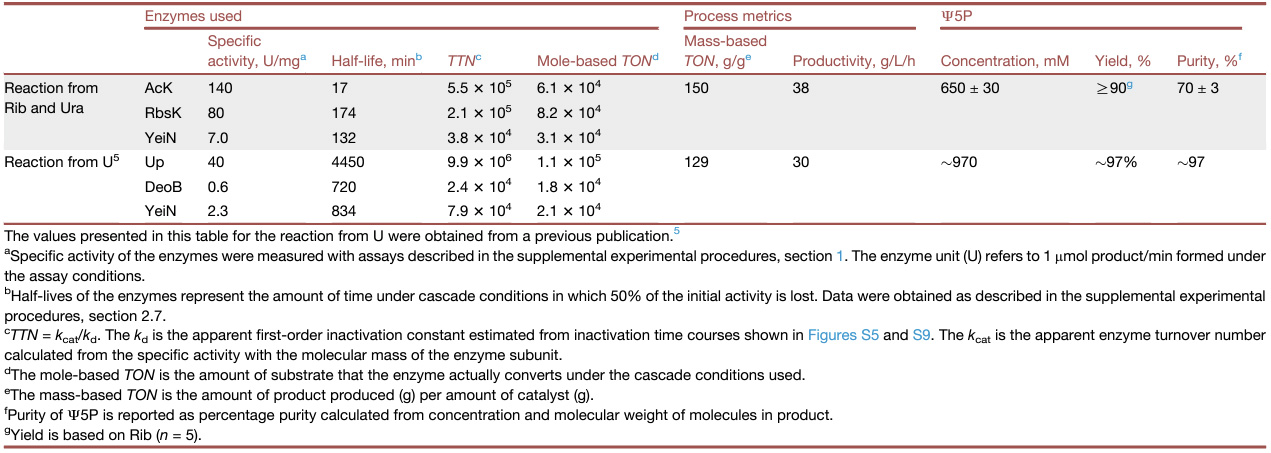
该论文研究的关键问题是此前报道的Ψ5P级联合成路径中使用的U原料是否能被更常见易得的原料(即Rib/Ura)所取代,同时保持合成路径的效率。而开发以Rib/Ura为原料的合成路径的主要挑战在于要高效地实现O5位选择性的Rib磷酸化反应。因此,作者比较了以Rib/Ura为原料和文献中报道的以U为原料合成Ψ5P的两种级联反应(表2),发现尽管两者的产率都很高,但从Rib/Ura原料级联反应中获得的Ψ5P产品浓度较低,这是由于AcP的可用浓度限制和pH控制引起的稀释所致。此外,两种路线的周转数相似。而就可比较的酶蛋白总用量而言,本工作报道的以Rib/Ura为反应原料的Ψ5P生产路径则具有更高的产量。同时,作者指出,将酶循环使用或提高其反应稳定性是提升总周转数的有效策略。例如,使用AcK的热稳定性变异体僵尸未来探究的选项之一。两种级联合成路径的产物纯度也有所区别。具体而言,Rib/Ura原料级联转化路径得到的Ψ5P产品浓度约为~ 70%,低于U原料路径所得的~ 97%浓度,醋酸盐是其主要的伴生产物,因而进一步纯化Ψ5P产品的工艺路线十分重要。反应所获得的Ψ5P可以直接磷酸化为ΨTP,也可以在反应混合物中直接脱磷酸化为Ψ,纯度超过97%。
表2. 两种级联反应过程合成Ψ5P的指标对比
鉴于激酶对底物磷酸化具有足够的位点和立体控制,反应设计和工程的挑战在于高效再生核苷5'-三磷酸(NTP)磷酸供体。此前已报道的激酶反应面临反应控制因素复杂、成本高、难以扩大化、产物选择性低分离困难等问题,因此使用利用AcP的AcK反应具有独特优势,对磷酸化反应具有优异的产率。AcP原料的合成需求、pH控制需求和对水解的敏感性是其主要缺点。对于Ψ5P合成,基于反应工程的节约性原则,更倾向于直接从AcP进行AcK反应。相关计算显示,当前研究中所展示的Rib磷酸化过程的产量(950 mmol/L/h)已经接近了物理OTR(氧气转移速率)的上限。总体来说,该研究通过优化Rib磷酸化过程实现了以AcP为磷酸供体的反应类型中创纪录的产物浓度和产量。性能结果表明,依赖于NTP的磷酸化反应能与工业生物催化的技术经济目标相匹配。
结论
本工作成功展示了一种用于合成C-核苷类似物的一锅法磷酸化-缩合级联反应策略,该策略具有高效性、灵活性等显著特征。在研究工作中,通过优化ATP的循环利用促进激酶催化的磷酸化反应,以及优化固体尿嘧啶底物的添加方式从而促进缩合反应,显著提高了磷酸化和缩合步骤的反应效率。总的来说,这种策略不仅为合成Ψ5P提供了一种有效的途径,而且因其具有合成C-核苷产品的能力而在生物学应用以及RNA结构与功能研究中存在潜在的应用价值。此外,本工作涉及到的生物催化与反应工程的结合与反应参数优化策略,有望在工业生物催化中发挥重要作用。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Phosphorylation-condensation cascade for biocatalytic synthesis of C-nucleosides
Andrej Ribar, Martin Pfeiffer, Bernd Nidetzky
Chem Catal., 2024, DOI: 10.1016/j.checat.2024.101127
(本稿件由Cell Press供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号