上海交大杨宇&同济朱小立Chem:基于滚环扩增技术的DNA-酶偶联物在生物医学领域展现广阔前景
近日,上海交通大学杨宇教授(点击查看介绍)团队联合同济大学附属第十人民医院朱小立教授(点击查看介绍)团队在Cell Press细胞出版社旗下Chem 期刊上发表了最新研究,为酶在生物医学领域的应用开辟了新方向。研究团队成功开发了一种基于滚环扩增(RCA)技术的长链多价DNA-酶偶联物,具有核壳型纳米结构(RCA-DEN),显著提升了酶的稳定性和功能性,并展示出在疾病诊断、治疗等生物医学应用中的巨大潜力。
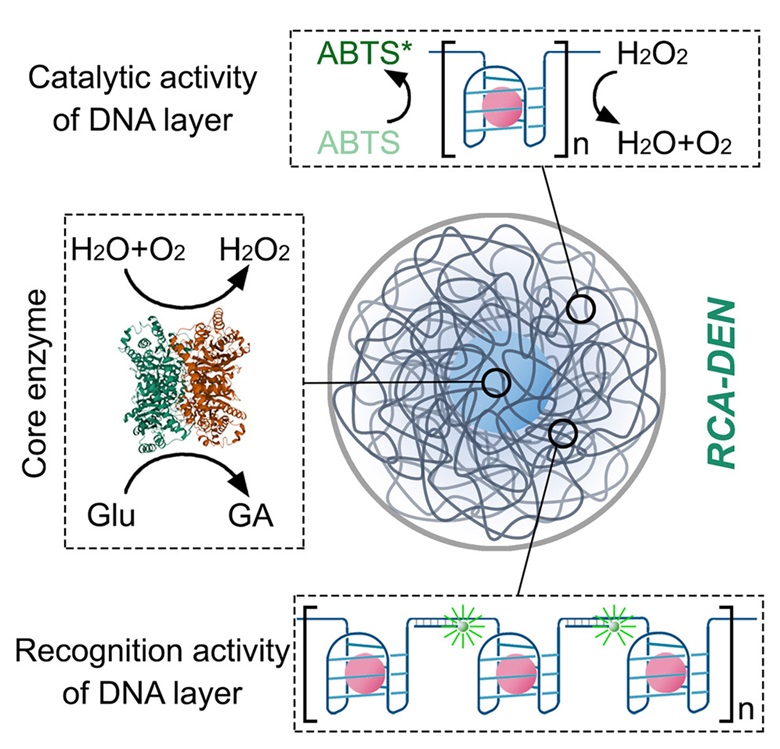
酶作为一类具有精妙结构和多样功能的生物大分子,在生物医学领域中扮演着重要角色。然而,酶在实际应用中常面临不稳定、靶向性差、递送复杂等挑战。针对这些问题,研究团队创新性地提出了基于RCA技术的DNA-酶偶联纳米结构解决方案。通过RCA技术高效引入高密度功能DNA,在酶表面形成核壳结构的DNA-酶偶联物(RCA-DEN),这种设计不仅显著增强了酶和DNA的稳定性,还保留了酶的催化活性,成功应对了酶在实际应用中的技术难题。
研究团队通过一系列严格实验验证了RCA-DEN的优异性能。结果显示,RCA-DEN在制备过程中能够有效保留酶和DNA的活性,并在储存、抗核酸酶降解、抗蛋白酶降解及极端环境下表现出卓越的稳定性,为其在复杂生物环境中的应用奠定了坚实基础。
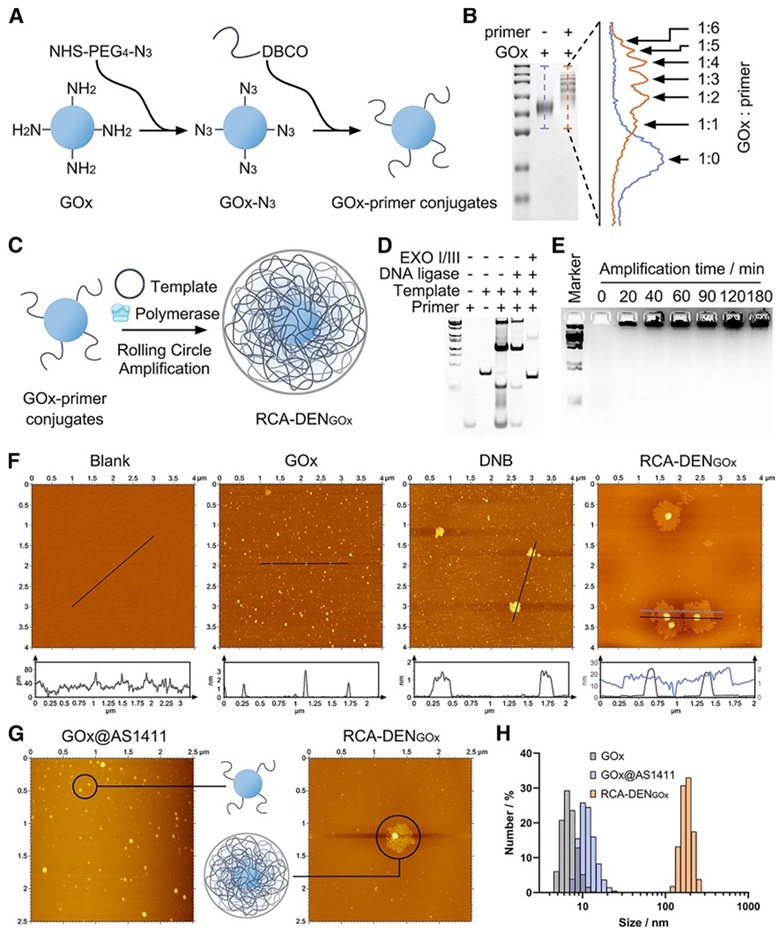
图1. RCA-DEN的制备和表征
在功能验证方面,RCA-DEN展现了出色的选择性催化和级联催化能力。尤其是在多巴胺检测中,RCA-DEN HRP通过多巴胺适配体实现了多巴胺的高效选择性富集与催化,为生物传感与生物分析提供了全新思路。此外,RCA-DEN GOx实现了从葡萄糖到过氧化氢,再到显色底物的高效级联催化,为葡萄糖检测提供了一种准确而高效的方法。
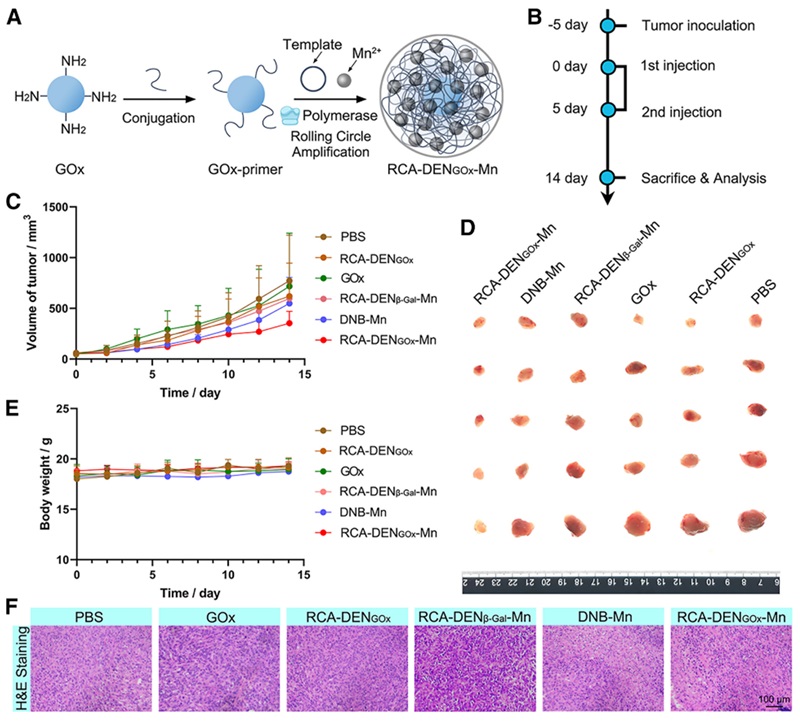
图2. RCA-DEN介导的饥饿与化学动力学协同疗法
更令人振奋的是,RCA-DEN在肿瘤治疗中展现了广阔前景。研究团队通过掺杂锰离子(Mn²⁺),制备出Mn掺杂的RCA-DEN GOx(RCA-DEN GOx-Mn),展现出卓越的抗肿瘤效果。实验表明,RCA-DEN GOx-Mn能在肿瘤部位消耗葡萄糖并产生过氧化氢,进一步通过Mn²⁺催化生成羟基自由基,成功实现饥饿疗法与化学动力学疗法的协同抗肿瘤效果。体内实验进一步验证了其显著的抑瘤作用,且无明显副作用。
此外,RCA-DEN具有模块化设计与可编程性,适用于多种酶的固定化,并可通过调整模板序列实现功能的定制化设计,这一特性为其在生物医学领域的广泛应用提供了无限可能。
这项研究不仅为酶在生物医学领域的应用提供了新思路与新方法,也为未来疾病诊断、治疗等生物医学技术的革新奠定了坚实基础。研究团队表示,他们将继续深入探索RCA-DEN的潜力,推动其在更多领域的应用,为人类健康事业作出更大贡献。
该工作得到谭蔚泓院士的大力指导,并获得国家自然科学基金、科技部重点研发计划等多个项目支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Rolling circle amplification-based DNA-enzyme nanostructure for immobilization and functionalization of enzymes
Dongsheng Mao, Wenxing Li, Xueliang Liu, Jingqi Chen, Dali Wei, Lei Luo, Qianqin Yuan, Yu Yang, Xiaoli Zhu*, Weihong Tan
Chem, 2024, DOI: 10.1016/j.chempr.2024.10.002
导师介绍
杨宇
https://www.x-mol.com/university/faculty/376831
朱小立
https://www.x-mol.com/university/faculty/381390
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号