Nature:不寻常的镍配合物,不寻常的XEC反应
在包括新药研发的许多领域,筛选化合物库以找到合适分子——这种类似“沙中淘金”的策略已成为主流。自然而然地,开发能够快速合成多种化合物的通用方法至关重要。交叉偶联是拓展化合物库的一种常用方法,尤其是通过还原偶联反应直接由大量碳亲电试剂构建C-C键——此类反应也称为亲电交叉偶联(XEC)——为快速实现分子的多样化提供了一种极具吸引力的方法。在芳基/乙烯基和烷基亲电试剂的交叉偶联反应中,Csp2-Csp3交叉产物的选择性主要源于金属催化剂与芳基或烷基亲电试剂的不同反应机制和速率。相比之下,相似的亲电试剂(如两个烷基亲电试剂)通过XEC反应选择性形成交叉偶联产物却并非易事,这是因为催化剂通常无法区分两个亲电试剂,进而难以构建Csp3-Csp3键(图1a)。与氧化还原中性反应不同,两个亲电试剂的还原偶联通常会导致难以预测的交叉偶联和均偶联混合物,因此往往需要使用过量的亲电试剂来保证交叉偶联产物的选择性。近年来,化学家致力于开发烷基-烷基XEC反应,特别是通过大小区分烷基片段已成为烷基底物进行XEC反应的最成功方法之一,例如:1)MacMillan等人利用自由基分选策略实现了3°烷基氧化还原活性酯(RAE)和1°烷基溴化物的选择性Csp3-Csp3键偶联;2)Kawamata、Baran和Shenvi等人利用类似的分选策略实现了3°和1°烷基RAEs之间的还原偶联反应;3)See和Lin展示了一种依赖于空间控制的闭壳体、2e-类似物,即通过对活化3°烷基溴化物的受控电还原产生稳定的3°碳负离子,并通过SN2反应优先与1°烷基卤化物进行偶联而非3°烷基卤化物。尽管如此,但要想选择性地实现具有相似空间特性的烷基亲电体的XEC反应仍充满挑战。近日,美国俄亥俄州立大学Christo S. Sevovi、美国默克公司(Merck & Co. Inc.)Dipannita Kalyani等研究者利用一种廉价的有机金属催化平台,成功地实现了烷基亲电试剂的还原交叉偶联反应(图1b),即在还原条件下通过烷基卤化物、氧化还原活性酯或吡啶鎓盐的氧化加成直接形成稳定且可分离的NiII(alkyl)配合物,该配合物与另一分子烷基亲电试剂发生交叉偶联便可构建Csp3-Csp3键。此外,通过脱卤、脱羧或脱氨基偶联的各种组合,该方法能够快速多样化地合成氨基酸、天然产物、药物分子和类药物构建砌块,进一步展现出其实用性。相关成果发表在Nature 上。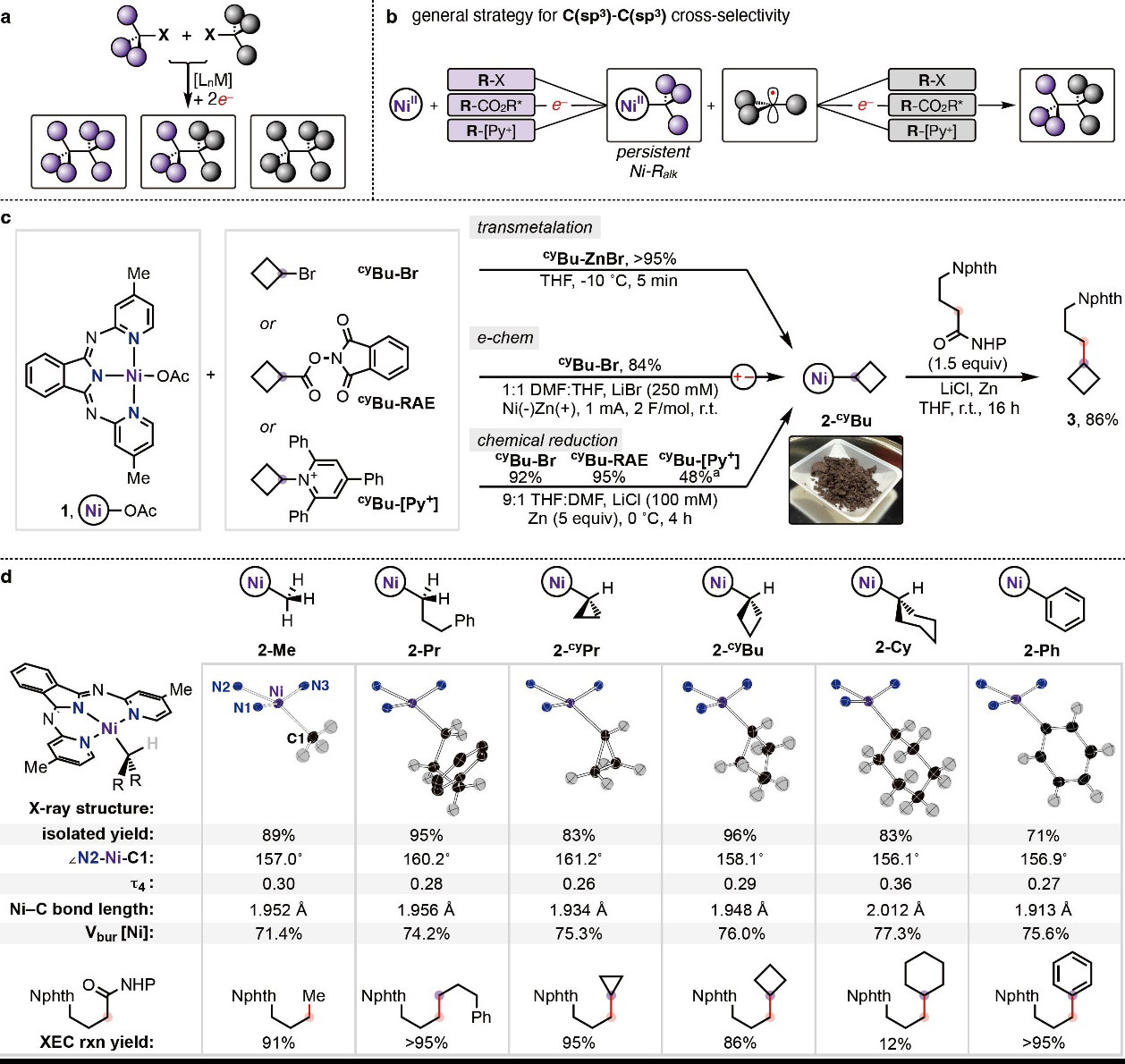
图1. 镍-烷基配合物的合成方法、合成应用及性能研究。图片来源:Nature
首先,作者对稳定Ni(alkyl)配合物的形成及其稳定性进行了研究(图1c)。鉴于环丁基有机锌试剂与(MeBPI)NiII(OAc)配合物1之间的转金属化可简洁高效地获得Ni(alkyl)配合物,因此作者在-10℃下向1的THF溶液中加入烷基锌试剂,发现黄色的悬浊液迅速变成均相的紫色溶液,接着在手套箱中用碱性氧化铝过滤并蒸发溶剂后便可获得深紫色固体,1H NMR分析显示其具有与烷基配合物 2-cyBu一致的抗磁共振信号。值得一提的是,仲烷基配合物可在溶液和固态下稳定存在数周,并且2-cyBu与烷基RAE在还原条件下发生Csp3-Csp3偶联反应,从而以86%的产率获得交叉偶联产物3。其次,作者尝试通过电化学(e-chem)方式制备2-cyBu,具体而言:在合成芳基配合物的条件下对1和环丁基溴化物进行电解后形成棕色溶液,1H NMR分析表明其具有等摩尔量的黄色起始原料1和紫色产物2-cyBu。尽管Ni(alkyl)配合物的形成不完全,但烷基溴被完全消耗,作者推测这可能是由于电化学驱动芳基卤化物与烷基卤化物的OA机制不同所致,其中芳基溴化物的OA是协同过程,而烷基卤化物是逐步自由基途径,1和芳基卤化物的CVs证明了OA机制的差异。进一步研究发现在低电流密度和过量烷基溴(2 equiv)的条件下可限制Ni(II)的过渡还原,以84%的产率合成2-cyBu并且反应对底物高度依赖。随后,作者使用具有高表面积的金属粉末作为弱还原剂(相对于1),在THF:DMF(9:1)为混合溶剂、LiCl为添加剂的条件下,Zn粉可促进cyBuBr与1的OA反应,4 h后能以接近定量产率获得2-cyBu。此外,该条件可拓展到Katritzky吡啶盐和烷基RAEs的OA反应,分别以48%和95%的产率生成相应的配合物。如图1d所示,作者还合成并表征了2-Me、2-Pr、2-cyPr、2-Cy和2-Ph取代的镍配合物,同时在未优化条件下使用烷基RAE对六种有机镍配合物进行还原偶联反应。另外,晶体学分析表明这些有机镍配合物采用扭曲的平面正方形几何结构,而且从平面正方形到四面体几何结构的畸变是导致C(sp2)-C(sp3) XEC反应产率较低的原因之一,其可以通过τ4参数来量化。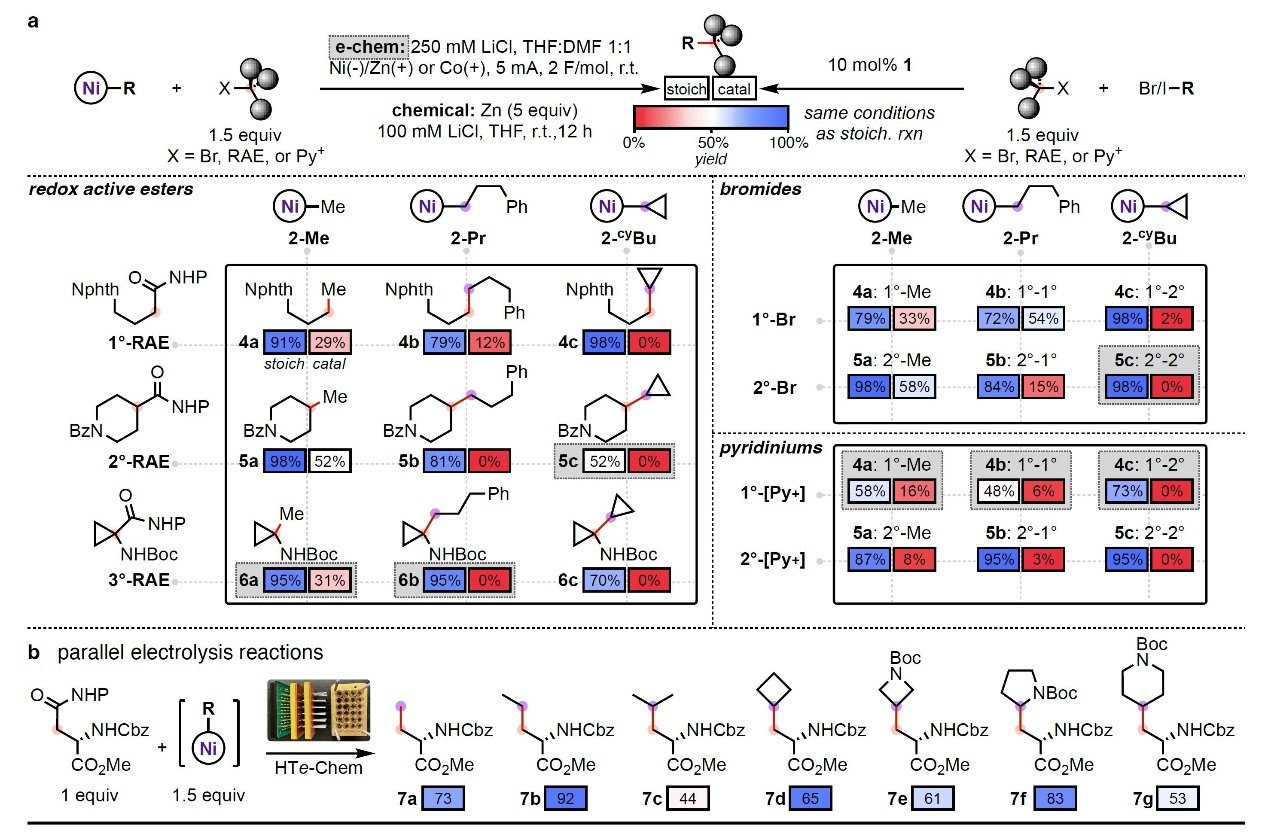
图2. 有机镍配合物的合成及其反应性研究。图片来源:Nature随后,作者在电化学或化学还原条件下对未取代(2-Me)、一级(2-Pr)和二级(2-cyPr)烷基Ni配合物与1°、2°和3°烷基亲电试剂(卤化物、RAEs和吡啶盐)的反应活性进行了研究(图2a),结果显示未受阻的烷基亲电试剂(如:1°或2°烷基卤化物和RAEs)与2-Me/2-Pr烷基镍配合物进行反应时产率较高(4a-b和5a-b),而用锌粉进行反应时大位阻烷基试剂之间形成偶联产物(5c、6a-b)的产率通常较低(<20%)。鉴于化学还原未能促进1°烷基吡啶盐的偶联反应,因此作者在THF/DMA中以NaI作为电解质通过恒定电流进行电化学反应,其可以显著提高烷基吡啶鎓盐(4a-c)或受阻烷基亲电试剂(5c、6a-b)的电化学反应产率(<20%→>90%)。与3°烷基RAEs的反应相反,3°烷基溴化物进行反应时通过烷基中间体的异构化作用会生成结构异构体的混合物,而1°或2°烷基溴化物进行Csp3-Csp3键偶联(4和5)而非异构化。如图2b所示,作者还开发了一系列Ni(alkyl)配合物与一种亲电试剂(如:天冬氨酸衍生的烷基RAE)之间的平行电解反应,具体而言:将偶联反应从3 mL缩小到0.35 mL并在HTe-Chem反应器中进行电解后,这些反应都能以良好的产率生成产物(7a-7g),可用于快速构建非天然氨基酸化合物库。另外,耐受性研究表明反应无需严格的干燥条件,此类反应的产率(7d,产率:66%)仅略低于在手套箱中严格惰性和干燥条件下进行的反应(产率:83%)。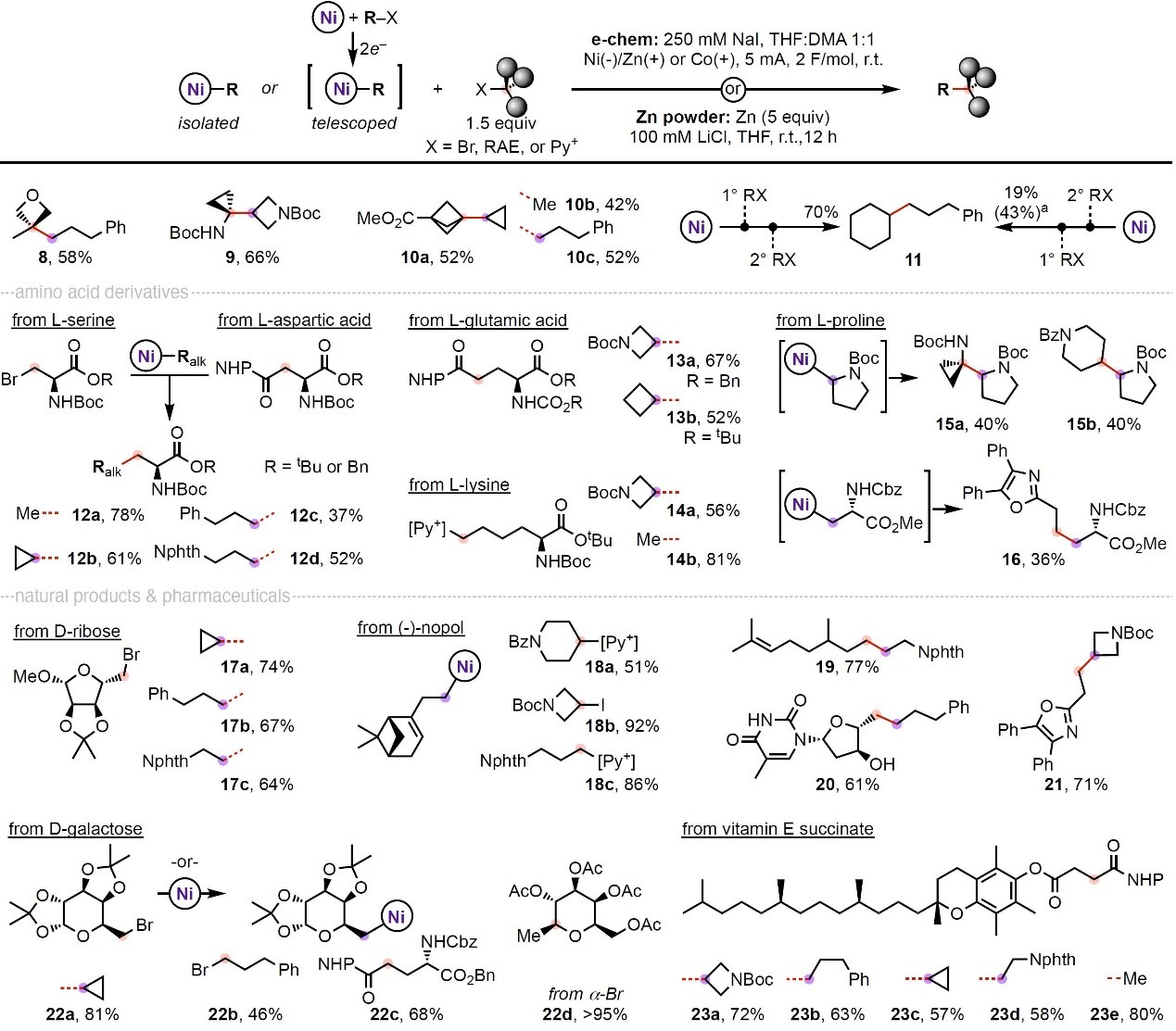
接下来,作者将开发的条件应用于其它底物的化学计量反应(图3),发现3°烷基RAEs与1°(8)和2°(9、10)烷基亲电试剂能够有效进行反应并获得相应的季碳产物。需要指出的是,大位阻底物参与的反应表明先活化取代度较低的底物,再引入取代度较高的底物作为第二个亲电试剂参与反应时,Csp3-Csp3键偶联最可靠(11,产率:70%),若颠倒此顺序会导致产率较低(19%)。另一方面,作者以AA片段作为第二个亲电试剂并与预先形成的有机镍络合物相结合,成功地实现了氨基酸脱氨基(赖氨酸,14a-b)、脱羧(天冬氨酸(12a-d)和谷氨酸(13a-b)、脯氨酸)和脱卤(丝氨酸,12a-d)交叉偶联反应,从而以中等至良好的产率生成了一系列衍生氨基酸。值得一提的是,该反应也可以按照相反的顺序进行,即脯氨酸和天冬氨酸片段先通过OA生成相应的Ni配合物,然后与烷基亲电试剂进行偶联便可形成相应的产物(15a-b和16)。此外,药物分子和天然产物衍生的烷基亲电试剂同样能兼容该反应,例如:1)溴化半乳糖和核糖与Ni(alkyl)配合物进行反应并成功安装1°(17b-c)和2°(17a、22a)烷基片段,而且α-Br-半乳糖底物与Ni(Me)配合物反应时以优异的产率形成单一的立体异构体——甲基化半乳糖22d;2)半乳糖的有机镍配合物可与多种烷基溴化物(22c-b)进行反应;3)烷基吡啶(18a、18c)和卤化物(18b)能与卤化诺普醇衍生的OA配合物顺利进行偶联;4)胸苷衍生物(20)可以在游离醇或酸性胺的存在下制备,并且药用相关的氮杂环丁烷片段可以很容易地安装到奥沙普秦衍生物(21)的骨架上;5)相应有机镍中间体的偶联可轻松获得多种香茅醇(19)或维生素E(23a-e)的衍生物。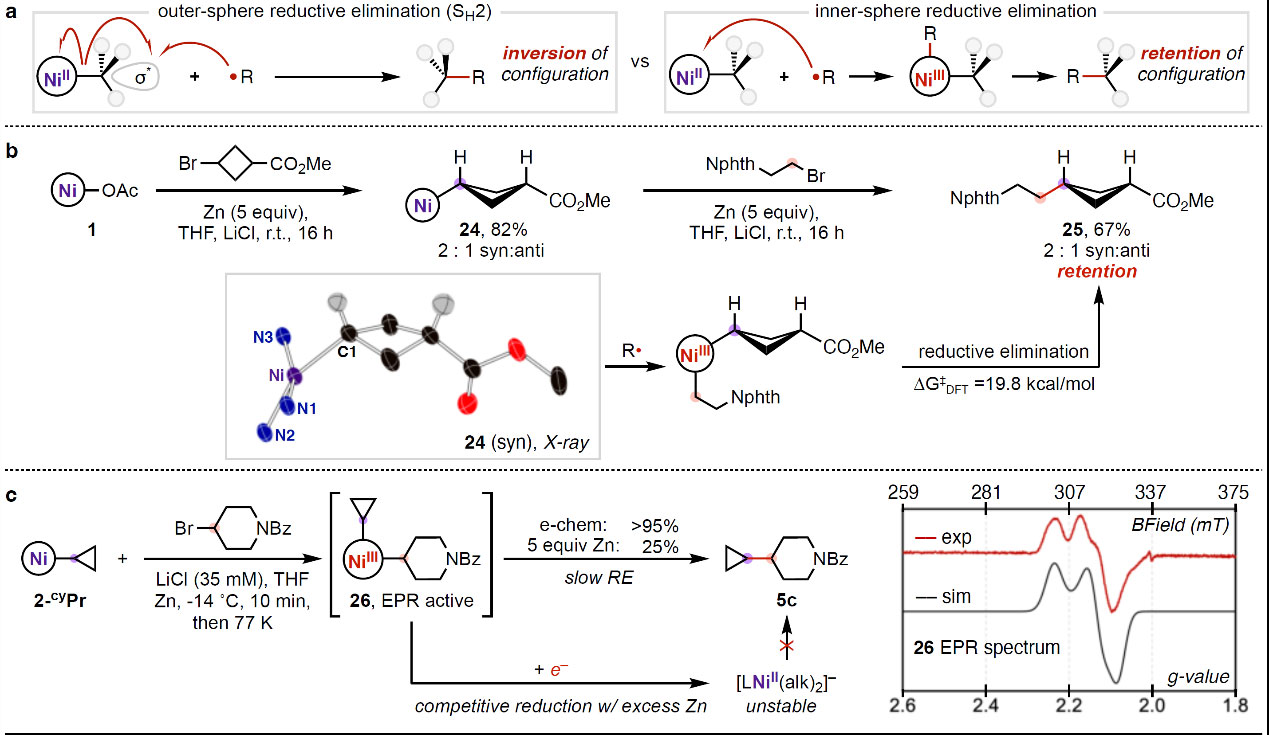
如图4a所示,通过Ni(alkyl)配合物形成C-C键有两种途径:1)瞬态烷基自由基与Ni烷基配合物进行双分子均裂取代(SH2),该过程会翻转碳原子上的立体化学;2)NiII(alkyl)配合物捕获烷基自由基并生成NiIII(dialkyl)配合物,发生还原消除(RE)以获得Csp3-Csp3偶联产物,该过程会保留碳原子上的立体化学并将起始原料的非对映体比率(d.r.)转移到产物上。基于此,作者进行了一系列实验来探究反应机理,具体而言:1)烷基溴通过OA形成Ni(alkyl)配合物24的混合物(syn:anti=2:1),在与烷基溴进行反应时以67%的产率和syn:anti=2:1获得交叉偶联产物25(图4b),进而支持了内球反应机制;2)24在溶液中可稳定存在并且其d.r.值不会随时间而变化,同时2-己-1-烯配合物的偶联反应在Ni-烷基键均裂后会进行快速1,5-环化且仅形成线性产物,未检测到基于自由基的环化产物,进而证实了Ni-烷基键在溶液中不会可逆地均裂并验证了立体化学探针的设计;3)密度泛函理论(DFT)计算显示NiIII(dialkyl)配合物26进行RE的自由能垒为19.8 kcal/mol,而2-Ph进行类似反应的能垒是16.3 kcal/mol。另外,Csp3-Csp3键偶联的计算能垒与在0°C进行偶联时Ni(alkyl)紫色溶液在数小时内缓慢转化的观察结果相一致(0°C时∆G‡=19.8 kcal/mol、t1/2≈20 min),这些结果表明NiIII(dialkyl)中间体在室温下可持续存在数分钟且可在低温下被检测到;4)在低温下进行两个仲烷基片段的偶联反应并对反应液进行电子顺磁共振(EPR)光谱分析后检测到NiIII(dialkyl)物种26。基于图2a的研究,EPR检测到的假定NiIII(dialkyl)物种具有合成相关性,相同的烷基片段能以接近定量的产率形成 5c,但是只有在电化学偶联时才能获得高产率,以Zn作为还原剂促进的偶联反应仅以18%的产率生成5c,这是由于缓慢进行C(sp3)-C(sp3) RE的NiIII(dialkyl)中间体可能会被高表面积Zn粉竞争性还原,而电还原仅在电极上以受限电流发生。本文在还原条件下通过烷基卤化物、氧化还原活性酯或吡啶鎓盐的氧化加成直接形成稳定且可分离的NiII(alkyl)配合物,该配合物与另一分子烷基亲电试剂发生交叉偶联便可构建Csp3-Csp3键。此外,通过脱卤、脱羧或脱氨基偶联的各种组合,该方法能够快速多样化地合成氨基酸、天然产物、药物分子和类药物构建砌块,进一步展现出其实用性。原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):
Reductive alkyl-alkyl coupling from isolable nickel-alkyl complexes
Samir Al Zubaydi, Shivam Waske, Volkan Akyildiz, Hunter F. Starbuck, Mayukh Majumder, Curtis E. Moore, Dipannita Kalyani, Christo S. SevovNature, 2024, 634, 585-591. DOI: 10.1038/s41586-024-07987-9











