中国科学技术大学黄汉民团队Chem Catal.:金属电子梭催化炔烃的高选择性反式双烷基化反应
近日,中国科学技术大学黄汉民教授(点击查看介绍)在Cell Press细胞出版社期刊Chem Catalysis 上在线发表了一篇题为“Electron-Shuttle Catalysis Enables Regioselective and Stereospecific Dialkylation of Alkynes”的成果。黄汉民教授长期致力于发展新型催化策略,建立了金属电子梭催化新范式,并在此前的研究中利用镍催化剂作为金属电子梭,开辟了烯烃双sp3碳官能团化的新路径(Nat. Catal. 2023, 6, 847-857)。在这项研究中,作者继续沿用这一新的催化范式,开发了具有高区域选择性和立体特异性的炔烃反式双烷基化反应。该反应可以从多个简单组分出发一步构建多取代烯烃,从而高效地合成一系列含氟烯丙胺类化合物。此外,在合成氟代产物的基础上,作者还进一步开发了氢化锂铝高效脱氟氢化反应,形式上实现了炔烃的双伯烷基化反应。
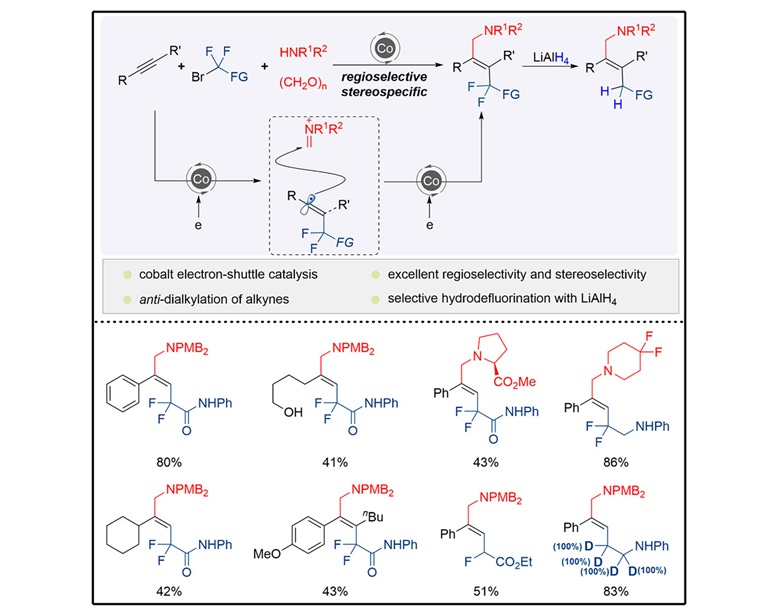
过渡金属催化的炔烃双碳官能化反应是合成多取代烯烃最直接且最有效的方法之一。在此前的报道中,这类反应通常通过经典的过渡金属催化循环实现,机理上历经碳金属中间体(图1,左侧)。然而,这些报道中反应底物往往只限于端炔,且其它偶联试剂中必须包含卤代芳烃或一级烷基卤代烃。此外,此前研究通过使用含不饱和键(如C=C、C=O和C=N)的化合物作为偶联试剂,还建立了基于氧化环化策略的炔烃双官能化方法(图1,右侧)。但氧化环金属化的机理历程决定了该类反应只能生成顺式选择性的产物,限制了这种方法在合成反式选择性产物中的应用。
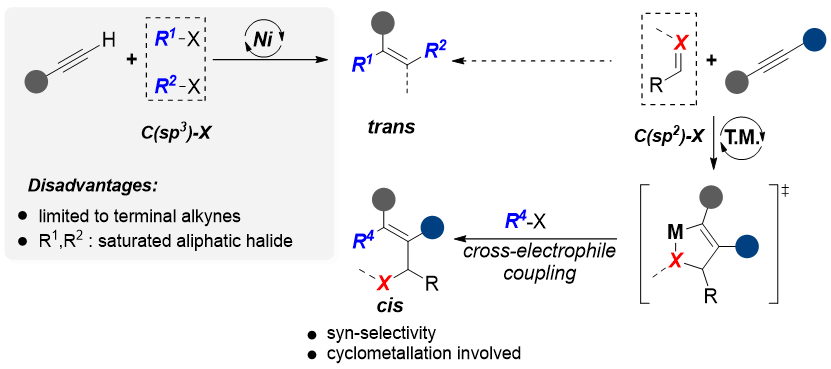
图1. 过渡金属催化炔烃的双官能团化反应策略
黄汉民教授长期致力于发展新型催化策略,建立了金属电子梭催化新范式,并在此前的研究中利用镍催化剂作为金属电子梭,开辟了烯烃双sp3碳官能团化的新路径。进一步地,作者希望能够在炔烃双官能化反应中沿用并拓展金属电子梭催化策略,从机理上突破氧化环金属化过程的限制,有效提高炔烃和烷基化试剂底物的适用范围,并逆转反应的E/Z选择性。本文中,作者使用钴催化剂作为金属电子梭催化多组分反应,通过连续的自由基过程完成自由基的产生和淬灭,进而实现对端炔和内炔的反式双烷基化反应,为高效、立体特异性地合成多取代烯烃提供了一种简单方法(图2)。反应过程中,还原态的金属电子梭首先诱导烷基自由基的生成,随后该自由基对炔烃进行自由基加成,生成线性的烯基自由基中间体II。由于位阻效应,烯基自由基II将会在位阻较小的一侧对亚胺正离子III进行自由基加成,形成氮正离子自由基中间体IV,最后被还原为立体专一性的目标产物。溴代氟烷烃的引入对此反应的立体选择性起到重要作用,同时产物中的烯丙位氟原子可以通过新开发的脱氟氢化反应简便脱除,从而得到形式上双伯烷基取代的烯烃。因此,该方法可被视为是氧化环化策略在炔烃双烷基化反应中的重要补充。
值得注意的是,该反应的成功实现需克服以下三种潜在的竞争反应:1)反应体系中的炔基金属物种可以与多聚甲醛或者亚胺正离子发生亲核加成反应;2)炔烃也可以与多聚甲醛或原位生成的亚胺正离子,在钴催化剂的作用下经历氧化环金属化生成相应的副产物;3)此外,还可能会形成烯基金属物种,导致单烷基化副产物的产生。
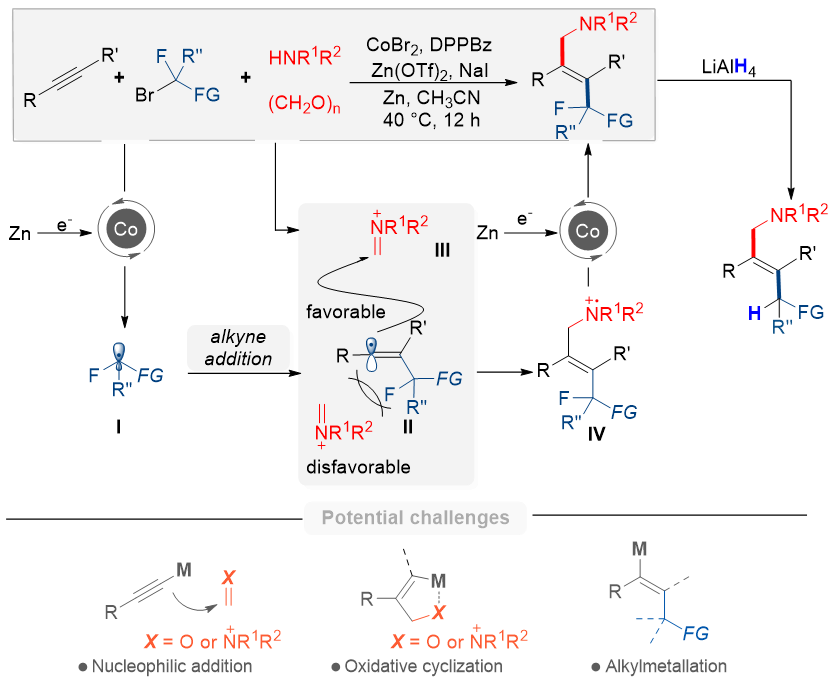
图2. 金属电子梭催化策略实现炔烃的双官能团化反应
通过对电子梭催化体系进行一系列优化,作者成功克服了上述提到的诸多挑战,实现了以炔烃、溴代氟烷烃、仲胺以及多聚甲醛为底物的四组分反应。反应以10 mol%的CoBr2作为催化剂前体,12 mol%的DPPBz为配体,50 mol%的Zn(OTf)2为Lewis酸活化试剂,40 mol%的NaI为添加剂,Zn为还原剂,在乙腈溶剂中,40 ℃反应12小时,能以80%的收率得到高区域选择性和高立体选择性的炔烃氟烷基化胺甲基化产物1。
对炔烃的底物考察结果表明(图3),反应对含各种官能团的芳基端炔和烷基端炔都能很好地兼容,并能以高区域选择性和立体选择性得到E式的三取代烯烃。值得注意的是,对于位阻较大的内炔,该反应体系也同样适用,得到反式加成的产物。此外,作者也对一些小分子化合物进行了后过渡修饰,成功获得了相应的目标产物。
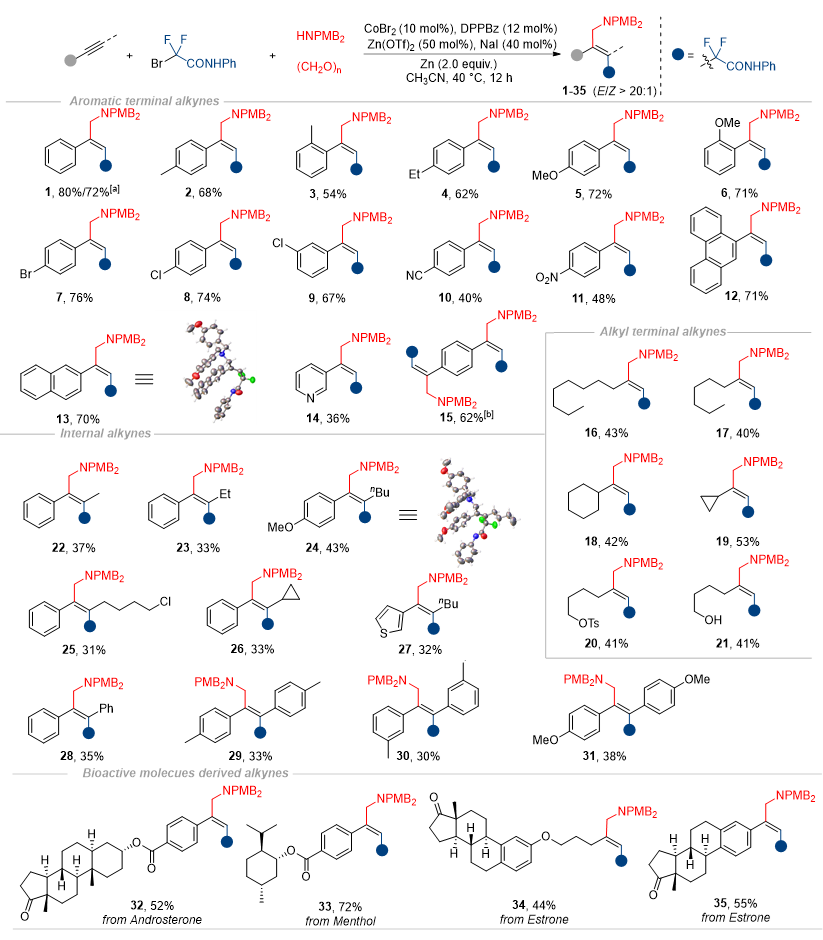
图3. 炔烃的底物拓展
除此之外,作者继续考察了对二级胺以及溴代氟烷烃的底物适用范围(图4)。如图所示,链状的二级胺或环状的含氮杂环化合物在此反应体系中都可以很好地兼容。通过对溴代烷烃的底物拓展可以观察到,不论是取代的二氟酰胺类溴代烷烃,还是含氟酯类的溴代烷烃都可以得到相应的炔烃反式加成产物。
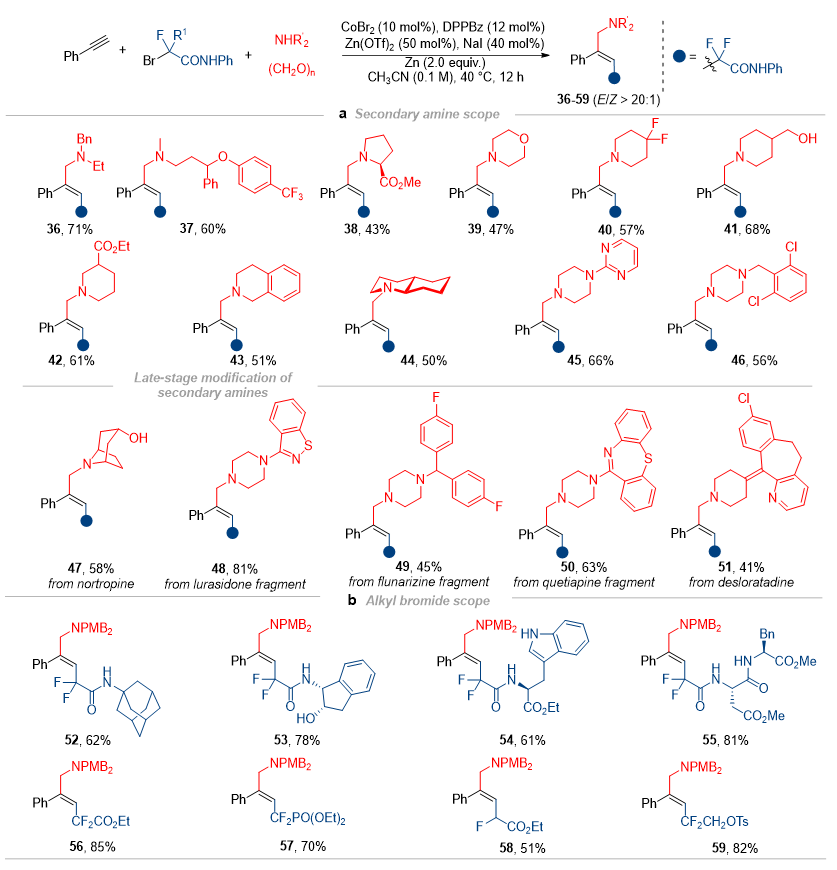
图4. 二级胺与溴代烷烃的底物拓展
在完成上述工作之后,作者进一步尝试对反应产物进行转化应用(图5)。首先可以通过NaBH4和LiOAc的共同作用实现酰胺的还原,以88%的分离收率得到一级醇化合物60。此外,可以通过硝酸铈胺氧化作用实现底物1的脱苄过程,以93%的分离收率得到61(图5A)。还可以通过分子内的反应得到吡咯烷酮62(图5B)。值得一提的是,作者开发了LiAlH4还原体系,实现了产物脱氟氢化的过程。可以选择性地实现对烯丙位氟的脱氟氢化,而不影响其它位点的氟原子。通过氘代实验,作者初步探究了此脱氟氢化过程的机理,可以发现当使用LiAlD4作还原剂时,根据底物中烯丙位含氟个数不同,分别以83%的收率得到含四个氘的产物,和以68%的收率得到含三个氘的产物(图5C)。
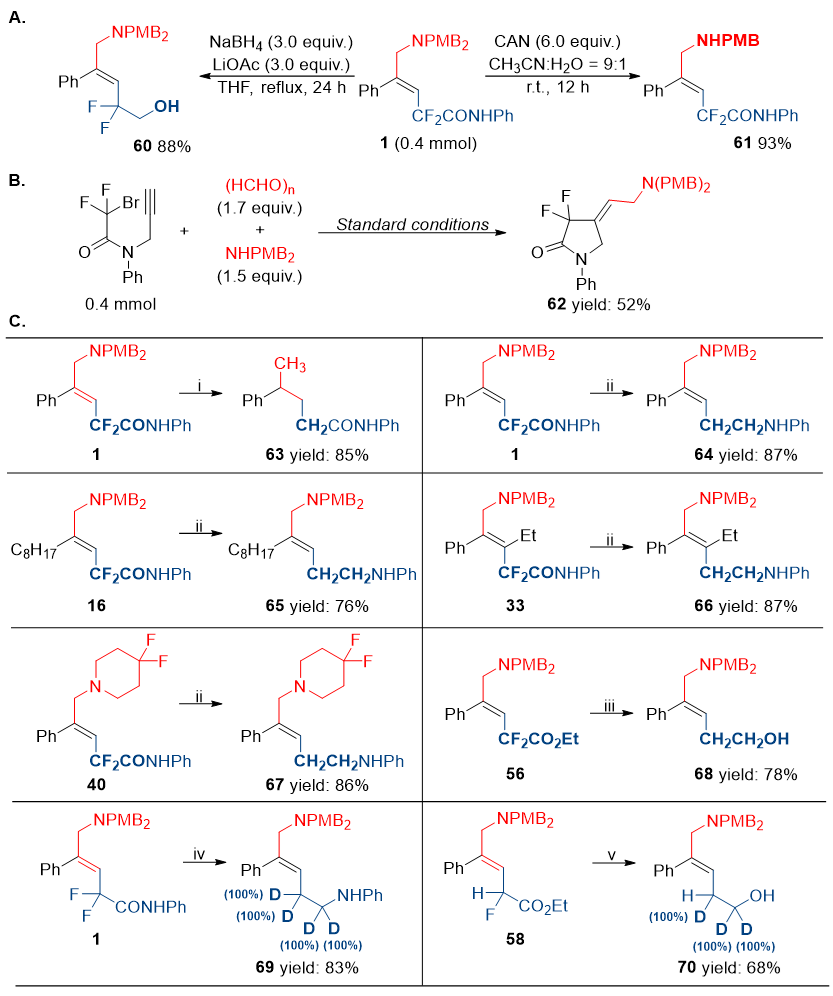
图5. 合成应用
为了进一步理解反应机理,作者进行了自由基捕获实验、对照实验以及自由基钟实验(图6)。实验结果表明,该多组分反应经历了连续的自由基过程,该反应由溴代氟烷烃启动,金属钴不参与成键,仅起到电子的传递作用。综上所述,机理与作者预先提出的策略完全吻合。
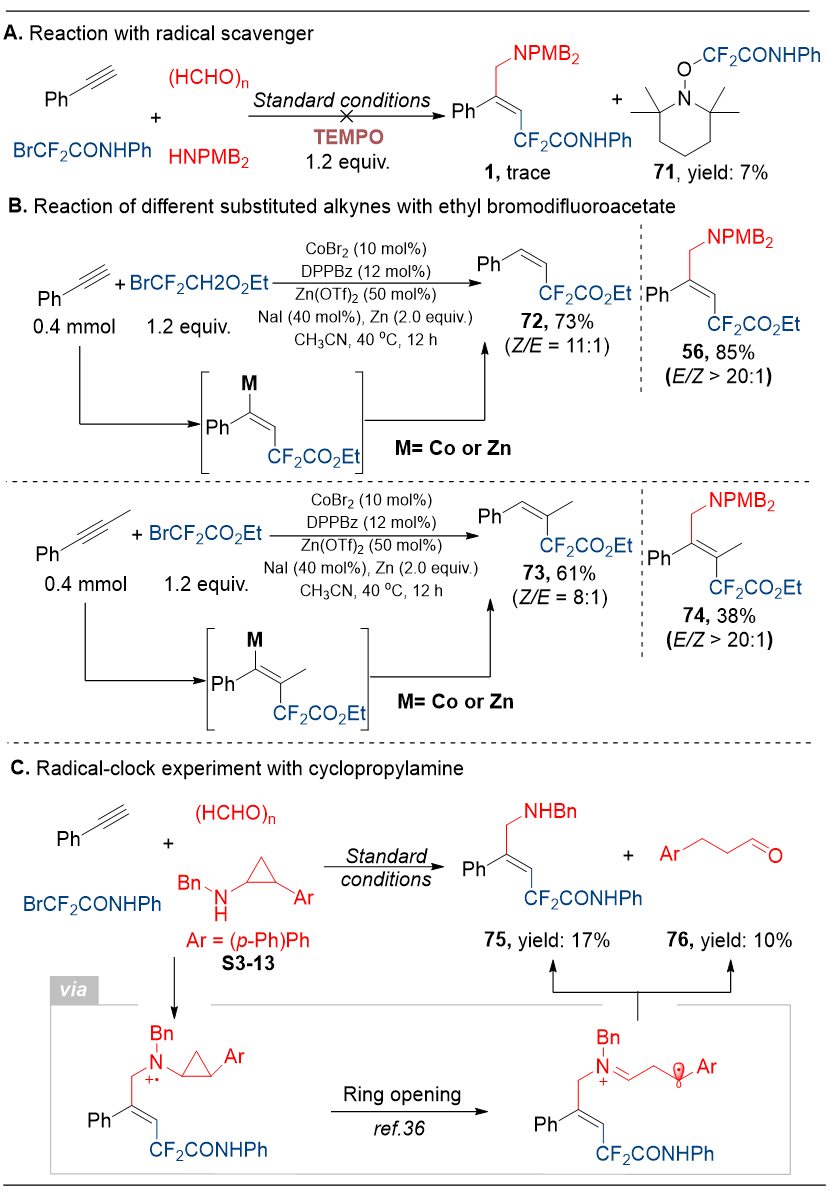
图6. 机理实验
综上,黄汉民教授通过将该课题组发展的金属电子梭催化新范式与课题组前期对胺甲基化反应的长期研究相结合,开发了一种新颖的四组分炔烃的双烷基化反应。该反应使用金属钴催化剂作为电子梭,催化溴代氟烷烃和原位得到的亚胺正离子与炔烃发生串联自由基加成反应,成功获得了一系列多取代烯烃,反应具有很好的区域和立体选择性。此外,使用简单的LiAlH4作为还原剂,可以顺利实现烯丙基氟化物的脱氟氢化反应,从而形式上实现反式的炔烃双伯烷基加成反应。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Electron-shuttle catalysis enables regioselective and stereospecific dialkylation of alkynes
Zhiting Wang, Changqing Rao, Hanmin Huang*
Chem Catal., 2024, DOI: 10.1016/j.checat.2024.101129
导师介绍
黄汉民
https://www.x-mol.com/university/faculty/74099
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号