通过不对称衍生化和离子淌度-质谱法同时测定脂质C=C键的位置和顺反构型
近日,吉林大学化学学院国新华教授课题组发表研究论文,该研究中他们将C=C双键不对称衍生化与离子淌度-质谱结合,对脂质中双键的位置和顺反构型进行了全面解析,为离子淌度-质谱技术在分子结构分析中的应用提供了新的见解。不饱和脂类中C=C键的位置和顺反异构体对其生物活性有显著影响。同时识别不饱和脂类中C=C键的位置和顺反异构体非常重要,然而仍然是一个具有挑战性的任务。
烯烃环化反应不仅在有机合成领域占据重要地位,并且在生信分析方面应用颇多。其中的三元环化和三元环本身的平面结构引起了作者的注意。当1,2-二取代双键形成三元环时,顺式构型两取代基位于三元环同侧,而反式构型取代基位于三元环平面异侧。当二取代烯烃两取代基不同,且第三个原子存在差异较大两基团时,烯烃三元环化会形成一对非对映异构体。由于空间位阻的影响,顺式双键倾向于形成一种异构体,而反式双键会形成比例相近的一对异构体。基于离子淌度对非对映异构体的分离作用,衍生后,顺式双键在淌度中表现出单峰,而反式双键为双峰,进而对双键立体构型进行判断。
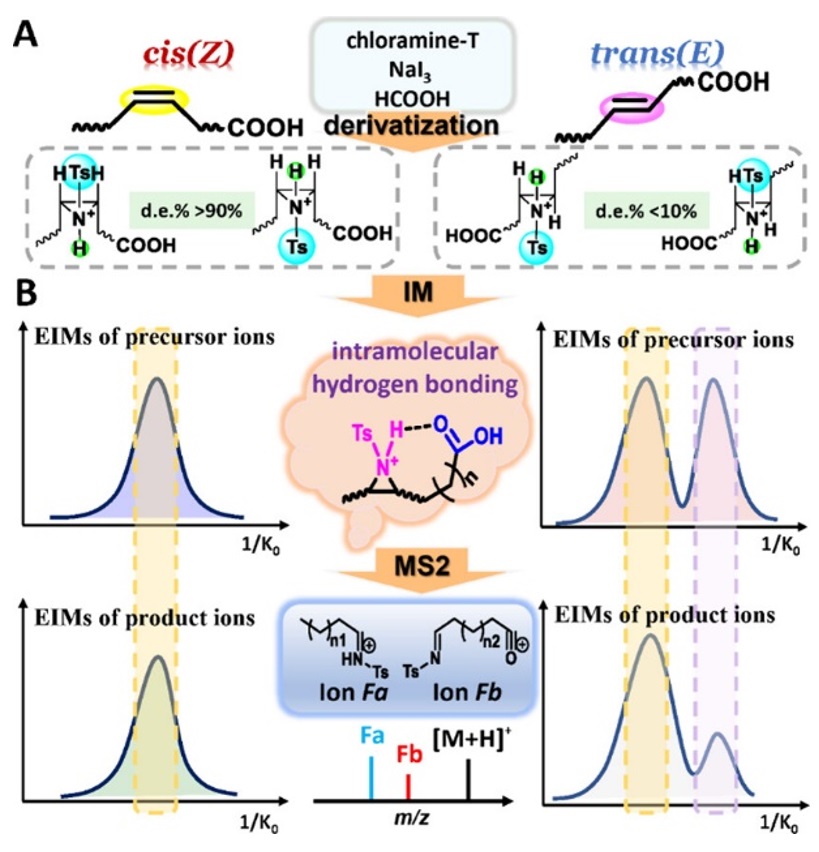
图1. 通过不对称衍生化和离子淌度-质谱法同时测定脂质 C=C 键的位置和顺反构型原理演示。(A)由于空间位阻的影响,顺式或反式双键衍生化后异构体的相对比例不同。(B) 利用离子淌度谱和MS/MS谱分析了脂质中双键的位置和顺反式构型,其中分子内氢键起关键作用
不饱和脂质中的C=C键是典型的具有两个不同取代基的1,2-二取代双键,可以通过不对称衍生化和离子淌度分离来鉴定不饱和脂质中C=C键的顺反型。实验结果验证了作者的猜想,顺式不饱和脂肪酸进行N-tosylaziridine衍生化后,其母离子的离子淌度谱中呈现单峰,而反式脂肪酸呈现双峰。对其进行CID碎裂,产生特殊的子离子信号,以此鉴定C=C键的位置。
当然,仅仅依据母离子的离子淌度谱图来对脂质双键构型进行鉴定是不够的,一方面由于不同双键位置的同分异构体母离子质谱峰是相同的,相互之间势必造成干扰;另一方面面对多双键的情况,母离子淌度峰形无法说明每个双键的构型,这些问题在以往的方法中是难以解决的。本研究作者充分利用了TIMS质谱(淌度池-碰撞池)的仪器结构,母离子先进行淌度分离再进行碎裂,所以碎片离子的到达时间与形成该子离子的母离子理论上是相同的,而子离子可以反映双键的位置。作者利用子离子的淌度峰对双键构型进行鉴定,利用碎片峰对位置鉴定,进而实现了对双键位置和构型的同时检测。该方法也适用于多双键体系,由于存在多个反应位点,其母离子的淌度情况较为复杂,而利用子离子的淌度很好地对其进行了简化,容易得到不同位置双键各自的结构信息。
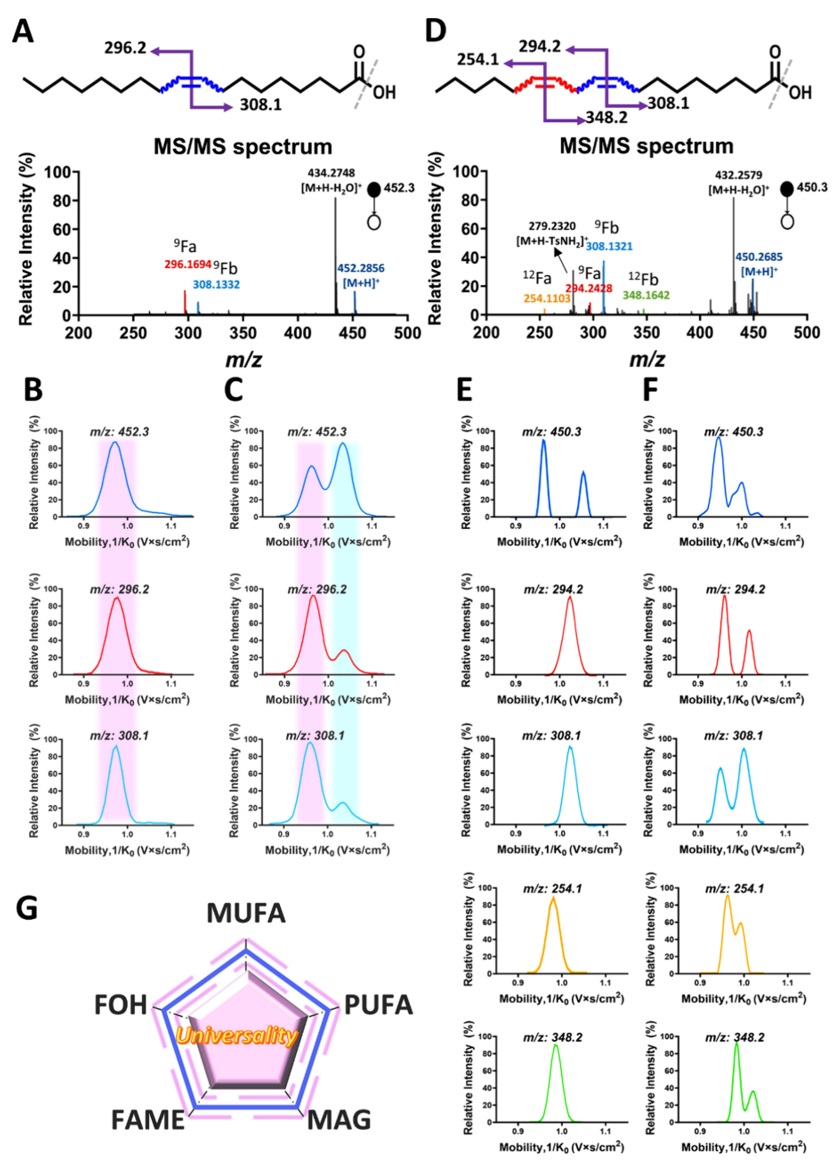
图2. 不对称衍生化用于识别不饱和脂质中C=C键的位置和顺反构型,以FA 18:1 (Δ9)和FA 18:2 (Δ9, Δ12)为例。(A) 衍生化FA 18:1 (9Z或9E)在m/z 452.3的MS/MS谱。(B,C)衍生化后(B) FA 18:1(9Z)和(C) FA 18:1 (9E)正离子模式下质子化前体离子及其产物离子的离子淌度谱。(D)衍生化FA 18:2(9Z, 12Z或9E,12E)在m/ z 450.3处的MS/MS谱。(E,F)衍生化(E) FA 18:2(9Z, 12Z)和(F) FA 18:2(9E, 12E)正离子模式下质子化前体离子及其产物离子的离子淌度谱。(G) 不对称衍生化体系用于识别不饱和脂质中双键的位置和顺反式构型的适用范围。
此外,作者对不同的加合离子峰进行分析时发现,只有质子化离子[M+H]+存在单双峰的差异。作者对此推测:分子内氢键增加了反式脂肪酸形成的两非对映异构体之间的差异。分子内氢键的存在通过1H NMR和理论计算进行了证明。
进一步,作者利用淌度相对峰面积对顺反异构体比例进行了定量分析,利用子离子峰强度对不同位置双键位置异构体进行相对定量,为复杂样品中不同C=C键的异构性的定量分析提供了新途径。
该方法被成功地应用于确定环境应激下细菌膜脂质中发生的C=C键的顺-反几何转换的检测和定位,并跟踪了大鼠脊髓损伤前后不饱和脂质的异构体分布情况。
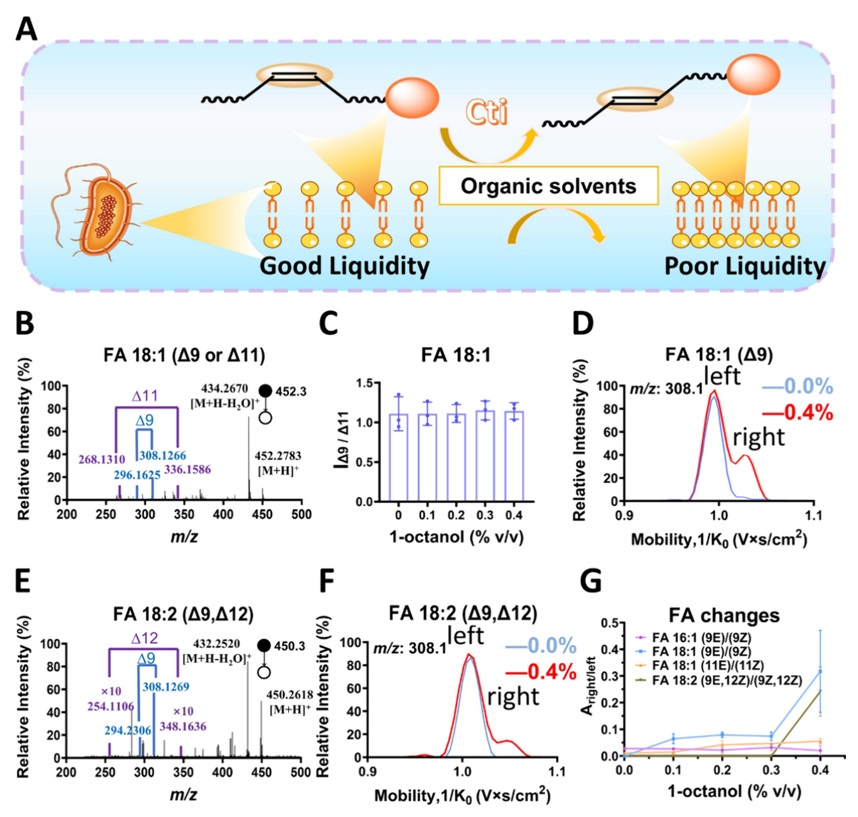
图3. 环境应激下细菌膜脂质中的双键的顺-反几何转换。 (A) 细菌脂质顺反异构化示意图。(B-D) 1-辛醇刺激下细菌中FA 18:1(Δ9或Δ11)的异构体变化情况。(E、F) 1-辛醇刺激下细菌中FA 18:2(Δ9, Δ12)的异构体变化情况。 (G) 1-辛醇刺激下细菌中几种脂肪酸的变化。
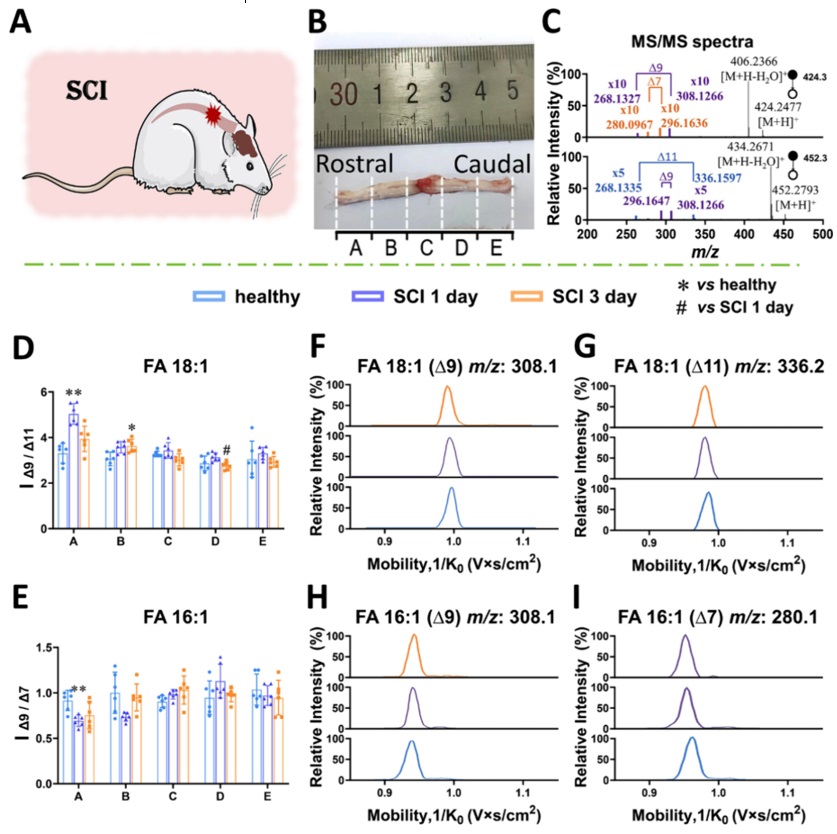
图4. 损伤前后大鼠不同脊髓节段中双键异构体比例的变化。(A)大鼠脊髓损伤示意图。(B)脊髓分段示意图。(C)衍生化FA 18:1(Δ9或Δ11)和FA 16:1 (Δ9或Δ7)的MS/MS谱。(D、E)不同节段中FA 18:1(Δ9或Δ11)和FA 16:1(Δ9或Δ7)位置异构体变化情况。(F-I) A节段FA 18:1(Δ9或Δ11)和FA 16:1(Δ9或Δ7)顺反异构体变化情况。
该成果近期发表在Journal of the American Chemical Society 上。吉林大学化学学院博士研究生唐帅为文章的第一作者,吉林大学化学学院国新华教授和中国科学院长春应用化学研究所王浩助理研究员为论文的共同通讯作者。国新华教授课题组长期从事生物质谱新技术和新方法的研究,及核酸二级结构的拉曼光谱分析。王浩博士长期从事质谱新技术和新方法的开发以及生物医用高分子研究。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Simultaneous Determination of the Position and Cis–Trans Configuration of Lipid C=C Bonds via Asymmetric Derivatization and Ion Mobility–Mass Spectrometry
Shuai Tang, Hao Wang*, Huihui Zhang, Mingyu Zhang, Jiancheng Xu, Chun Yang, Xuesi Chen, Xinhua Guo*
J. Am. Chem. Soc., 2024, DOI: 10.1021/jacs.4c08980
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!


































 京公网安备 11010802027423号
京公网安备 11010802027423号