JACS:活细胞内源性激酶活性调控的新策略
激酶在细胞信号转导中扮演着至关重要的角色,人工调控激酶活性对于深入理解激酶功能具有重要意义。目前的技术手段主要有遗传密码子拓展和融合蛋白质技术,然而这些技术需要引入外源性激酶,不可避免地对原始生理环境造成扰动,也不适用于很多的天然细胞。内源性激酶功能的关闭可通过选择性的小分子抑制剂实现,但人工操控内源性激酶功能的开启具有很大的挑战性。北京大学深圳研究生院潘峥婴(点击查看介绍)课题组提出了一种简便有效的光控共价调控剂(Opto-covalent modulator,OCM)策略,该方法糅合了激酶小分子共价抑制剂和光激活的脱笼化学两种技术,灵巧地实现了对人天然细胞中内源性激酶活性的关闭与开启。这一工作近期发表在Journal of the American Chemical Society 上,文章的第一作者是北京大学博士研究生翁伟智。
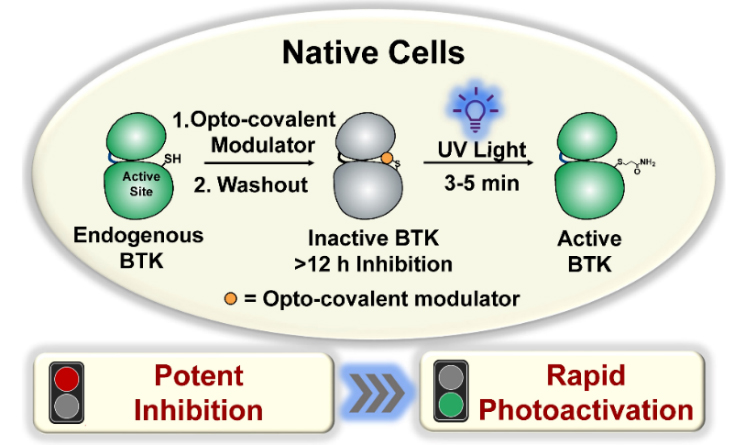
图1. 光控共价调控剂调控策略示意图。
以明星药物靶标布鲁顿激酶(BTK)为例,采用其创造的药物分子伊布替尼(Ibrutinib)为模板,潘峥婴课题组通过保留伊布替尼与BTK激酶的基本结合模式,在恰当位置引入光控基团,生成了光控共价调控剂OCM-1。在活细胞中,OCM-1高效抑制内源性BTK激酶的活性,简单的洗脱即可除去游离的化合物以大幅减少脱靶作用,而再经过3-5分钟的光照便能快速恢复激酶的活性。光控共价调控剂在多种类型的B淋巴瘤/白血病细胞株和人原代外周血单核细胞中都展现出优异的调控效果。
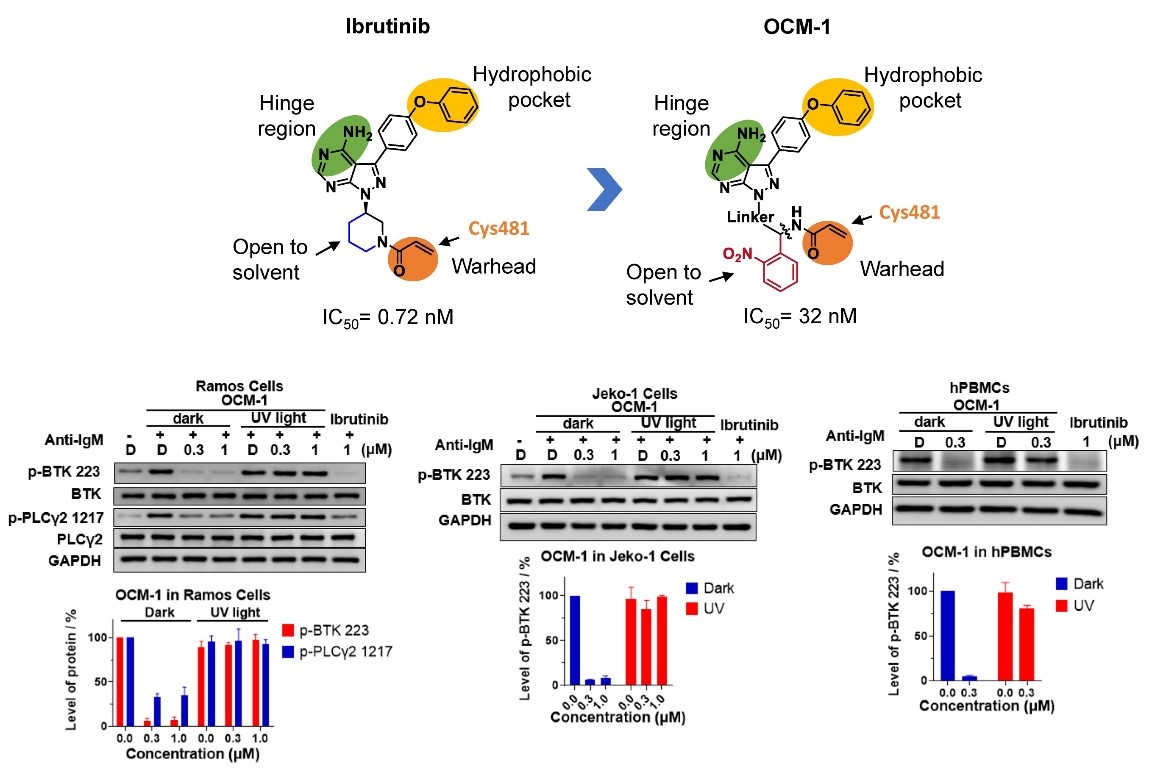
图2. 光控共价调控剂OCM-1高效调控活细胞中内源性BTK激酶的活性。
对比需要基因操作的方法,光控共价调控剂策略直接适用于天然细胞内源性激酶,具有对生物体系扰动小、适用性广、操作简单等明显的优点;而且随着激酶共价抑制剂的快速发展,该策略适用范围也越加广泛。光控共价调控剂(OCM)策略通过在活细胞中直接操作内源性激酶,帮助深化对细胞信号转导乃至生命进程的理解,也有利于新颖药物的研发。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Potent Inhibition and Rapid Photoactivation of Endogenous Bruton’s Tyrosine Kinase Activity in Native Cells via Opto-Covalent Modulators
Weizhi Weng, Ping Zhang, and Zhengying Pan*
J. Am. Chem. Soc., 2024, 146, 28717–28727, DOI: 10.1021/jacs.4c06459
导师介绍
潘峥婴
https://www.x-mol.com/university/faculty/17148
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!































 京公网安备 11010802027423号
京公网安备 11010802027423号