智能自组装¹⁹F探针技术:提升生物代谢小分子的高效检测
传统监测方法在应对复杂的生物基质及结构相似的分析物时,常面临灵敏度和分辨率的限制,影响了检测结果的准确性。近日,中国科学院有机化学研究所的赵延川(点击查看介绍)团队研发了一种新型自组装19F标记核磁共振(NMR)探针,该探针通过与核苷酸等小分子结合,触发探针的解聚集过程,进而激活19F核磁共振信号,生成独特的信号指纹,进而在分子层面实现复杂体系的原位多组分实时检测 (图1)。这项技术为生物机制研究、酶动力学分析、药物筛选及疾病诊断等领域提供了新的解决方案。
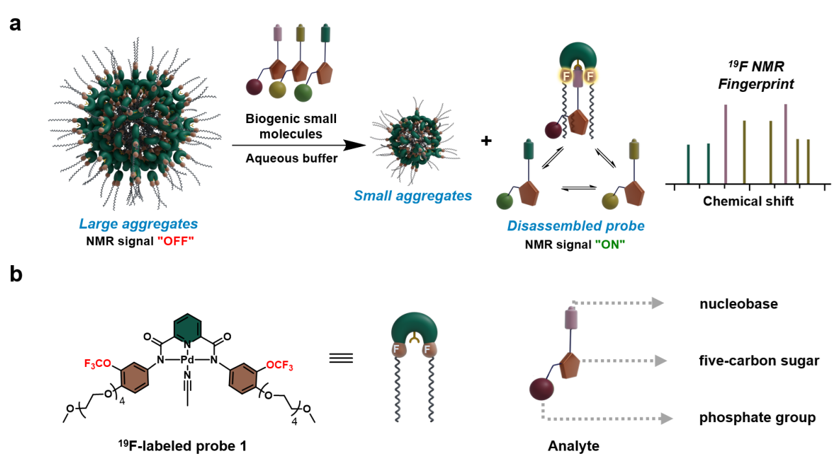
图1. 智能自组装含氟探针检测原理示意图。图片来源:Angew. Chem. Int. Ed.
传统原位检测方法在面对复杂的生物样品时,难以区分结构相似的分析物,而本研究报道的新型探针通过其自组装和解聚机制,能够在与不同生物分子结合时,产生独特的19F NMR指纹信号,精确识别和区分多种分析物。以核苷酸为例,探针能够同时识别并区分八种常见的DNA和RNA组成单元,包括AMP、GMP、CMP、UMP等。不同核苷酸产生各自独特的19F信号,因而在复杂混合物中依然能够准确区分每种组分 (图2)。作者还评估了蛋白质等生物大分子对检测的影响,结果表明,即使在存在蛋白质等干扰物质的情况下,探针仍能保持良好的检测性能。此外,通过添加内标分析物,这一检测方法可以实现对样品中的组分进行定量分析,进一步增强了其在实际生物样品检测中的应用潜力。
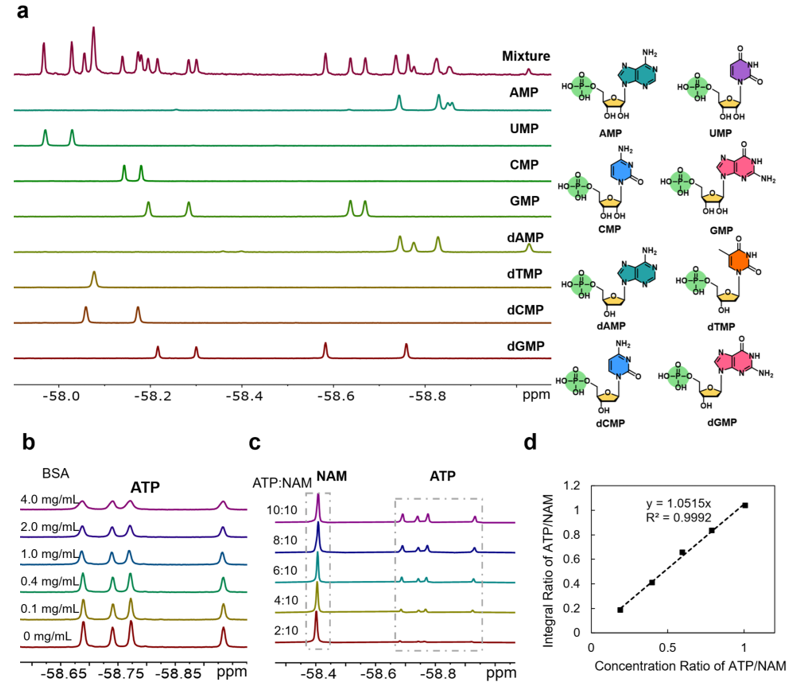
图2. 使用 19F 标记探针检测小分子代谢物。图片来源:Angew. Chem. Int. Ed.
该方法可以用于生物代谢过程的实时检测,以ATP水解酶Apyrase活性的检测为例,当探针与ATP、ADP和AMP结合时,将产生与各分析物对应的独特19FNMR信号。这些信号的强度变化能够精确追踪ATP在Apyrase催化下的逐步水解过程。具体表现为,随着反应的进行,ATP信号逐渐减弱,而ADP信号先是增强然后减弱,AMP信号则持续增强。此外,通过对不同来源的Apyrase样品进行检测,该系统能够区分其ATPase与ADPase的活性,从而证实该技术在酶活性评估及质量控制中的应用价值 (图3)。这种19F标记的探针为酶促反应的实时监测提供了一种高效工具,不仅能精确评估酶活性,还适用于药物筛选。随着此技术的进一步普及与应用,其将在疾病诊断和生物技术领域发挥更大的作用。
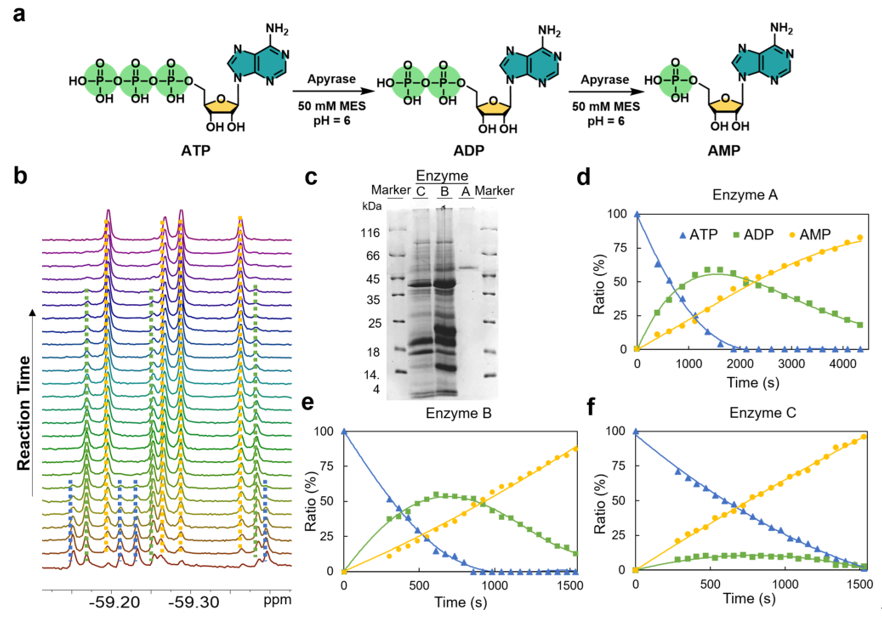
图3. 多步酶促反应的原位实时监测。图片来源:Angew. Chem. Int. Ed.
这一成果近期发表在Angew. Chem. Int. Ed.上,上海有机所赵延川课题组的徐振创博士、王晨阳硕士、何胜源硕士为该论文的共同第一作者,赵延川研究员为通讯作者。该工作得到了国家自然科学基金和中国科学院上海有机化学研究所先进氟氮材料重点实验室的经费支持。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Enhancing Molecular-Level Biological Monitoring with a Smart Self-Assembling 19F-Labeled Probe
Zhenchuang Xu,† Chenyang Wang,† Shengyuan He,† Jian Wu, Yanchuan Zhao*
Angew. Chem. Int. Ed., 2024, DOI: 10.1002/anie.202417112
赵延川研究员简介

赵延川,2007年本科毕业于吉林大学化学系;2012年获中科院上海有机化学研究所理学博士学位;之后在美国麻省理工学院化学系从事博士后研究。2017年5月加入中国科学院上海有机化学研究所先进氟氮材料重点实验室,任课题组长。在包括J. Am. Chem. Soc., Angew. Chem. Int. Ed., Chem. Rev., Cell Reports Phys. Sci., JACS Au, Anal. Chem. Macromolecules等学术刊物发表论文70余篇。研究团队一直致力于基于时空维度调控的新型有机功能分子的研究。发展了基于分子识别的色谱核磁共振分析方法,检测中无需分离,无需标记,实时在线地得到类似于色谱峰的检测信号,精准对应复杂体系中的各个组分。发展了新型仿生离子受体—calix[4]trap (杯芳烃离子阱),其具有目前文献报道最高的K+/Na+选择性。
课题组近期计划招收博士后1名,从事磁共振和核医学影像方面的研究,欢迎有志于从事相关研究的优秀人才加入。
赵延川
https://www.x-mol.com/university/faculty/65906
课题组网站
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



































 京公网安备 11010802027423号
京公网安备 11010802027423号