新冠mRNA疫苗在人类血液中的分布研究
注:文末有研究团队简介及本文科研思路分析
在新冠疫情大流行期间,mRNA疫苗以其卓越的效果和快速研发速度脱颖而出,尤其是由Moderna公司开发的SPIKEVAX mRNA疫苗已成为全球范围内重要的疫苗之一。该疫苗通过脂质纳米颗粒(Lipid Nanoparticles, LNP)包裹信使核糖核酸(mRNA),并将其递送至细胞内,随后由细胞翻译生成抗原蛋白,诱发免疫反应。然而,尽管疫苗的临床效果显著,对其在人体内的分布和代谢过程仍然缺乏充分的研究。
由澳大利亚皇家墨尔本理工大学(RMIT)居易博士带领的研究团队与墨尔本大学Stephen Kent教授合作,开展了针对新冠mRNA疫苗在人体血液中的分布和代谢过程的研究,特别聚焦于其mRNA和脂质成分的动力学特征。该团队对19名受试者进行了研究,这些受试者接种了Moderna SPIKEVAX新冠疫苗,并在疫苗接种后的不同时间点收集血液样本,检测疫苗成分在血液中的浓度及其衰减模式。
研究表明,疫苗接种后1-2天,脂质纳米颗粒中的mRNA和可离子化脂质在血液中的浓度达到峰值,随后呈现出指数衰减的趋势。具体而言,mRNA在血液中的浓度峰值为0.19 ng/mL,离子化脂质的峰值为3.22 ng/mL。研究还显示,该疫苗的mRNA在接种后14-15天内仍可在37%的受试者体内检测和定量分析,而可离子化脂质则在7天内衰减至背景水平。
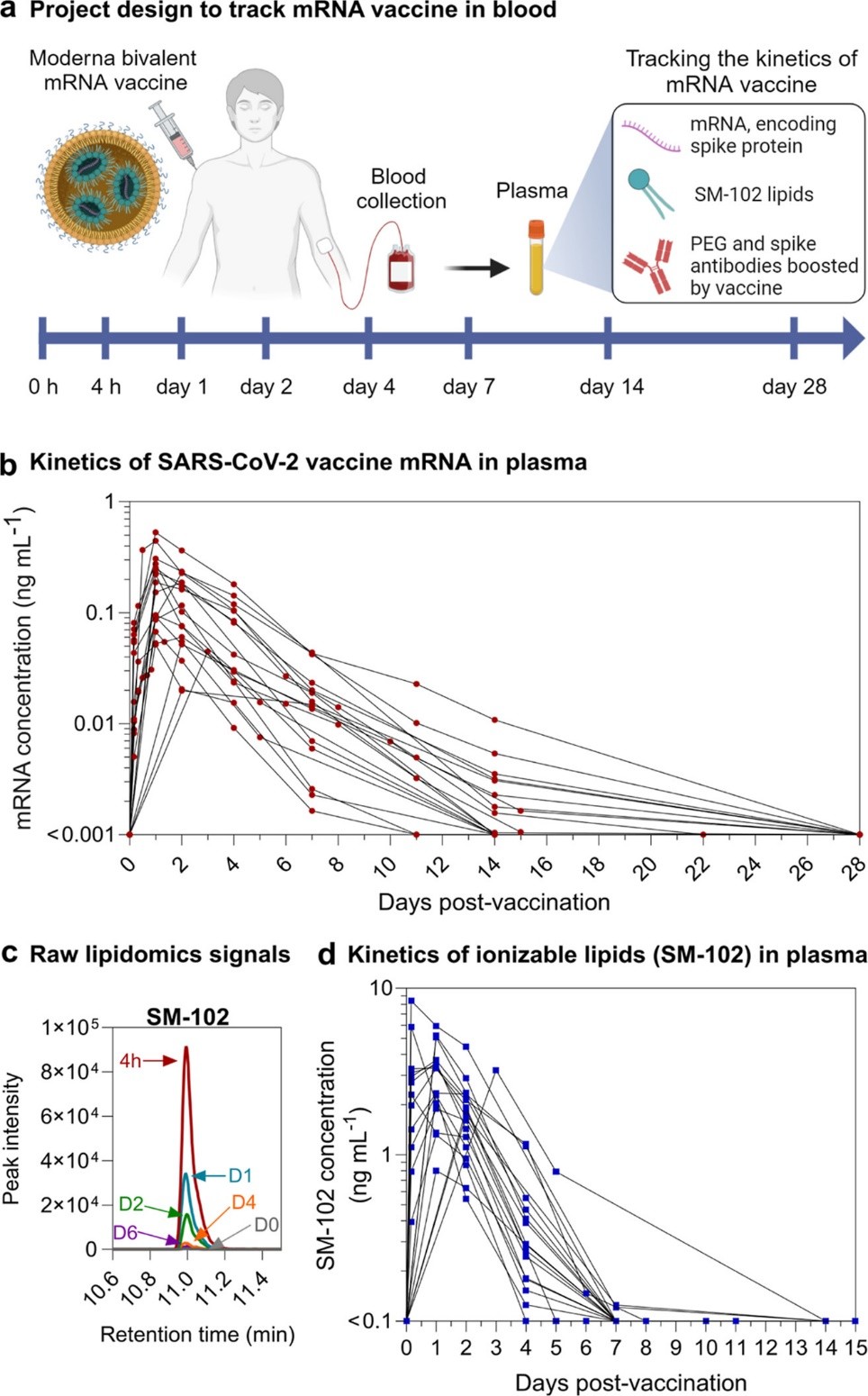
图1. mRNA疫苗中的mRNA和离子化脂质在血液中的衰减。图片来源:ACS Nano
研究特别关注了疫苗中聚乙二醇(PEG)对免疫系统的影响。PEG是纳米颗粒外层的成分,研究发现,尽管PEG抗体的存在未显著影响疫苗的代谢速率,但mRNA和可离子化脂质的血液浓度与PEG特异性抗体水平有关,并且单核白细胞吞噬脂质纳米颗粒的能力与PEG抗体在血液中的增高成负相关。

图2. 人体血液实验用于研究脂质纳米颗粒和免疫细胞的相互作用。图片来源:ACS Nano
本研究为了解新冠 mRNA疫苗在人类体内的分布提供了新的见解,并揭示了PEG抗体在疫苗代谢中的潜在作用。研究结果不仅有助于优化未来疫苗的设计,还对其他基于纳米颗粒的治疗手段具有借鉴意义。
这一成果近期发表在ACS Nano 上,文章的第一作者是墨尔本大学Stephen Kent教授和RMIT 博士后研究员李诗瑶。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Blood Distribution of SARS-CoV-2 Lipid Nanoparticle mRNA Vaccine in Humans
Stephen J. Kent, Shiyao Li, Thakshila H. Amarasena, Arnold Reynaldi, Wen Shi Lee, Michael G. Leeming, David H. O’Connor, Julie Nguyen, Helen E. Kent, Frank Caruso, Jennifer A. Juno, Adam K. Wheatley, Miles P. Davenport, Yi Ju
ACS Nano, 2024, 18, 27077–27089, DOI: 10.1021/acsnano.4c11652
居易博士简介

居易博士是RMIT大学博士生导师,澳大利亚研究委员会 (ARC) Discovery Early Career Researcher Award (DECRA) 获得者。他于2017年在墨尔本大学获得博士学位,导师是Frank Caruso教授,之后在墨尔本大学进行博士后研究。2021年,他作为副校长博士后研究员(Vice-Chancellor’s Postdoctoral Fellow)转到RMIT大学任职。在此期间,他于2023年在Victora Fellowship的资助下前往曼彻斯特大学进行海外研究访问。他的研究兴趣涵盖基础的生物–纳米相互作用研究和开发用于靶向药物和基因递送的新型纳米颗粒的转化研究。他的工作在材料科学和纳米技术的多个方面具有开创性。例如,他的研究表明个体特异性的生物分子冠层可以调节纳米颗粒与人体血液中的免疫细胞相互作用(ACS Nano 2020),并且他还证明了针对新冠开发的mRNA疫苗能够在人体血液中诱导PEG聚合物特异性抗体(ACS Nano 2022 和 Nat. Rev. Immunol. 2023)。他的研究成果已发表在69篇同行评审的期刊文章中,被引用超过4000次,平均FWCI为3.44。他目前担任《Journal of Materials Science》期刊副主编,并担任澳大利亚皇家化学学会 (RACI) 维多利亚分会的委员会成员。
https://www.rmit.edu.au/contact/staff-contacts/academic-staff/j/ju-dr-yi-david
科研思路分析
Q:这项研究最初是什么目的?或者说想法是怎么产生的?
A:尽管mRNA疫苗的主要作用是发生在局部淋巴结,但之前的研究表明小剂量的mRNA会出现在被接种疫苗者的母乳中。我们希望通过量化血液中mRNA和脂质成分的浓度来更好地理解这种现象。并且疫苗中的mRNA和脂质纳米颗粒在人体的代谢尚未被深入研究。之前的研究表明,PEG是一种常用于纳米颗粒的成分,可能会引发人体的免疫反应。我们因此假设,PEG特异性抗体可能会影响mRNA疫苗在血液中的清除速度。
Q:研究过程中遇到哪些挑战?
A:要在如此复杂的生物体系中,准确、灵敏地检测出极低浓度的mRNA和脂质成分,我们必须开发精细的检测方法。我们使用了数字滴定聚合酶链式反应和质谱等高精度检测手段,成功量化了血液中的疫苗成分。研究过程中检测到的疫苗成分量相对较低,且存在个体差异,这给我们在数据分析和结果解释上带来了复杂性,我们需要进行深入的统计分析以揭示疫苗成分在血液中的动态变化。此外,我们需要进一步厘清PEG抗体和疫苗代谢之间的关系,尽管抗体水平与疫苗成分存在相关性,但实际对代谢过程的影响不如预期明显,这提示该现象的机制可能比简单的免疫反应更加复杂,未来希望有相关领域的研究者一起合作将相关研究推动到更高的层次。
Q:该研究成果可能有哪些重要的应用?哪些领域的企业或研究机构可能从该成果中获得帮助?
A:研究揭示了疫苗成分的分布和代谢动力学,以及PEG抗体的免疫反应对纳米颗粒药物的影响,这有助于帮助制药公司进一步优化mRNA疫苗及药物的设计,增强其安全性和有效性,减少副作用。对于专注于纳米颗粒药物传递系统的公司可以参考这项研究来改进纳米颗粒的设计,以避免免疫系统清除,从而提高药物的生物利用度。从事免疫反应、抗体研究的科研机构可将该研究的PEG抗体研究成果应用于抗体生成机制的进一步探索,从而为新型免疫疗法的发展提供支持。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!



















































 京公网安备 11010802027423号
京公网安备 11010802027423号