厦门大学朱志课题组JACS:细胞外囊泡的聚糖指纹图谱分析助力液体活检
细胞外囊泡(EVs)是细胞分泌的纳米/微米级脂质双层囊泡,携带着丰富的聚糖,这些聚糖在细胞间通讯和疾病进展中发挥着重要作用。然而,由于EVs在体液中的异质性以及聚糖结构的复杂性,检测EVs聚糖一直存在挑战。最近,厦门大学化学化工学院的朱志教授(点击查看介绍)研究团队成功开发了一种膜特异性分离和凝集素诱导EV聚集(MESSAGE)策略,实现了血浆中EV聚糖图谱的快速、高灵敏、选择性分析,并用于结直肠癌(CRC)精准早期诊断、转移监测。
研究人员基于EVs的膜结构及其表面聚糖的特性,使用带有去硫生物素标记的膜特异性识别探针,在10倍稀释的血浆样本中无偏倚地捕获纳米级EV。利用链霉亲和素包被的磁珠进行有效地富集,同时排除游离的糖蛋白。随后,通过竞争性识别机制释放EV。分离出的EV与凝集素一起孵育,以靶向并识别EV表面存在的聚糖结构。通过凝集素诱导的EV聚集策略,将EV聚糖表达转化为动态光散射(DLS)可检测的尺寸信号。此外,使用癌症特异性凝集素组合进行EV聚糖的多重分析产生了疾病衍生EV的独特聚糖指纹。并与机器学习集成,从而可在复杂体液中实现疾病特征的早期检测,并能够特异性评估癌症转移(图1)。
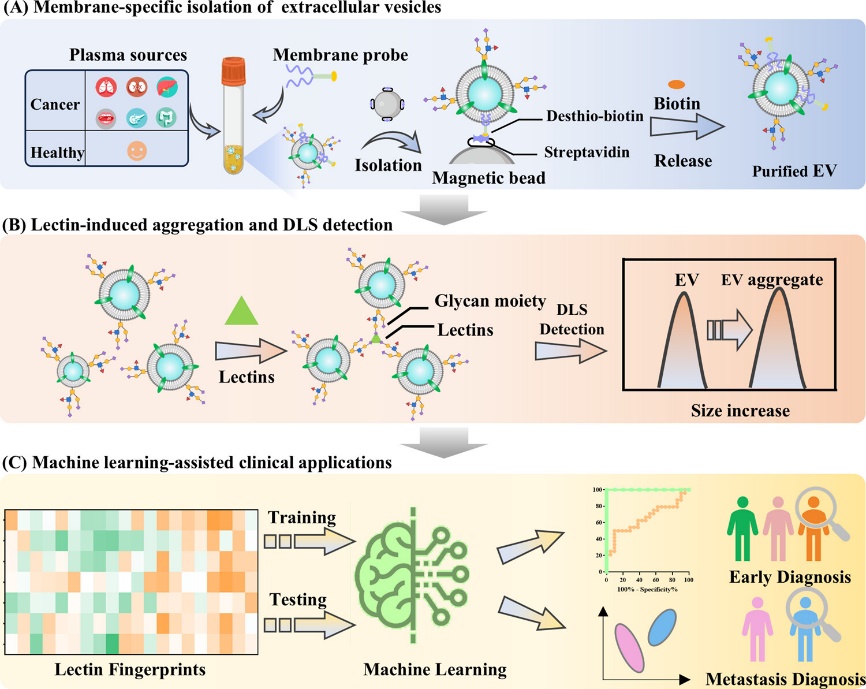
图1. 膜特异性分离和凝集素诱导EV聚集(MESSAGE)策略,用于EV聚糖直接检测的原理。图片来源:J. Am. Chem. Soc.
利用膜特异性分离和竞争释放的技术,研究人员成功捕获了EV。与EV分离的金标准方法超速离心法(UC)相比,膜特异性分离的EV在纯度、时间、效率及其生物活性等方面均有较好的性能。进一步,研究人员利用释放后EV表面聚糖与凝集素的特异性相互作用,使得单分散的EV变成EV簇,实现将EV聚糖表达信息成功转化为DLS可检测的尺寸大小信息(图2)。
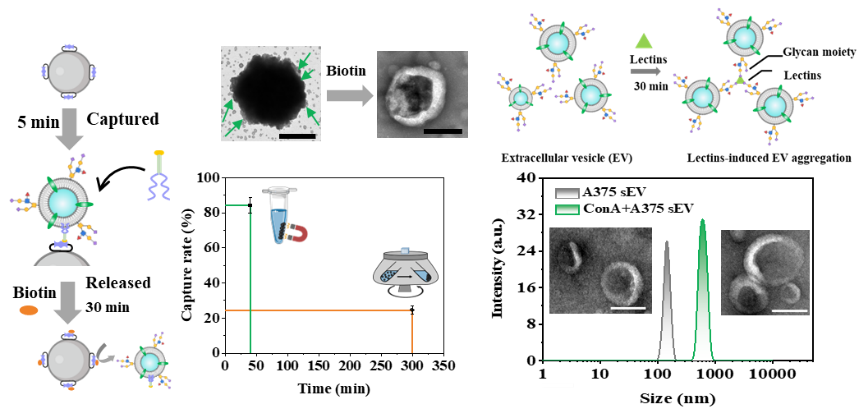
图2. MESSAGE策略的可行性验证。图片来源:J. Am. Chem. Soc.
借助MESSAGE策略的高特异性和高灵敏性,研究人员绘制六种不同癌症的聚糖指纹图谱,研究发现不同癌症的EV聚糖表达存在显著异质性,结合机器学习的方法,有效的实现不同种类癌症的精准分类(图3)。
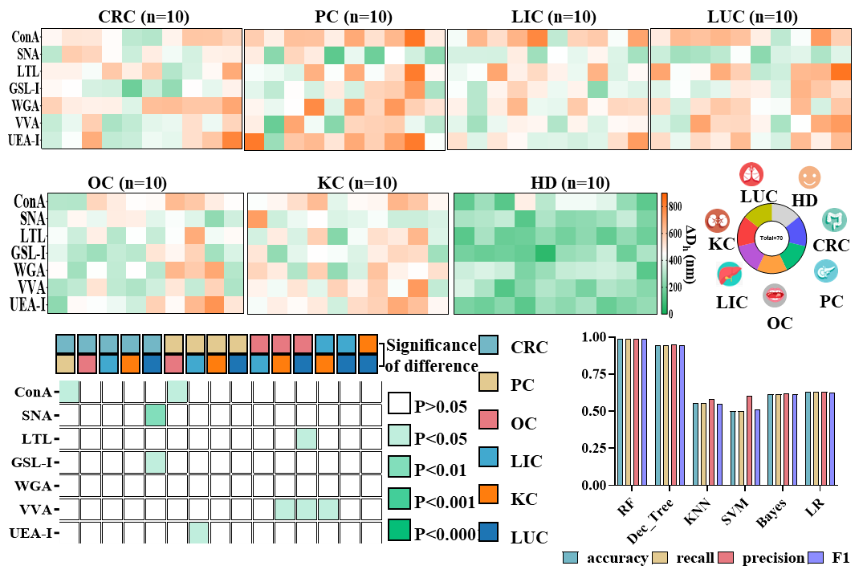
图3. 机器学习助力EV聚糖凝集素指纹图谱的癌症分类。图片来源:J. Am. Chem. Soc.
进一步,研究人员将MESSAGE技术应用在结直肠癌(CRC)的早期诊断及转移监测。利用MESSAGE获取临床血浆EV聚糖图谱。基于机器学习算法构建EV聚糖特征,实现了CRC精准诊断,且准确率达到100%。在CRC转移监测方面,EV聚糖特征对癌症发生转移的判断准确率达到88.5%,并可作为CRC患者是否发生转移的标志物(图4、图5)。
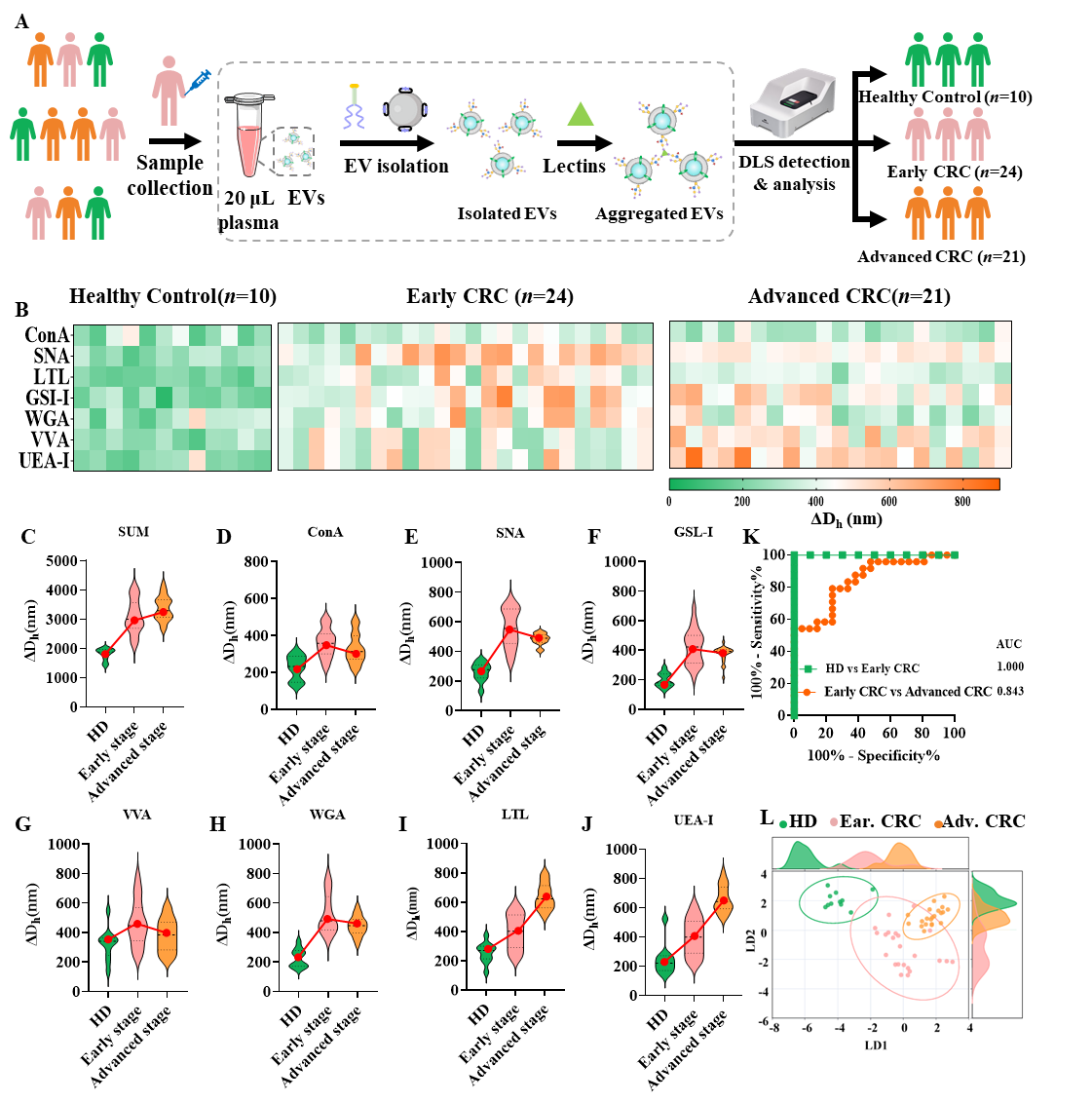
图4. MESSAGE策略在结直肠癌早期诊断中的应用。图片来源:J. Am. Chem. Soc.
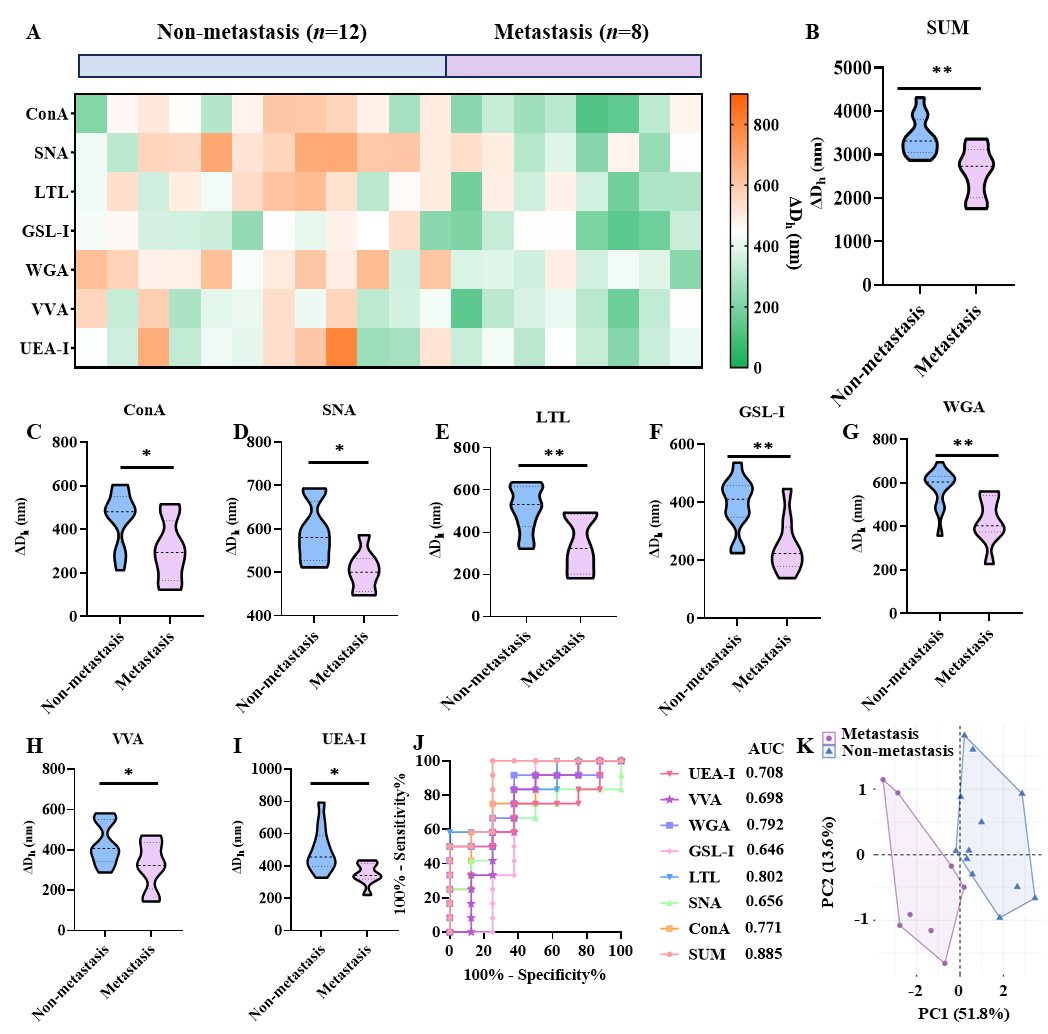
图5. MESSAGE策略在结直肠癌转移监测中的应用。图片来源:J. Am. Chem. Soc.
综上所述,该技术在疾病筛查和进展监测方面展现出显著潜力,特别是在癌症诊断与监测领域。该技术不仅具备快速、非侵入性、可扩展性以及高精确度等优势,而且通过融合机器学习算法,显著提升了数据处理的精确性。此外,研究表明,EV聚糖可以作为液体活检的潜在生物标志物,为精准医疗领域提供了一种新的工具。这一发现不仅拓宽了液体活检的应用范围,而且为个性化医疗策略的实施提供了科学依据。
这一成果近期发表在Journal of the American Chemical Society 上,厦门大学化学化工学院博士研究生张桂华为论文第一作者,厦门大学朱志教授为论文通讯作者。该工作得到国家重点研发计划和国家自然科学基金的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Fingerprint Profiling of Glycans on Extracellular Vesicles via Lectin-Induced Aggregation Strategy for Precise Cancer Diagnostics
Guihua Zhang, Xiaodan Huang, Yanli Gong, Yue Ding, Hua Wang, Huimin Zhang, Lingling Wu, Rui Su, Chaoyong Yang, Zhi Zhu*
J. Am. Chem. Soc. 2024, DOI: 10.1021/jacs.4c10390
导师介绍
朱志
https://www.x-mol.com/university/faculty/14205
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号