长春应化所林君/马平安/丁彬彬团队:多酶模拟钼铜双原子纳米酶触发氧化应激级联扩增用于高效协同癌症治疗
单原子纳米酶(SAzyme)具有极高的原子利用率和媲美天然酶的催化性能,被广泛应用于活性氧(ROS)介导的肿瘤治疗。然而,催化反应中间体在单原子活性位点上较高的反应能垒,以及肿瘤微环境(TME)中过表达的谷胱甘肽(GSH)等还原性物质限制了肿瘤细胞氧化应激的扩增过程,导致治疗效果不理想。尽管具有多样化催化活性位点的双原子纳米酶(DAzyme)有望实现不同金属原子的互补功能和协同作用,其在癌症治疗中的应用仍处于起步阶段。
近期,中国科学院长春应用化学研究所林君研究员、马平安研究员和丁彬彬副研究员团队报道了一种具有多酶模拟催化活性的钼铜双原子纳米酶用于高效协同癌症治疗。相关工作发表在期刊Angew. Chem. Int. Ed.上。该团队通过简单的主客体原位组装及高温热解策略构建了具有多种催化活性位点的钼铜双原子纳米酶(MoCu DAzyme),并将其用于类酶催化/光热协同抗肿瘤治疗 (图1)。(1) MoCu DAzyme具有类过氧化物酶(POD)、氧化酶(OXD)、谷胱甘肽氧化酶(GSHOx)和烟酰胺腺嘌呤二核苷酸磷酸(NADPH)氧化酶(NOX)活性,可通过产生多种ROS、耗竭GSH并阻断其再生实现氧化应激的级联扩增,诱导肿瘤细胞凋亡;(2) 较之于催化活性位点单一的钼单原子纳米酶(Mo SAzyme),铜原子的引入、双原子位点的形成、以及各活性位点间的协同催化作用显著增强催化底物吸附,降低反应中间体能垒,赋予MoCu DAzyme更强的类酶催化活性;(3) 得益于非晶态的氮掺杂碳基底,MoCu DAzyme具有优异的近红外二区(NIR-II)光热转换性能,可实现高效的光热治疗;并通过升温促进ROS生成,增强类酶催化治疗的疗效。
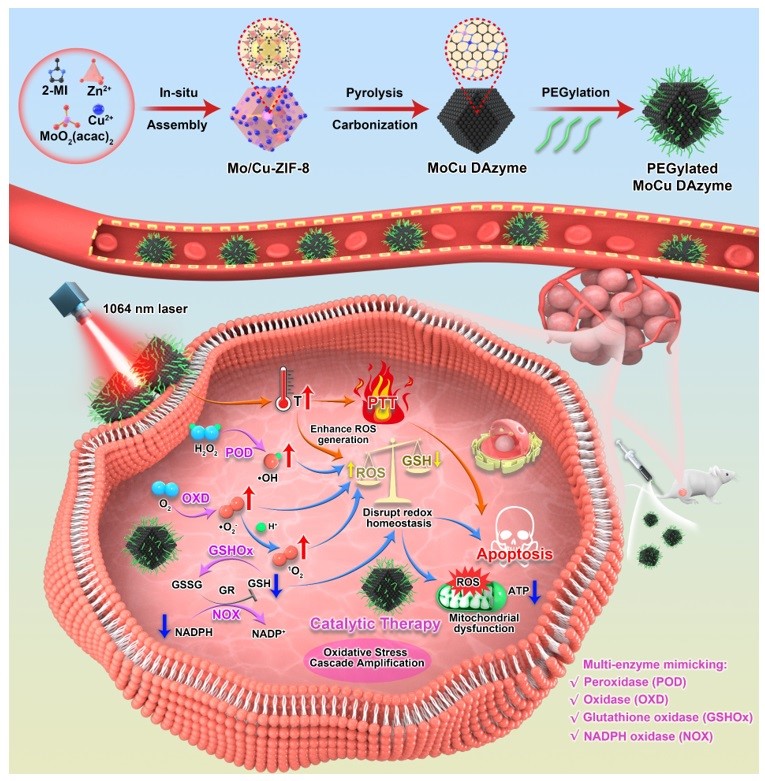
图1. MoCu DAzyme的制备路径及其用于协同肿瘤治疗的机制示意图。
作者通过透射电子显微镜(TEM)、能量色散X射线谱(EDS)元素映射、X射线衍射(XRD)等表征证实了MoCu DAzyme的成功合成。通过像差校正高角度环形暗场扫描透射电子显微镜(AC-HAADF-STEM)及其线扫描强度分布图等分析初步验证了单原子位点和双原子位点的共存(图2)。
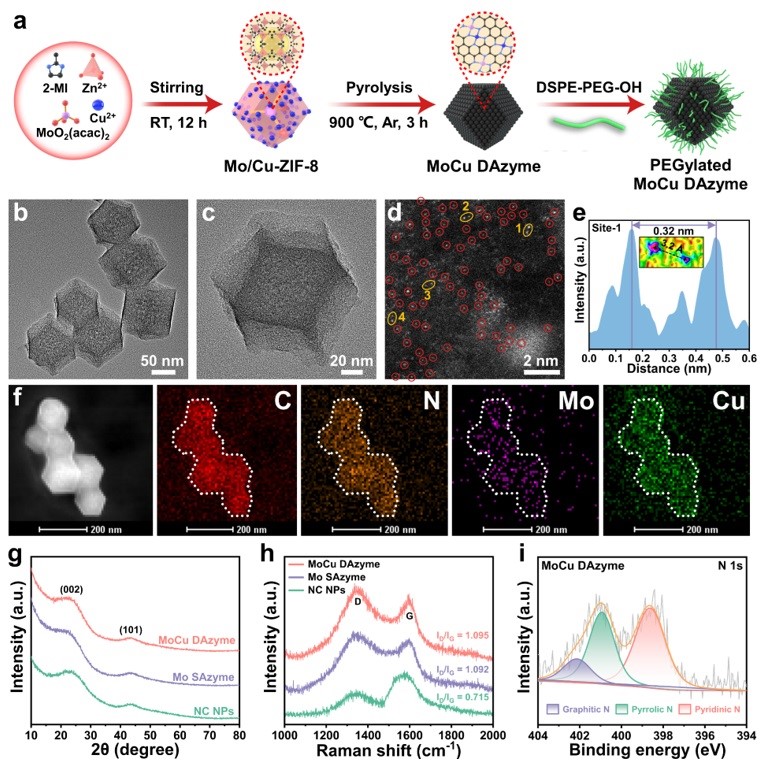
图2. MoCu DAzyme的制备路径及表征。
通过基于同步辐射光源的X射线吸收近边结构(XANES)和扩展X射线吸收精细结构(EXAFS)谱表征了MoCu DAzyme中Mo和Cu原子的氧化态和配位环境,并证实了双原子位点的存在。MoCu DAzyme同时具有Mo单原子、Cu单原子和Mo-Cu双原子活性位点(图3)。
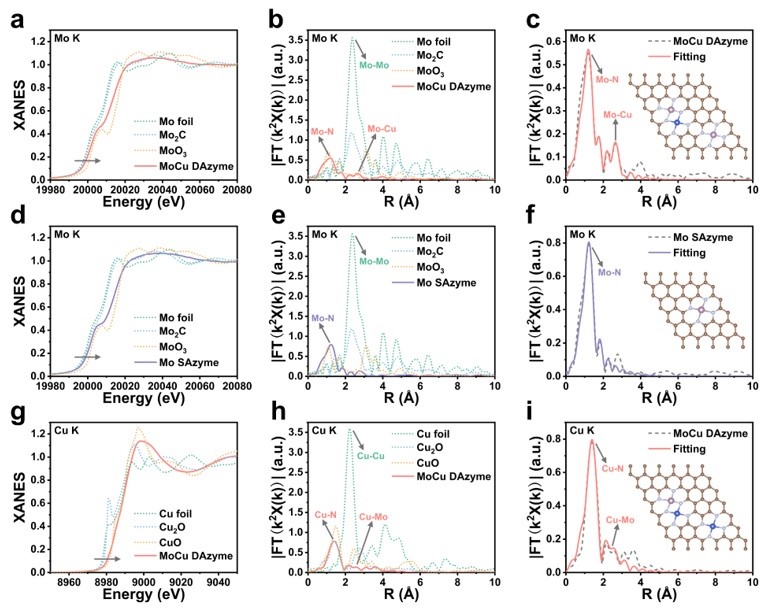
图3. MoCu DAzyme和Mo SAzyme基于同步辐射光源的相关表征。
MoCu DAzyme具有优异的光热转换性能,可用于1064 nm近红外光(NIR)触发的光热治疗。MoCu DAzyme具有类POD、OXD、GSHOx和NOX活性,且上述类酶催化活性均优于Mo SAzyme,可通过产生多种ROS、耗竭GSH、消耗NADPH进而阻断GSH再生,实现基于氧化应激级联扩增策略的多酶模拟催化治疗(图4)。
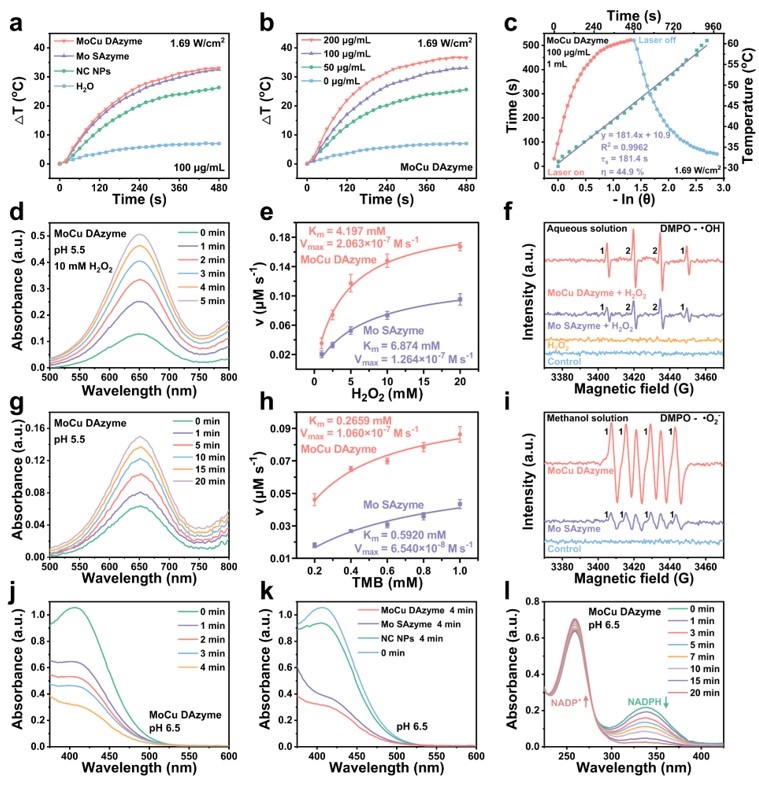
图4. MoCu DAzyme的光热转换和类酶催化性能。
为了深入探究MoCu DAzyme类酶催化活性优于Mo SAzyme的潜在机理,作者以类POD活性为例,采用密度泛函理论计算(DFT)分析了各催化活性位点的反应机理和自由能变化。计算结果表明,Mo-Cu双原子位点和Cu单原子位点对H2O2分子的吸附能力均强于Mo单原子位点,且双原子位点的吸附能绝对值最高,更有利于底物吸附。对于生成羟基自由基(• OH)的限速步骤,Mo-Cu双原子位点和Cu单原子位点的催化反应中间体能垒均低于Mo单原子位点,且双原子位点的能垒最低,更有利于限速步骤的进行。因此,MoCu DAzyme催化活性的增强可归因于引入少量Cu原子后,Mo-Cu双原子位点和Cu单原子位点的形成,以及多种活性位点的协同催化作用(图5)。
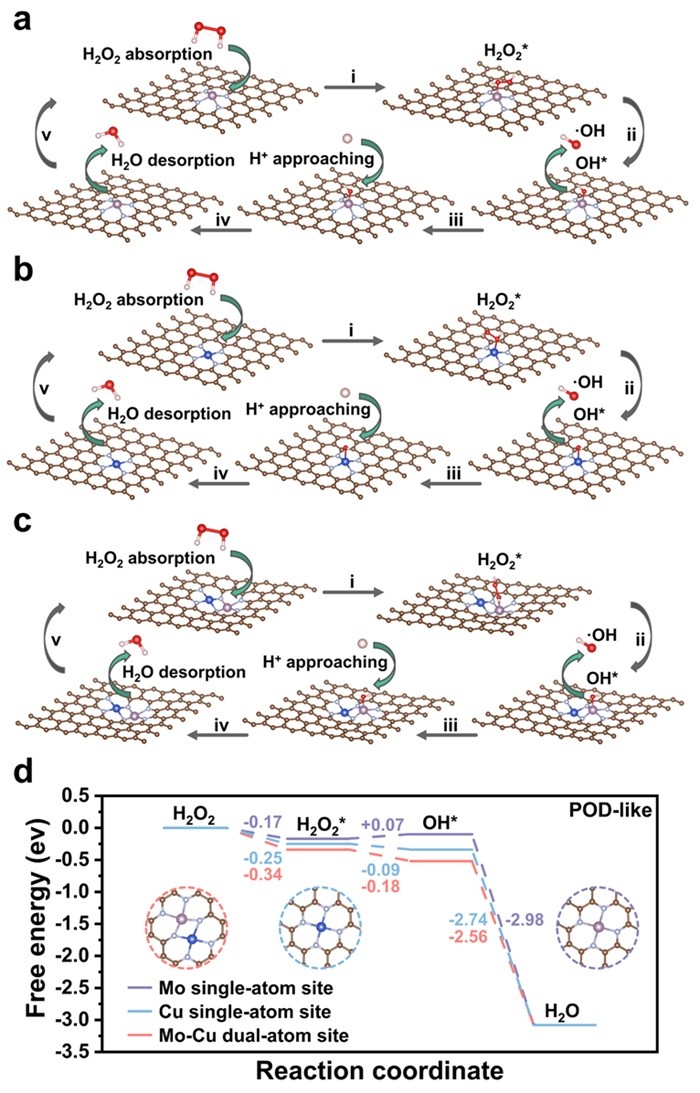
图5. 各催化活性位点的反应机理和自由能变化图。
细胞实验验证了MoCu DAzyme的体外抗肿瘤性能及相关作用机制。细胞毒性和凋亡流式实验表明MoCu DAzyme对小鼠乳腺癌(4T1)细胞具有高于Mo SAzyme的细胞毒性,且在NIR照射下表现出明显增强的肿瘤细胞杀伤能力。MoCu DAzyme 可通过产生ROS、消耗GSH和 NADPH有效放大肿瘤细胞内的氧化应激,从而导致线粒体功能障碍和细胞内ATP含量下降,且NIR照射能进一步增强上述作用(图6)。
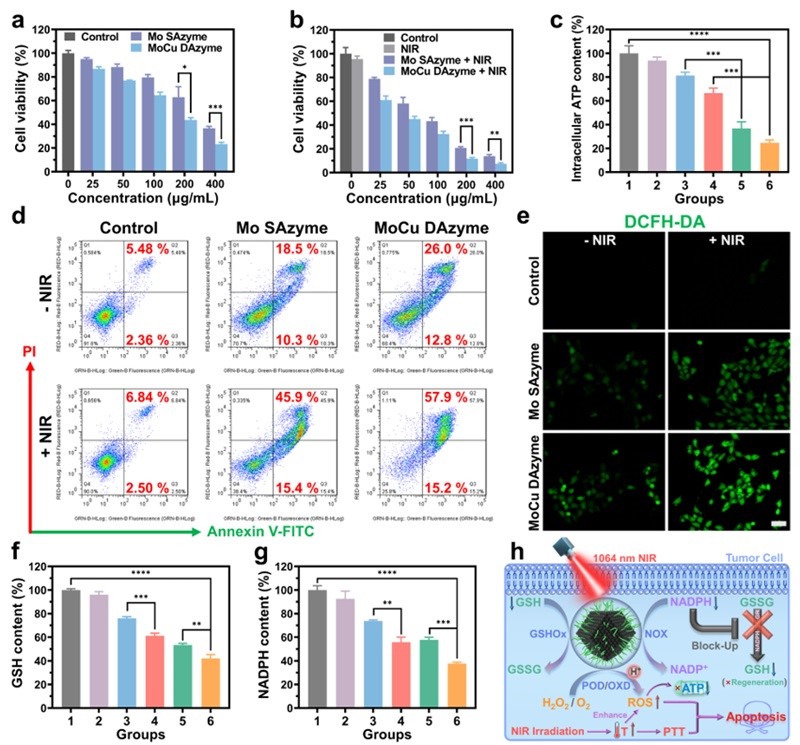
图6. MoCu DAzyme的体外治疗效果评估。
最后,该团队构建了Balb/c小鼠4T1荷瘤模型来验证MoCu DAzyme的体内抗肿瘤治疗效果。治疗期内的肿瘤体积变化、治疗结束后切除肿瘤的数码照片、肿瘤抑制率、肿瘤质量和各类肿瘤组织染色切片均证实了在NIR照射下MoCu DAzyme能有效抑制肿瘤生长,实现高效协同的肿瘤治疗(图7)。
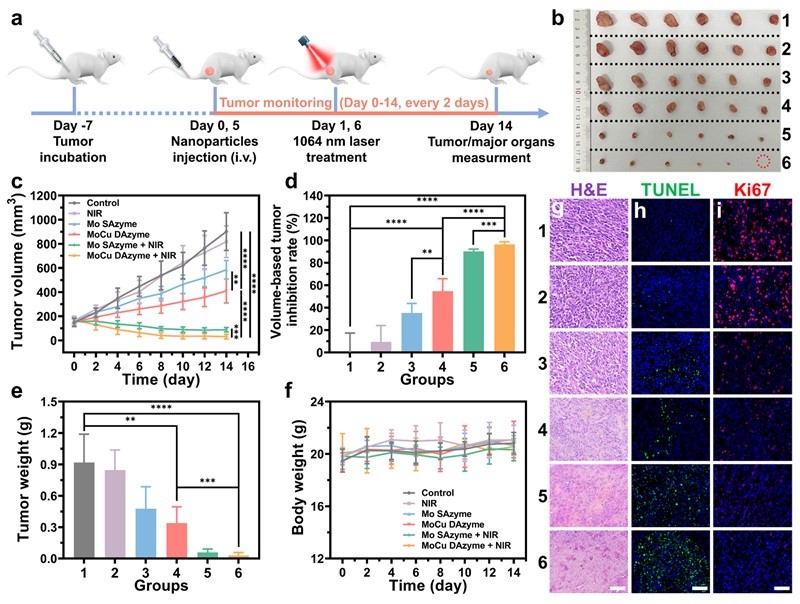
图7. MoCu DAzyme的体内协同抗肿瘤治疗。
综上所述,本文成功构建了具有多种催化活性位点和多酶模拟催化活性的钼铜双原子纳米酶(MoCu DAzyme)。与钼单原子纳米酶相比,铜原子的引入、双原子位点的形成以及各活性位点间的协同催化作用显著增强了底物吸附,降低了反应能垒,从而使MoCu DAzyme具有更强的催化性能。得益于上述类酶催化活性,MoCu DAzyme不仅能产生多样化的ROS,还能消耗GSH并阻断其再生过程,从而触发氧化应激的级联扩增。此外,得益于强烈的光学吸收,MoCu DAzyme也具有优异的光热转换性能。因此,MoCu DAzyme可实现高效的类酶催化/光热协同抗肿瘤治疗。这项工作有望推进双原子纳米酶的治疗应用,并为纳米催化癌症治疗提供更多有价值的见解。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Multi-Enzyme Mimetic MoCu Dual-Atom Nanozyme Triggering Oxidative Stress Cascade Amplification for High-Efficiency Synergistic Cancer Therapy
Ziyao Li, Binbin Ding, Jing Li, Hao Chen, Jiashi Zhang, Jia Tan, Xinyu Ma, Di Han, Ping'an Ma, Jun Lin
Angew. Chem. Int. Ed., 2024, DOI: 10.1002/anie.202413661
通讯作者简介

丁彬彬,中国科学院长春应用化学研究所副研究员,国家优青,吉林省高层次人才。2015年本科毕业于合肥工业大学,2020年博士毕业于中国科学院长春应用化学研究所,后留所工作至今。目前已发表论文70余篇,其中以第一/通讯作者(含共同)在Adv. Mater.(2篇)、J. Am. Chem. Soc.(2篇)、Angew. Chem. Int. Ed.(6篇)、Coord. Chem. Rev.(2篇)、Adv. Funct. Mater.、Adv. Drug Deliver. Rev.、Nano Lett.(2篇)等杂志上发表论文40余篇(IF≥10的24篇),申请中国发明专利10余项(授权6项)。主持包括博新计划、国家自然科学基金优秀青年基金/面上/青年等项目8项。获吉林省自然科学一等奖(3/5)和中国科学院院长特别奖(1/1)等奖励。目前担任中国稀土学会发光专业委员会委员,Exploration期刊学术编辑以及Nano Mater. Sci.、Asian. J. Pharm. Sci.、IMed等期刊青年编委。

马平安,中国科学院长春应用化学研究所研究员,博士生导师,国家优秀青年基金获得者(2019),吉林省中青年科技创新团队负责人。2010年毕业于东北师范大学,获博士学位。主要研究方向为无机纳米材料及生物医学应用。在Adv. Mater.、J. Am. Chem. Soc.、Angew. Chem. Int. Ed.、Nano Lett.、Mater. Today、Adv. Sci.、Biomaterials等国际学术期刊上发表SCI论文150余篇,被他人正面引用11000余次,H-index为59。获得吉林省自然科学一等奖(2022,排名第1)等科研奖励6项;主持国家自然科学基金、国家重点研发计课题等科研项目10余项。担任中国稀土学会发光专业委员会秘书长、稀土晶体专业委员会委员、稀土生物医学专业委员会委员、中国核学会分会理事,以及“Chinese Chemical Letters”、“Nano Research”、“中国稀土学报”、“分析化学”、“应用化学”等期刊编委/青年编委。
https://www.x-mol.com/university/faculty/281066

林君,中国科学院长春应用化学研究所研究员,博士生导师,国家杰出青年基金获得者,英国皇家化学会会士,科技部重点领域创新团队负责人,中国稀土学会理事,中国稀土学会发光专业委员会主任,Scientific Reports、中国稀土学报(中英文版)和发光学报编委。2002年获得国家杰出青年科学基金;2004年获得国务院政府特殊津贴;2007年入选“新世纪百千万人才工程国家级人选”;2017年入选万人计划“科技创新领军人才”。课题组自2000年以来一直从事纳-微米结构发光材料的控制合成、形态结构和性能调控及其在显示照明及生物医学领域的应用基础研究。在各种稀土发光材料的形貌控制技术、发光薄膜及其图案化技术、特色FED发光材料、多功能稀土上转换发光材料在生物成像和药物控制传递与释放等方面做出了具有原始创新和国际影响的研究工作。曾经/正在承担科技部973项目子课题、国家自然科学基金杰出青年基金项目、重点项目以及若干面上项目和国际合作项目。2009年和2014年分别获吉林省科技进步一等奖和吉林省自然科学一等奖。2014-至今连续入选“汤森路透全球材料领域高被引科学家”名录。至今已在国内外核心期刊如Chem. Rev.、Chem. Soc. Rev.、Mater. Today、J. Am. Chem. Soc.、Adv. Mater.、Angew. Chem. Int. Ed.、Adv. Funct. Mater.、ACS Nano、Nano Lett.等上面发表学术论文900余篇,截止目前这些论文共被他人引用8万余次(H指数145);获授权中国发明专利12项。应邀参加和参与组织国内外重要学术会议并做邀请报告100余次;获得2020年度中科院优秀导师奖,培养博士硕士研究生80余人(其中2人获得中国科学院院长特别奖,6人获得中国科学院院长优秀奖)。
https://www.x-mol.com/university/faculty/15805
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号