Nature:钯催化不对称合成间二取代苯的电子等排体
芳环骨架广泛存在于天然产物、生物活性分子以及功能材料中。特别是在生物活性分子中,引入芳环骨架具有多重作用,例如:1)芳环的刚性通常会限制可用的分子构象,进而降低芳香骨架与靶受体结合的熵成本;2)芳环可参与独特的非共价键相互作用,从而增强对受体结合位点的吸引力;3)芳环可与其它试剂发生交叉偶联,进而有助于快速构建和筛选不同的化合物库。然而,芳环骨架也会给药物开发带来不利影响,比如对药物分子的代谢稳定性、溶解度和亲脂性的影响。此外,平面的芳环缺乏三维立体性,而大多数药物靶点的结合口袋是手性的,这也限制了含芳环骨架药物分子的发现。为了解决上述问题,科学家开发了芳环的电子等排体——双环烷烃骨架(图1a),同时经过合适的设计,此类分子骨架不仅可以保留芳环的构象限制,而且还可以避免对药物分子的不利影响。另一方面,由于多数生物相关受体是手性的,因此不对称电子等排体的手性可能会增强或阻碍衍生配体与其同源受体的结合作用,例如:当MK-5108与有丝分裂激酶Aurora A的非活性DFG-out状态结合时(图1b),MK-5108的间二取代芳烃被置于Leu 139和Gly 216之间的疏水口袋中;若不对称苯电子等排体占据此结合口袋时,其在受体的上部区域占据更多空间或许更合适。此外,配体与其互补受体的“锁钥配合”可提高结合特异性,并且随着化合物中手性中心数量的增加,配体混杂性会降低。因此,迫切需要开发一种方法来控制整个分子的绝对构型以提高多种药物的作用效果。
近日,美国波士顿学院James P . Morken、Eranthie Weerapana以及斯坦福大学James K. Chen等研究者合作,利用Pd催化策略高对映选择性地将烃衍生前体转化为一种新型的间二取代苯环的电子等排体——含硼的3,5-二取代nortricyclanes(降三环庚烷),其C3和C5之间的键距(2.4 Å vs 2.4 Å)和键角(127° vs 120°)几乎与间二取代苯环相同(图1c)。此外,将降三环庚烷引入药物骨架中可以显著改善生物物理性质以及立体化学依赖的活性。相关成果发表在Nature 上。
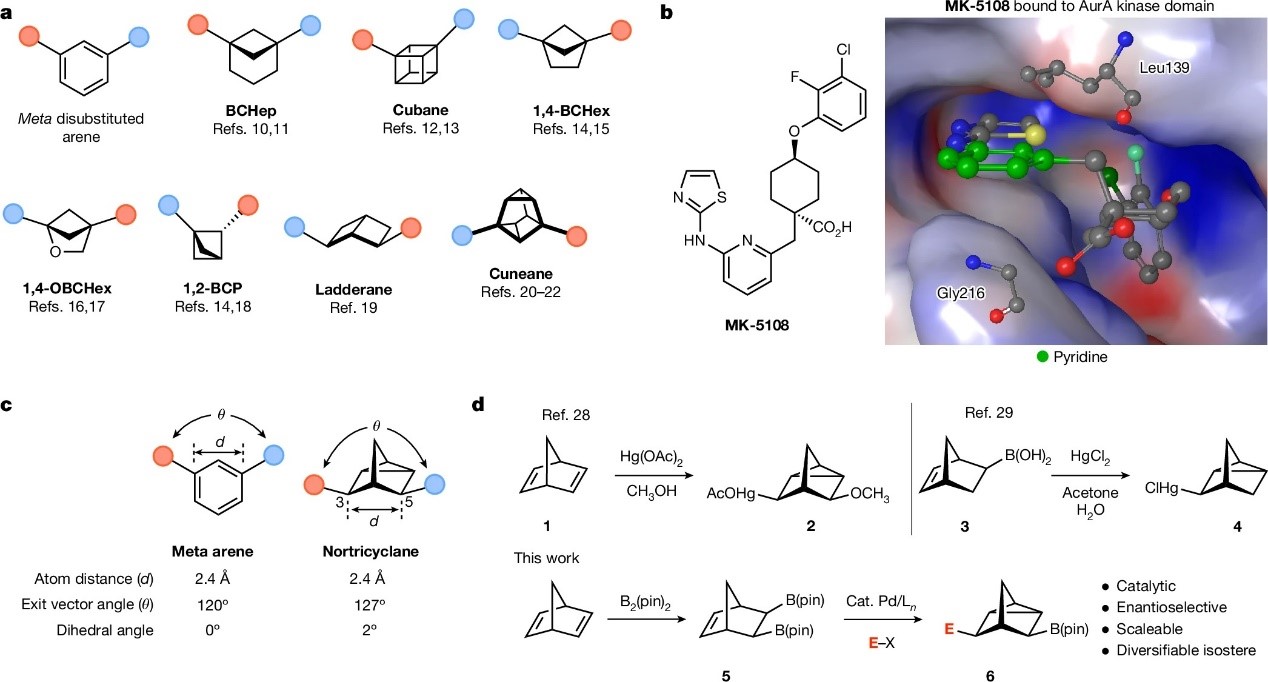
图1. 饱和双环烷烃作为芳香环的电子等排体替换。图片来源:Nature
先前的研究表明双环降冰片二烯骨架(1)凭借其两个π键之间的空间相互作用,在加入合适的亲电试剂后便可将双环[2.2.1]骨架转化为降三环庚烷(2,图1d);同时双环有机金属化物(3)经类似的亲电活化可导致闭环C-C键形成,从而获得降三环庚烷骨架(4)。基于此,作者试图利用催化量钯和有机亲电试剂来替代上述反应中的汞盐,同时经闭环和亲电试剂加成两步来合成降三环庚烷。事实上,当将此反应用于手性间二取代苯电子等排体的模块化构建时,作者发现内消旋二硼底物(5,室温稳定且易大规模制备)在催化量Pd(OAc)2和手性双芳基单膦配体L1的作用下能够有效进行对映选择性关环反应并生成手性降三环庚烷(6),6同时含有新引入的有机取代基和硼酸酯基团。在最优条件下,作者对亲电试剂的底物范围进行了考察(图2a),结果显示一系列带有吸/供电子基团的芳基溴化物(7-13、15-19)、杂芳基溴化物(14、20-23)甚至非芳香族亲电试剂(24、25)均可兼容该反应,以良好至优异的产率和对映选择性获得相应产物,不过强吸电子硝基取代的芳基溴化物(16)会降低对映选择性。其次,作者以廉价易得的市售降冰片二烯和B2(pin)2为原料,以克级规模合成了双(硼酸酯)底物5(图2b),5在0.5 mol% Pd(OAc)2的作用下实现了5 mmol规模反应,但需要将反应时间延长至24 h。此外,作者还对产物7的硼酸酯进行了衍生化(图2c),包括:Zn基催化交叉偶联(26)、Cu催化烯丙基化和羧基化(27和28)、直接胺化(29)、同系化(30)或氧化为醇(31)。
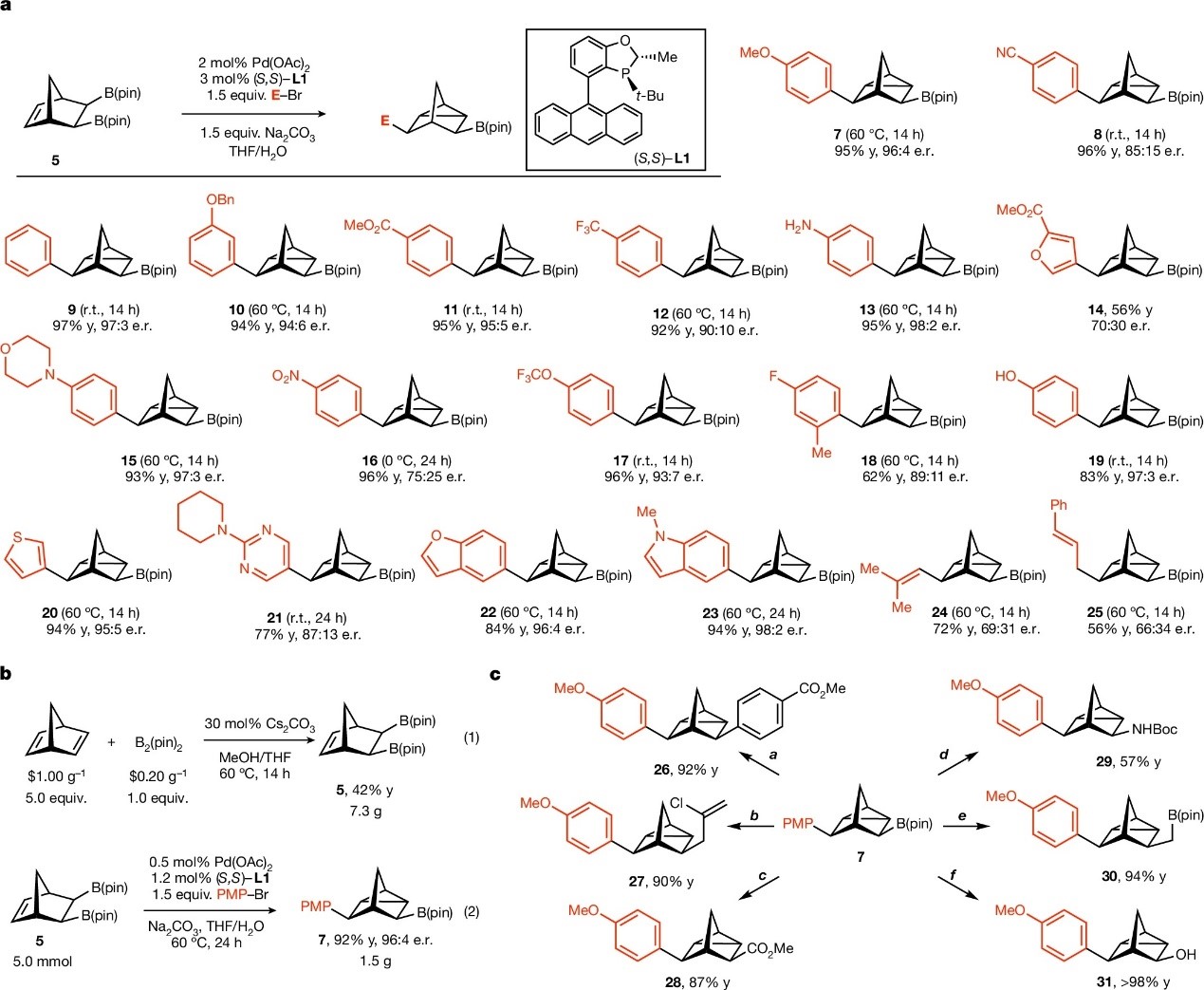
图2. 底物拓展及其衍生化。图片来源:Nature
接下来,作者通过密度泛函理论(DFT)计算对反应机理进行了研究(图3a),研究表明LPd(0)先与亲电试剂进行氧化加成,随后与32配位生成Pd-烯烃络合物(GS0),后者进行碳钯化时有两种途径:1)在path A(红色)中,烯烃经过渡态TS1a(0.7 kcal mol-1)进行碳钯化并产生Pd(II)中间体GS1a,再经过渡态TS2a进行罕见的Pd(II)置换,其中有机硼充当亲核试剂同时释放和还原金属;2)在path B(蓝色)中,当与Pd(II)结合时烯烃可能变得足够亲电,进而经过渡态TS1b(18.7 kcal mol-1)进行亲核钯化并生成GS1b,然后直接还原消除即可得到产物。另外,计算研究表明碳钯化途径的能垒比亲核钯化步骤低得多,但是从GS1a进行罕见的Pd(II)置换时TS2a的能垒为19.4 kcal mol-1(图3c)。值得注意的是,TS1a的13C KIE计算结果与Singleton实验确定的结果非常吻合(图3b),并且钯催化5的偶联反应在C2处KIE可忽略不计,这与碳钯化机理相一致。综上,这些结果证明碳钯化是对映选择性决定步骤,并且计算研究表明生成次要异构体的过渡态结构是将双环庚烷基的CH2桥直接置于空间受阻的蒽环体系之下(图3d),而主要异构体的过渡态构象则避免了此种相互作用。
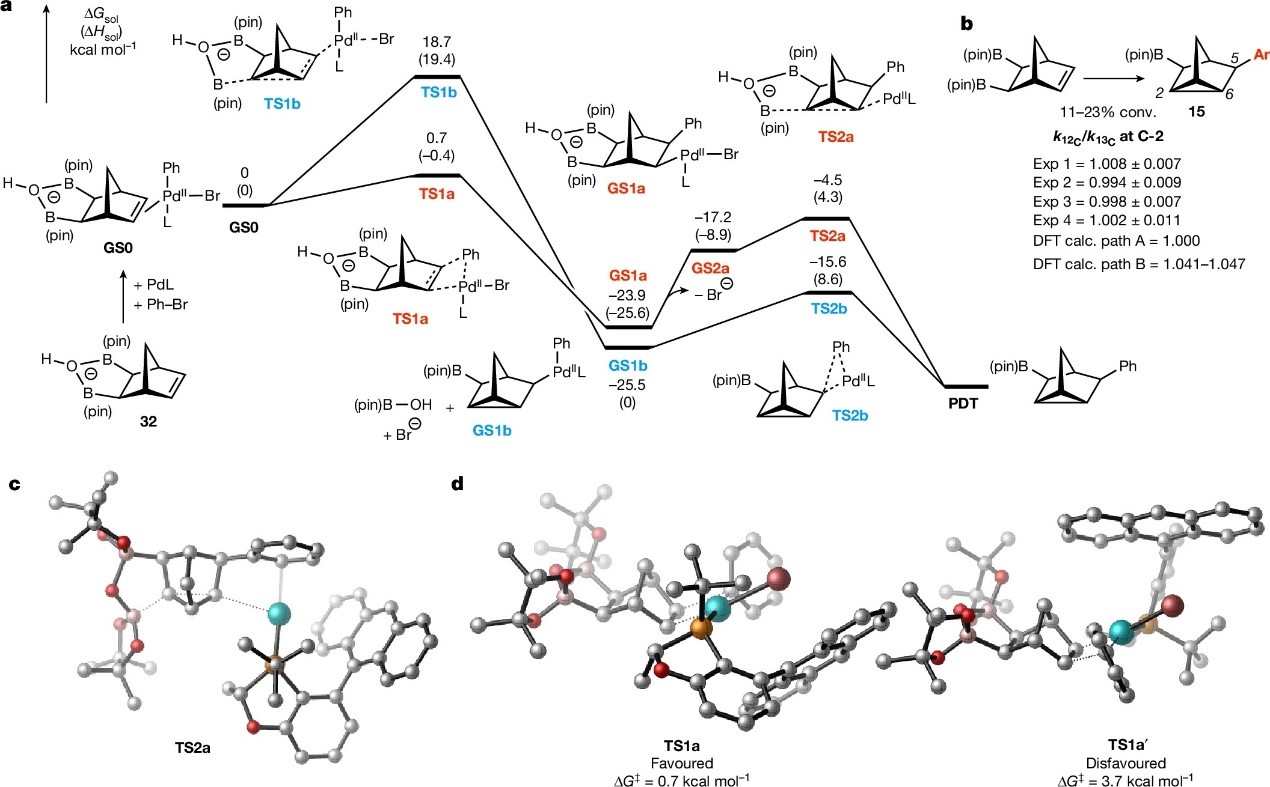
图3. 机理研究。图片来源:Nature
最后,作者将降三环庚烷骨架引入生物活性分子并对其理化性质进行了研究。具体而言:将脂肪酸酰胺水解酶(FAAH)抑制剂URB597中的苯环替换为降三环庚烷便可制备两种电子等排体(R,S)-33和(S,R)-33(图4a),两者分子量与URB597相似,但其在水性缓冲液中的溶解度增加了10倍,同时保持相当的亲脂性(α log D)。此外,小鼠肝微粒体测定表明两种等排体类似物相对于URB597表现出明显增加的代谢稳定性;而基于活性的蛋白质定量分析实验表明尽管(R,S)-33和(S,R)-33的活性远不如URB597,但这两种等排体类似物仍然具有抑制FAAH的能力并且表现出不同的抑制作用。类似地,将Hedgehog(Hh)通路抑制剂sonidegib中的苯环替换为降三环庚烷便可制备等排体(S,R)-34和(R,S)-34(图4b)。通过双荧光素酶测定法在Shh-LIGHT2细胞中进行测定,作者发现(S,R)-34和(R,S)-34对Hh信号的抑制作用为微摩尔级(IC50分别为0.50 μM 和0.20 μM),并且两种立体异构体的活性差异不大(P=0.26)。总体而言,降三环庚烷等排体的初步分析符合预期,并且用C(sp3)基等排体替换芳环后可使溶解度提高10-50倍。值得一提的是,降三环庚烷等排体(33和34)的立体化学依赖性活性似乎强化了形状在与生物靶标结合时很重要,但是即使未重新优化以结合其靶标受体的等排体类似物,也会检测到活性差异。
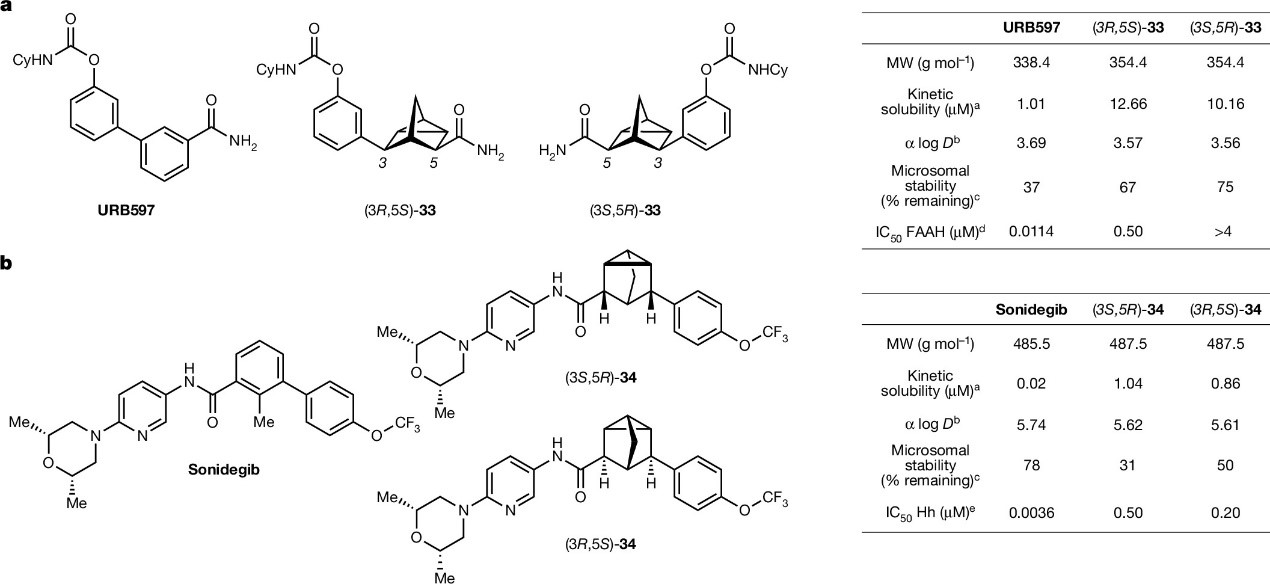
图4. 药代动力学研究。图片来源:Nature
总结
本文研究团队利用Pd催化策略以高对映选择性将烃衍生前体转化为新型的间二取代苯环的电子等排体——含硼的3,5-二取代降三环庚烷,其C3和C5之间的键距和键角几乎与间二取代苯环相同。此外,将降三环庚烷引入药物骨架中可以显著改善理化性质以及立体化学依赖的活性,从而为后续的药物研发开辟了新路线。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Catalytic asymmetric synthesis of meta benzene isosteres
Mingkai Zhang, Matthew Chapman, Bhagyesh R. Sarode, Bingcong Xiong, Hao Liang, James K. Chen, Eranthie Weerapana, James P. Morken
Nature, 2024, DOI: 10.1038/s41586-024-07865-4
(本文由吡哆醛供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
































 京公网安备 11010802027423号
京公网安备 11010802027423号