香港中文大学夏江团队Angew:基于多肽相分离的细胞表面抗体化修饰及其在靶向细胞疗法方面的应用
细胞疗法例如CAR-T作为一种新型抗癌疗法,因其优异的精准性、有效性和安全性受到人们的广泛关注。为了进一步提高细胞疗法的疗效,通过免疫细胞表面工程化来改善免疫细胞的靶向性成为了相关领域的研究热点之一。虽然目前已有多种天然或者非天然的材料被用于免疫细胞的表面工程化研究,但是绝大多数策略并不能完美地模拟细胞外基质的动态环境,会对免疫细胞产生或多或少的影响。细胞外基质中的许多蛋白分子是高度聚集的、动态、流动的,既能与环境进行快速交流又能保持相对的独立结构,这一奇特现象被称为液-液相分离(Liquid-liquid phase separation, LLPS)。除了蛋白质等生物大分子之外,多肽也被发现可以产生液-液相分离。因此,如果能够通过LLPS模拟细胞外基质的动态环境来进行免疫细胞表面工程化修饰将是一种理想的策略。
在前期研究的基础上,香港中文大学夏江教授(点击查看介绍)团队发展了一种简便易操作的基于多肽相分离的免疫细胞表面工程化策略,将抗体修饰于自然杀伤细胞 (NK cell) 表面,实现了癌细胞的精准高效杀伤。
作者首先精心设计并且筛选了系列多肽,最终找到了形成相分离的三肽(Fmoc-Lys-Gly-Dopa-OH)。该多肽易于合成,在生理条件下就可以发生相分离,形成凝聚层液滴;通过简单的混合之后能够对不同的分子如小分子染料、核酸、蛋白质和抗体等进行有效的募集。
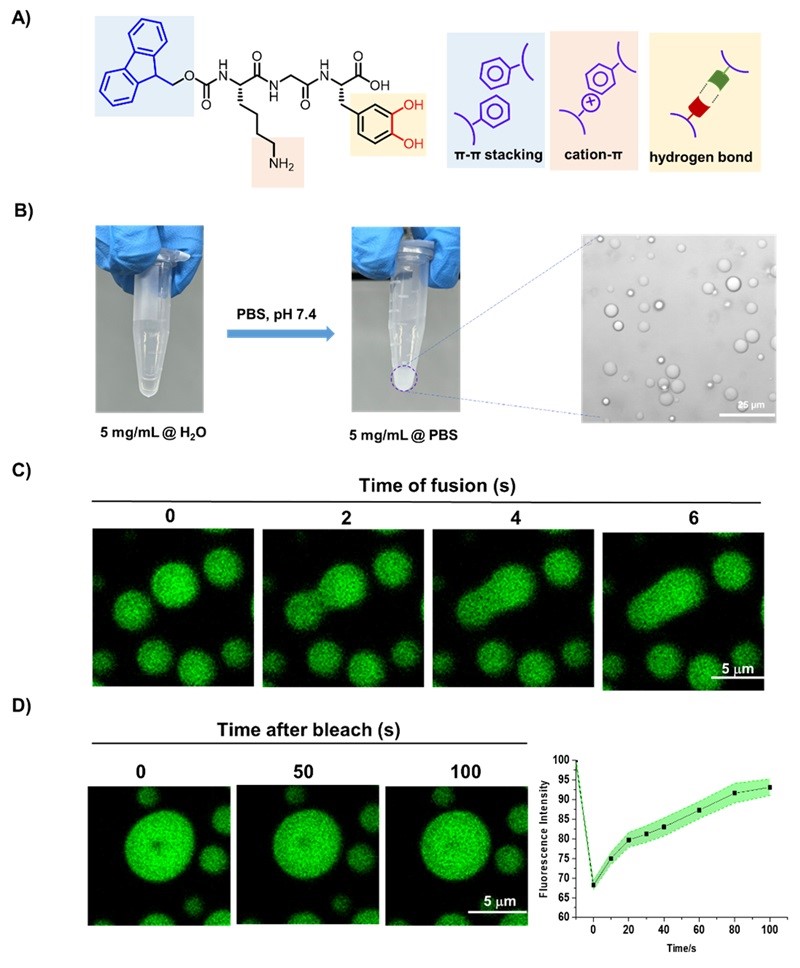
图1. 三肽(Fmoc-Lys-Gly-Dopa-OH)的相分离现象研究。图片来源:Angew. Chem. Int. Ed.
基于Fe3+与相分离多肽的相互作用,经过短暂地将多肽、蛋白分子、FeCl3以及细胞进行孵育即可将被多肽液滴募集的分子包被于细胞表面,实现有效的细胞表面工程化修饰。实验结果表明该策略可以适用不同的细胞表面工程化并且不会对细胞产生明显的毒性。
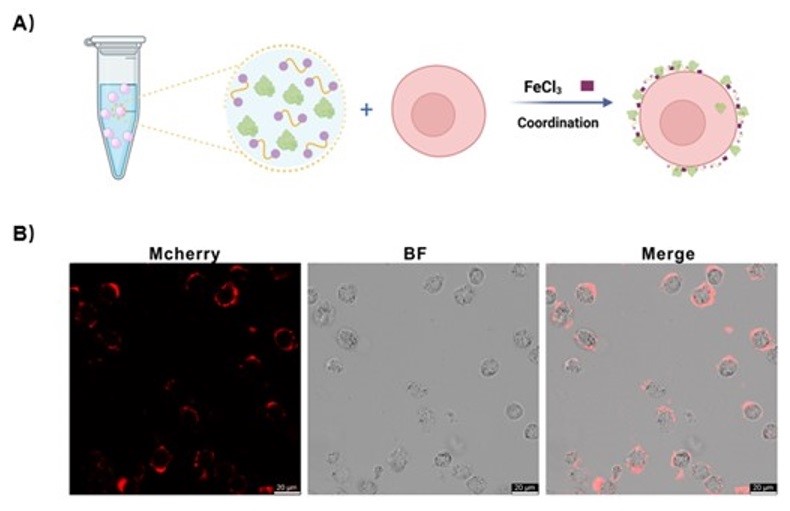
图2. 利用多肽相分离进行细胞表面工程化修饰。图片来源:Angew. Chem. Int. Ed.
最后作者利用该策略将商业化医用单抗西妥珠单抗 (Trastuzumab) 修饰在自然杀伤细胞表面,提高了自然杀伤细胞对癌细胞的靶向性,实现了对乳腺癌细胞的选择性高效杀伤。该工作表明相分离凝聚层可以作为一种新型的生物材料用于细胞表面工程化修饰并用于靶向性细胞治疗。
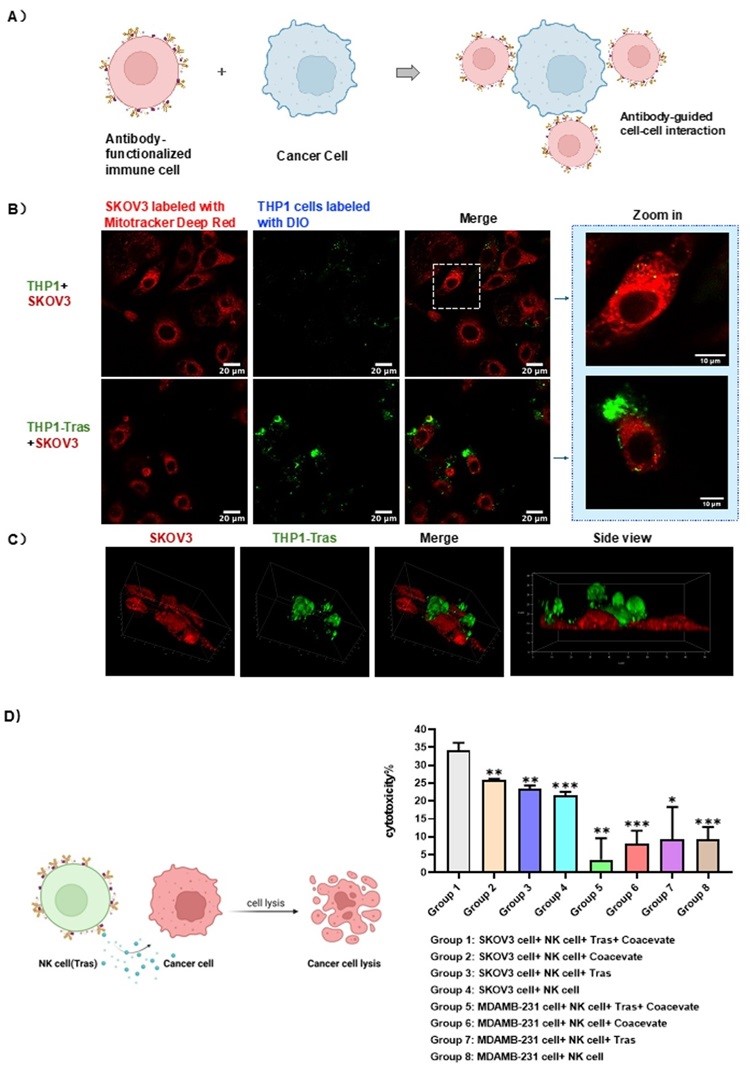
图3. NK细胞表面抗体工程化修饰及癌细胞杀伤实验。图片来源:Angew. Chem. Int. Ed.
本工作共同一作为香港中文大学化学系博士生陈红飞和鲍逸舒,通讯作者为香港中文大学化学系教授夏江。香港浸会大学曾祥泽教授提供了理论计算方面的帮助,香港大学Ryohichi Sugimura教授提供了细胞治疗方面的建议。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Cell Surface Engineering by Phase-Separated Coacervates for Antibody Display and Targeted Cancer Cell Therapy
Hongfei Chen, Yishu Bao, Xiaojing Li, Fangke Chen, Ryohichi Sugimura, Xiangze Zeng, Jiang Xia
Angew. Chem. Int. Ed., 2024, DOI: 10.1002/anie.202410566
导师介绍
夏江
https://www.x-mol.com/university/faculty/53892
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号