复旦大学刘妍君/刘宝红教授团队Chem. Biomed. Imaging | 微形貌诱导核变形触发染色质重组及细胞骨架重塑

通讯作者:刘妍君 教授,复旦大学;刘宝红 教授,复旦大学 作者:Hong Liang (梁红), Ya-Jun Wang (王亚君), Yixin Liu (柳懿芯), Wei Liu(刘伟), Baohong Liu* (刘宝红), Yan-Jun Liu* (刘妍君)
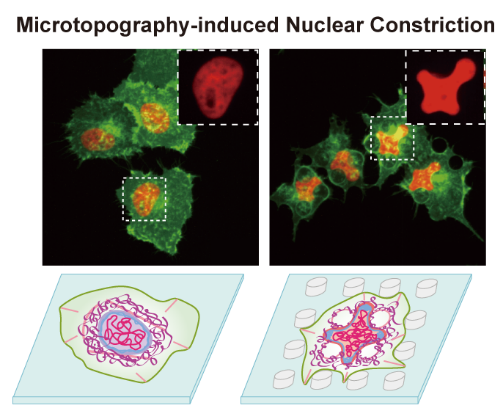
背景介绍
生物体内具有多样拓扑特征的微环境,在胚胎发育、免疫反应和肿瘤转移等生理病理过程中发挥着重要作用。目前已有研究报道,细胞能够通过接触引导(contact guidance)改变自身形态以适应拓扑基底,进而调控自身行为及命运。细胞核作为主要的遗传信息中心,能够感知并传递细胞周围的机械信号。机械环境引起的细胞核形变会改变信号转导及染色质构象进而影响细胞生存、基因稳定性和表达水平等。 细胞骨架-核骨架复合物(LINC)介导细胞骨架与细胞核之间的机械信号传递。当细胞受到机械力刺激时,细胞骨架发生重塑,并参与调控细胞核形变。然而,在限域微环境中,细胞核及细胞骨架如何协作以帮助细胞发生适应性形变有待阐明。基于此,复旦大学刘妍君/刘宝红教授团队利用微纳加工技术,设计并构建仿生限域微环境,研究细胞在机械环境中的行为变化。
文章亮点
近日,复旦大学刘妍君/刘宝红教授在Chemical & Biomedical Imaging上发表了微米级拓扑基底诱导细胞核形变并触发染色质重组及细胞骨架重塑的相关研究。研究团队基于微流控技术设计制备了不同尺寸的微柱阵列来探究限域微环境对细胞行为的影响。研究发现,微柱阵列诱导了细胞的明显形变(图1A),并导致细胞骨架的重塑(图1B)。与平面分布不同,肌动蛋白(actin)和波形蛋白(vimentin)在拓扑基底上围绕微柱分布(图1C、D)。此外,核骨架核纤层蛋白A/C(lamin A/C)在核内膜出现极化分布,在微柱引起的细胞核突起位置明显聚集(图1E)。结果表明,在适应机械环境时,细胞通过重塑细胞骨架来避免细胞核与微柱直接接触,从而保护细胞核。
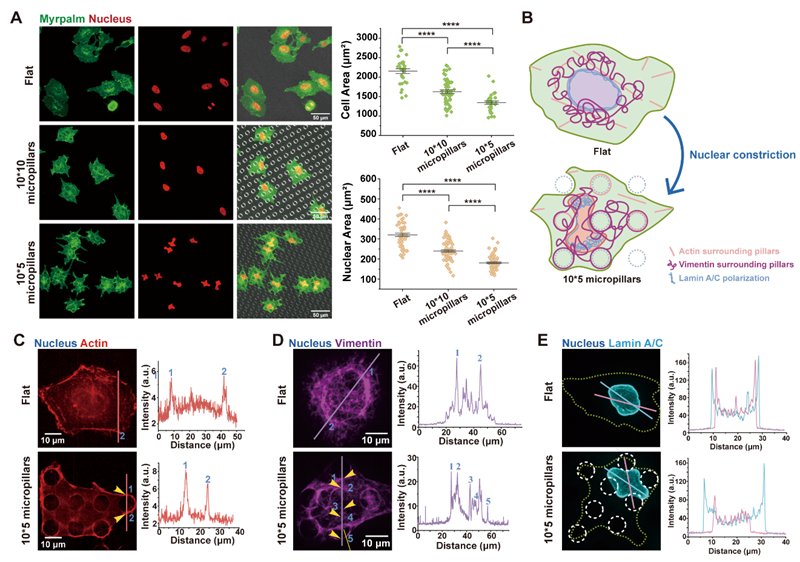
图1. 限域微柱阵列调控核形变及细胞骨架重塑
在限域微柱阵列上,细胞核内的染色质发生了显著的凝聚(图2A)。研究团队进一步探究了细胞适应拓扑基底时异染色质的表达情况。结果表明,在微柱阵列上,细胞内异染色质H3K9me3的浓缩斑面积减小,同时H3K9me3的表达水平下降(图2B-D)。此外,异染色质H3K27me3在微柱诱导变形的核突起处出现聚集分布,但其表达水平未发生变化(图2E、F)。这些结果表明,细胞适应限域微环境时能够调节异染色质的分布及表达水平。
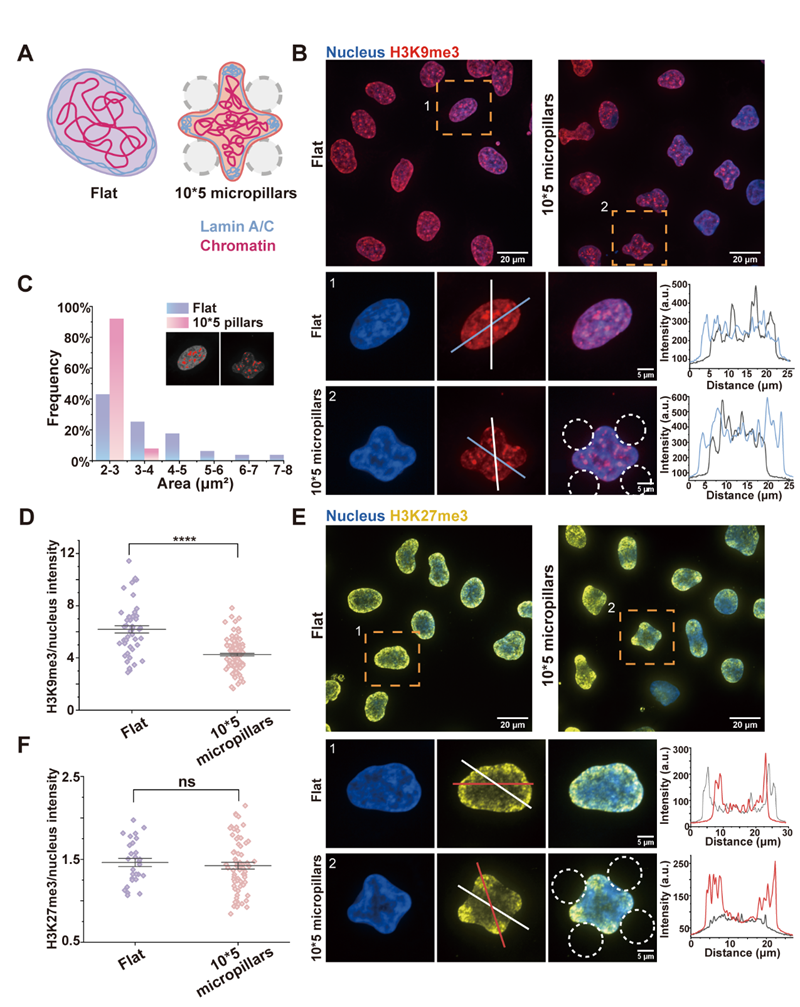
图2. 限域微柱阵列调控异染色质H3K9me3及H3K27me3重组
总结/展望 基于生物体内存在复杂的拓扑微环境,研究团队利用微纳加工技术在体外制备了微米级限域微柱阵列研究细胞的机械响应,并发现细胞核在微柱阵列中被高度束缚并发生显著形变,伴随着细胞骨架和核骨架的重塑。同时,H3K9me3和H3K27me3标记的异染色质发生重组。本研究工作强调了细胞在三维限域微环境中展现出的适应性形变,为理解机械环境对细胞行为的影响提供了新视角,并为疾病诊治提供了研究基础。 相关论文发表在高质量期刊Chemical & Biomedical Imaging上,复旦大学博士研究生梁红、博士后王亚君为文章的第一作者, 刘妍君教授和刘宝红教授为通讯作者。
通讯作者信息
刘妍君 教授

刘妍君(Yan-Jun Liu),复旦大学生物医学研究院教授、博士生导师,国际“人类前沿科学计划”青年科学家奖获得者。实验室一直致力于微流控芯片与生物医学交叉科学研究,主要开发和运用微流控芯片技术,重构体内细胞微环境;结合活细胞高分辨动态成像及细胞分子生物学方法,研究限域微环境中细胞力学响应;探讨机械力对细胞迁移、分裂等生物学行为的影响;揭示调控细胞行为的分子机制,为疾病治疗提供可行性策略。
扫描二维码阅读英文原文,或点此查看原文 Chem. Biomed. Imaging 2024, ASAP Publication Date: May 10, 2024 https://doi.org/10.1021/cbmi.4c00035 Copyright © 2024 The Authors. Co-published by Nanjing University and American Chemical Society 关于Chemical & Biomedical Imaging 所有的稿件都将经过严格的、公平的、高效的同行评审,我们致力于以期刊的文章质量赢得读者的信任。如有任何疑问,请发送电子邮件至 eic@cbmi.acs.org 点击“阅读原文”




如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!

















































 京公网安备 11010802027423号
京公网安备 11010802027423号