赵惠民教授课题组Science:不对称光酶法将氟基团引入烯烃
氟原子因其独特的电子性质和疏水性,广泛应用于有机分子特别是生物活性化合物中。氟化基团的引入可以显著增强分子的生物利用度、代谢稳定性和蛋白质相互作用。目前,约20%的药物市场产品包含氟化化合物。然而,自然界中仅有一种天然酶——5'-氟-5'-脱氧腺苷合酶(FDAS),能够将氟引入有机体,这极大限制了生物催化氟化化学的应用范围。近年来,美国伊利诺伊大学厄巴纳香槟分校(UIUC)的赵惠民教授(点击查看介绍)课题组在光酶催化领域取得了重要进展,特别是在利用光和依赖黄素单核苷酸(FMN)的烯烃还原酶驱动新型不对称转化反应方面。例如,光酶催化烯烃的不对称氢烷基化(Nature 2020, 584, 69, 点击阅读详细; Nat. Catal. 2022, 5, 586, 点击阅读详细; Nat. Chem. 2024, 16, 277)和光酶催化烯烃的不对称氢胺化(Nat. Catal. 2023, 6, 687; J. Am. Chem. Soc. 2024, 146, 10716)。在此前工作基础上,该课题组近日通过使用烯烃还原酶和传统的化学氟试剂,在光照条件下,将氟化基团不对称地引入到烯烃中。相关工作发表在近期的Science 上,先进生物能源和生物产品创新中心(CABBI)的博士后李茂霖为第一作者。


本文作者(从左至右):Wesley Harrison、苑玉杰、赵惠民、李茂霖和张郑一
具体而言,作者利用这种酶的光诱导特性生成含氟的碳自由基,然后通过酶催化的氢原子转移(HAT)过程实现高选择性的氟化基团引入。这种方法不仅拓展了酶催化氟化反应的范围,还在远离氟取代基的β、γ或δ位置上实现了高对映选择性,这是传统化学催化所难以达到的。

作者首先筛选了多种氟源,最终发现三氟碘乙烷(TFIE)在蓝光照射下,与烯烃在OYE1酶的催化下生成了具有高对映选择性的产物。通过优化反应条件,作者使用野生型OYE3酶实现了高达80%的收率和93%的对映选择性。进一步的实验显示,这种方法对多种底物具有广泛适应性,能够在多种烯烃上引入氟基团,表现出良好的收率和选择性。
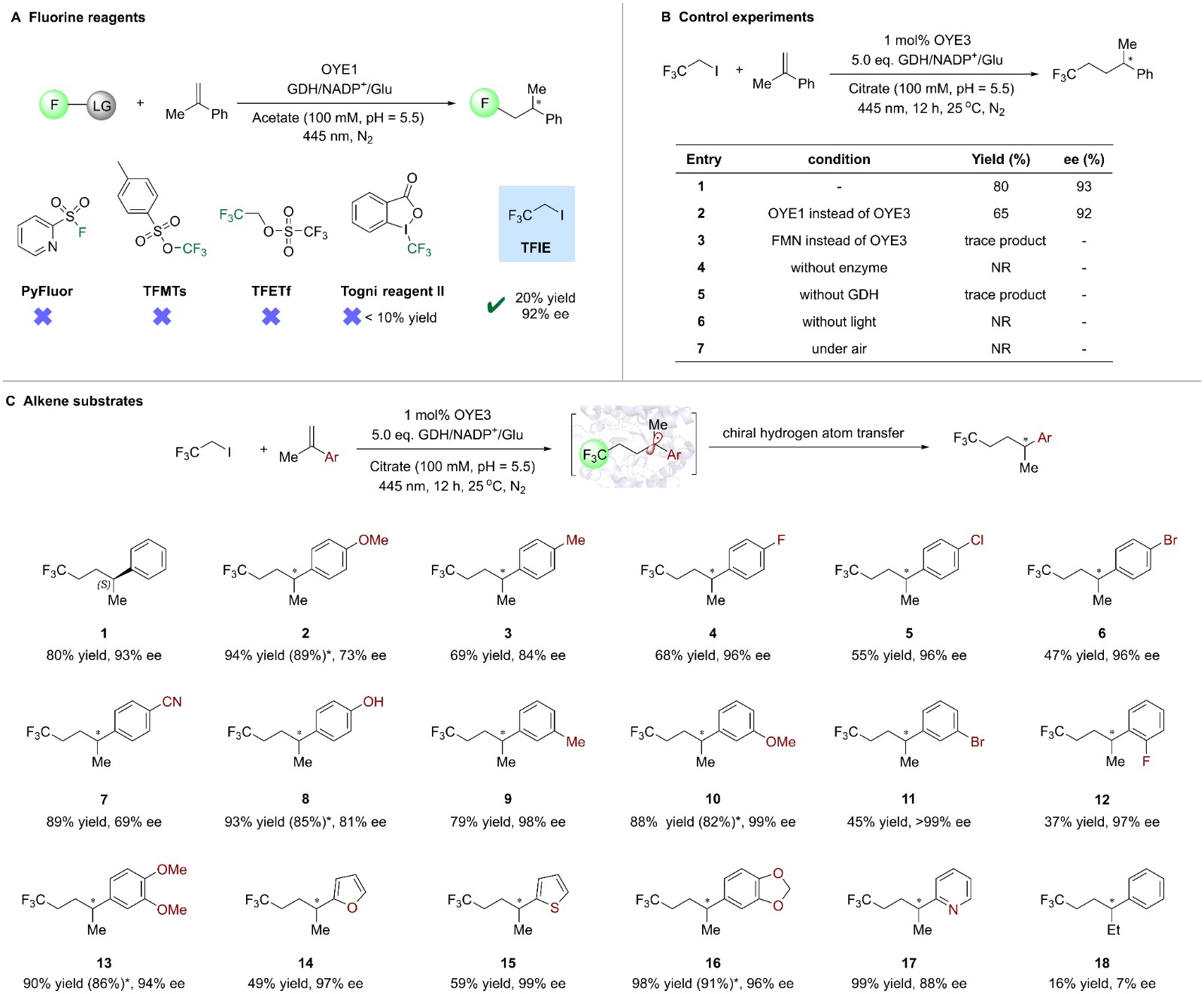
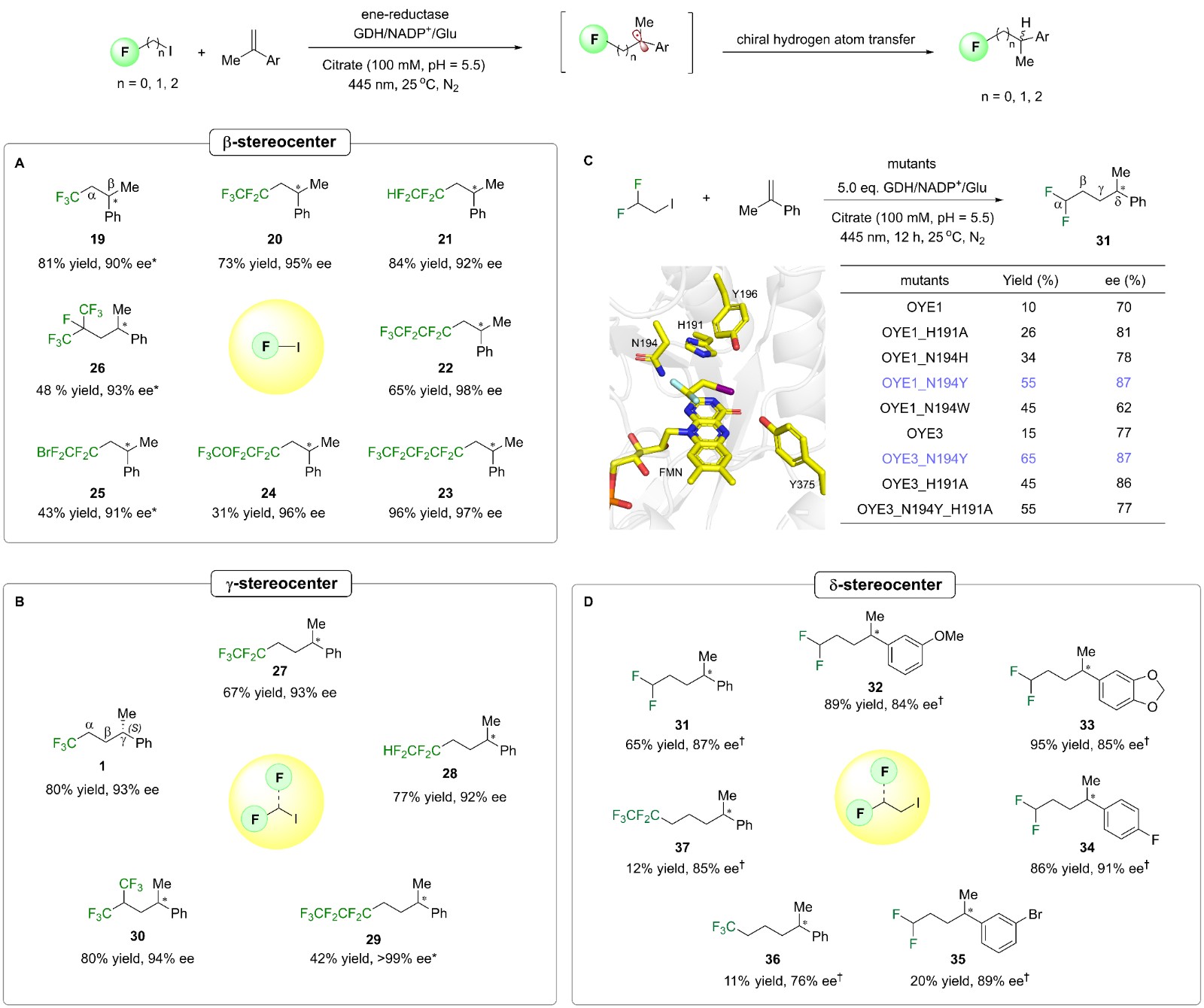
为了验证不对称光酶法在不同底物上的广泛适用性,作者进行了系统的氟试剂底物扩展实验。结果表明,该方法在多种氟试剂和底物组合中均表现出优异的效果,成功实现了远离氟取代基的β-立体中心、γ-立体中心和δ-立体中心的高对映选择性构建,展示了其广泛的应用潜力。
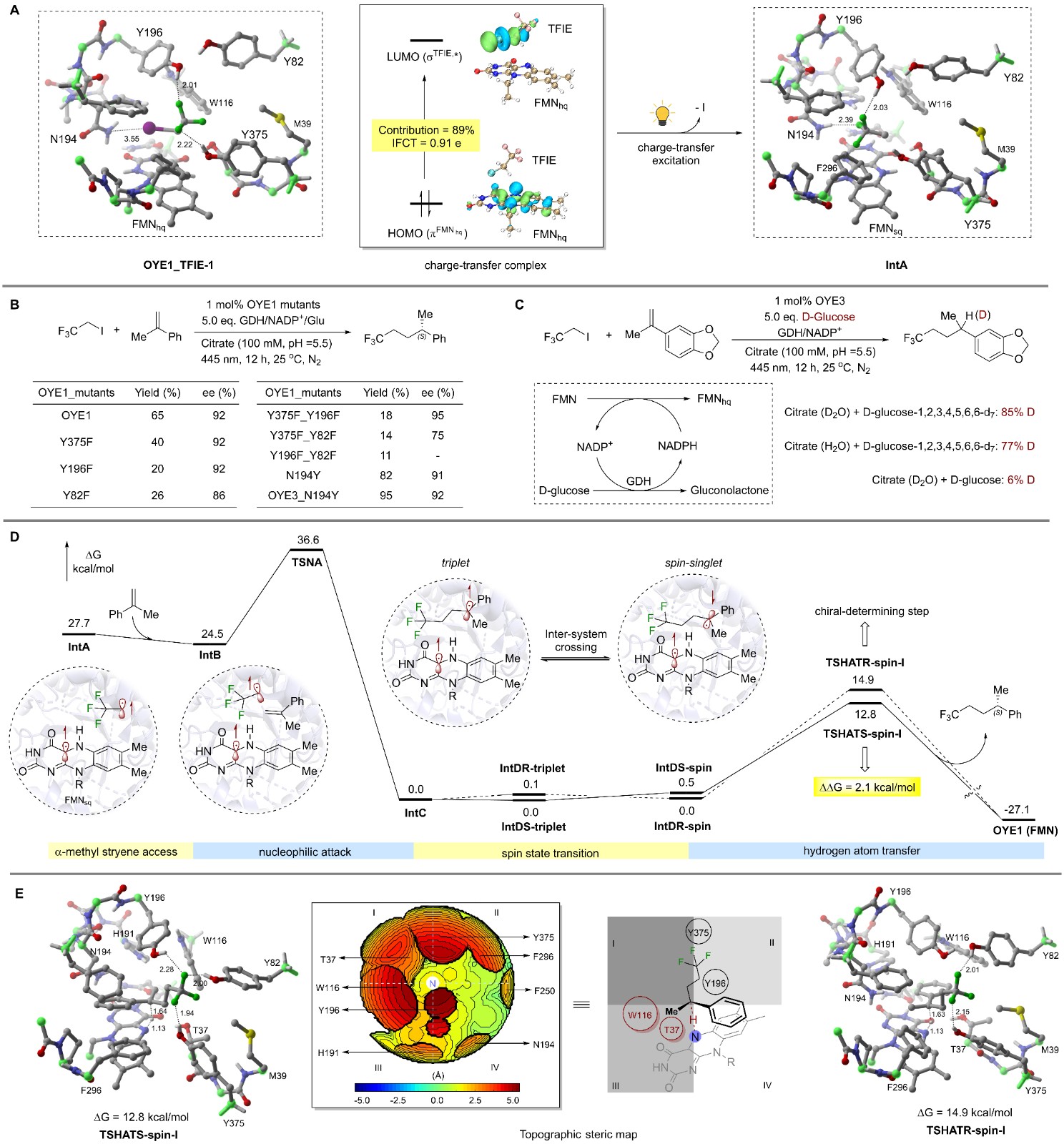
利用分子对接和量子化学簇模型的计算化学方法,作者详细解析了不对称光酶法的反应机理。首先,通过还原态的黄素单核苷酸(FMNhq)依赖的还原酶在光激发状态下引发电子转移,生成三氟乙基自由基和FMN的自由基半醌中间体(FMNsq)。量子化学簇模型结果表明,关键氨基酸残基(如酪氨酸Y196和Y375)通过氢键与氟化基团相互作用形成稳定的酶-底物复合物。氘标记实验显示,新立体中心的氢原子主要来自FMNhq。进一步的计算化学分析揭示,手性氢原子转移(HAT)过程中的R和S过渡态能量的显著差别(2.1 kcal/mol)确保了反应的高对映选择性。空间位阻分析则表明,特定氨基酸残基(如T37和W116)通过调控底物取代基的空间取向显著影响反应的立体选择性。这些发现综合解释了不对称光酶法中氟基团高效引入的分子机理。
作者的研究不仅增加了自然界利用氟的工具,还为酶-氟化学开辟了新的方向。这一创新技术有望在制药、农用化学品以及材料科学领域产生重要影响,推动高效、高选择性氟化化合物的合成。通过不对称光酶法将氟基团引入烯烃,为酶法合成手性氟化化合物提供了新的可能。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Asymmetric photoenzymatic incorporation of fluorinated motifs into olefins
Maolin Li, Yujie Yuan, Wesley Harrison, Zhengyi Zhang, Huimin Zhao*
Science, 2024, 385, 416-421, DOI: 10.1126/science.adk8464
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号