Science:DNA编码化合物库,双linker固相合成带来高纯度
近年来,DNA编码化合物库(DNA encoded libraries,DELs)技术已在制药行业内崭露头角,第一批使用DEL技术筛选发现的药物已进入临床开发后期,获批上市指日可待。DEL技术将化学合成与基因编码策略巧妙地结合起来,简单点说,就是用小片段DNA来标记小分子化合物,使得每个小分子都有独特的DNA片段标记作为“条形码”。使用者可以将靶点蛋白同时和整个库中的所有化合物进行孵育和筛选,然后通过商业化的扩增和测序技术读取能结合靶点蛋白的化合物的DNA“条形码”,就可以确定其“身份”。相比传统方法,DEL技术速度快、成本低、容量巨大(可达到千亿数量级),可快速从几千万至数十亿分子中遴选出结构新颖、具有潜在成药性的化合物,进而极大地缩短药物研究周期、降低研发成本。然而,目前DEL合成在水溶液中通过均分-混合(split-and-pool)程序进行且通常需要2-4个循环,而且所需化学结构的最终展示会随着均分和混合轮次的增加而减少,这会导致副产物截断结构的增加,纯度降低,严重地限制了基于亲和力选择的配体发现,极大影响了实际上可用的DEL库大小并限制了DEL技术的实际应用。此外,目前的DEL还无法通过分析工具评估显示产率。相比之下,液相DEL合成的一个明显替代方法是在固相载体上构建DEL(美国Scripps研究所的Sydney Brenner和 Richard Lerner于1992年提出),即肽和DNA链在同一磁珠上交替合成,并且目前已经建立了基于磁珠的DEL筛选(即使用微流体系统对编码磁珠进行筛选)。尽管如此,使用固相合成来构建容量大、纯度高并且在释放后可以进行基于亲和性选择的DEL却尚未见诸报道。
近日,瑞士苏黎世联邦理工学院(ETH Zurich)的Jörg Scheuermann教授课题组报道了一种基于磁珠的固相合成—然后自纯化释放DEL库的构建方法(图1)。每个库成员的第一个和最后一个构建砌块都通过可以相互正交化学裂解的linker连接到磁珠上;依次裂解第一个和最后一个linker并在期间进行清洗,可以确保最终库中仅包含完整的化合物,以大大提高纯度。利用这一概念,作者合成了一个三循环1100个成员的DEL,其中包含碳酸酐酶(CA)II/IX配体4-磺酰胺苯甲酸(SABA)作为11个第三循环构建砌块之一。此外,将磁珠上的高效合成与自纯化(SP)策略相结合,可以合成5种高纯度的结构单元化合物以及包括难以偶联的结构单元化合物。相关成果发表在Science 上。
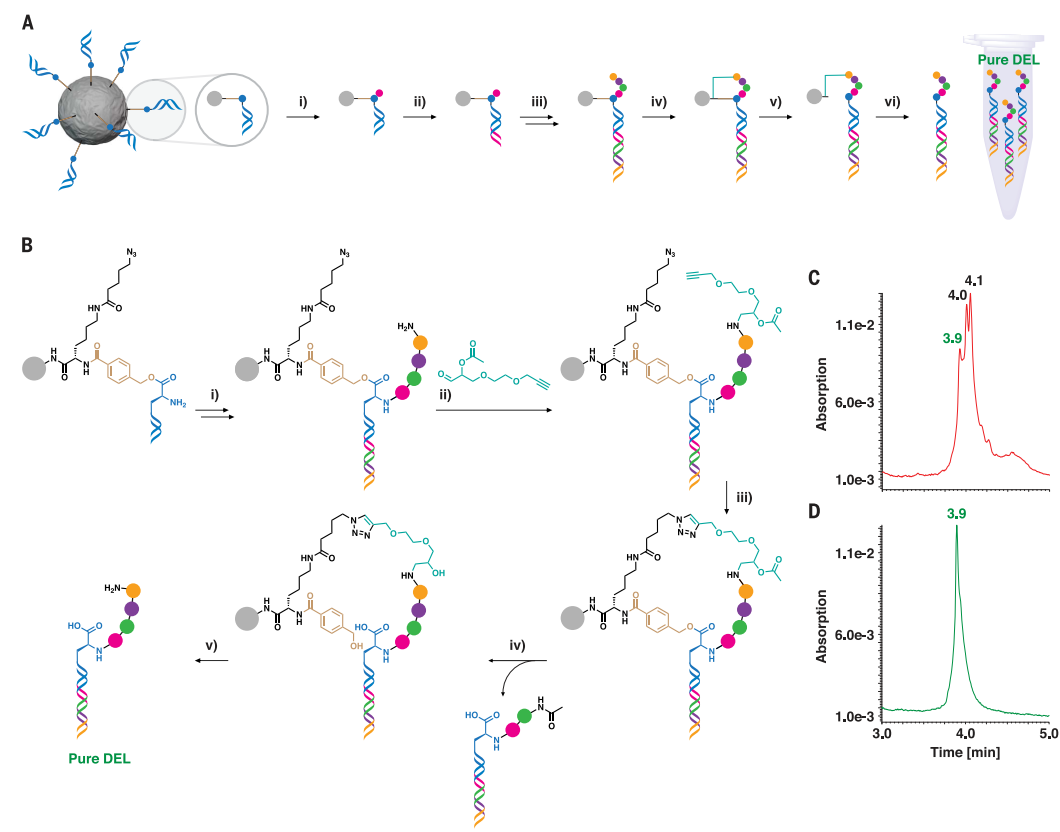
图1. 磁珠固相合成及自纯化制备DEL。图片来源:Science
首先,作者使用了基于两个正交linkers的纯化方案。如图1A所示,磁珠上SP DEL合成过程如下:三功能骨架通过第一个碱可裂解的4-羟甲基苯甲酸(HMBA)linker连接到氨基修饰的固相载体上,而其它两个官能团则分别用于连接增长的DNA条形码和化学结构。在骨架结合后,进行合成、封端和编码的均分-混合循环。接着,在最后一个化学构建砌块上安装第二个可氧化裂解的linker,从而为固相载体提供了第二个共价连接。在第一个linker裂解后,只有那些通过第二个linker附着的化合物仍然留在固相载体上,而所有封端的截短物都被释放出来并且可以被冲洗掉。在彻底清洗磁珠后,所需产物通过第二个linker的氧化裂解而释放出来。另外,作者选择了直径较小的磁珠(2 μm)作为固相载体,从而可以在可管理的体积内容纳大型库。由于处理的磁珠数量至少应与所需的库大小相匹配,因此2 μm磁珠可以轻松承受数十亿的库大小,同时仍可实现每毫升>100个磁珠携带相同的DEL成员。
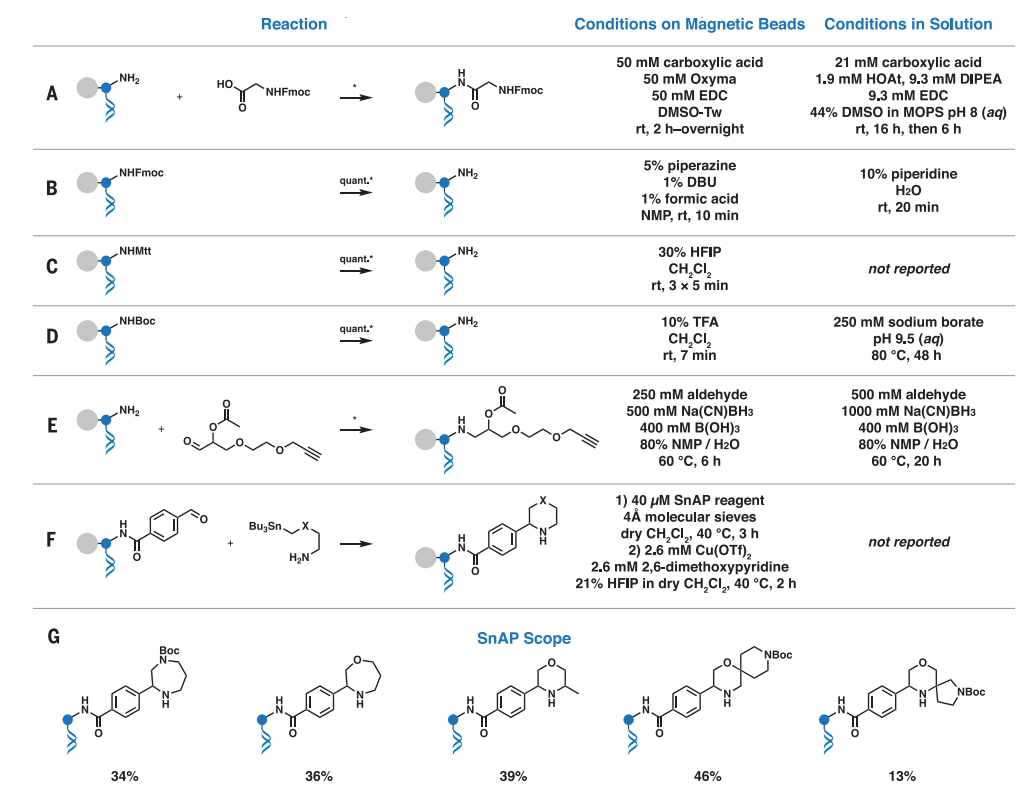
图2. 基于磁珠上固相合成的DNA相容反应。图片来源:Science
其次,为了评估固相载体的反应范围,作者测试了在溶液中为DEL合成建立的化学反应以及在水存在下无法进行的化学反应。如图2A和2B所示,作者在非质子溶剂中使用标准偶联条件以及各种天然和非天然、易偶联和难偶联的氨基酸结构单元研究了基于9-芴基甲氧基羰基(Fmoc)的固相肽合成。当使用天然氨基酸结构单元的五个反应循环时产生了两种DNA结合化合物(图3A、3B)以及三种含有难偶联的大位阻2-氨基异丁酸(Aib)单元的化合物(图3C-3E),其中化合物C中Aib被引入一次,化合物D和E中Aib被引入两次,并且Aib残基被甘氨酸隔开或连续地包含。在裂解 HMBA linker后,作者观察到所需产物与不同量的截短中间体有效释放,而通过自纯化分别释放便可得到5种纯产物。另外,固相合成方案还可进行高合成价值的无水DNA兼容转化,这在水性条件下非常具有挑战性(如:Boc和Mtt脱保护,图2C、2D)。需要指出的是,作者还在磁珠上实现了与水不相容的SnAP化学,这有望实现具有高结构多样性的杂环和螺环DELs(图2F、2G)。总之,磁珠上的DNA相容性合成可以实现各种化学转化,而基于溶液的DEL合成方案却无法实现。
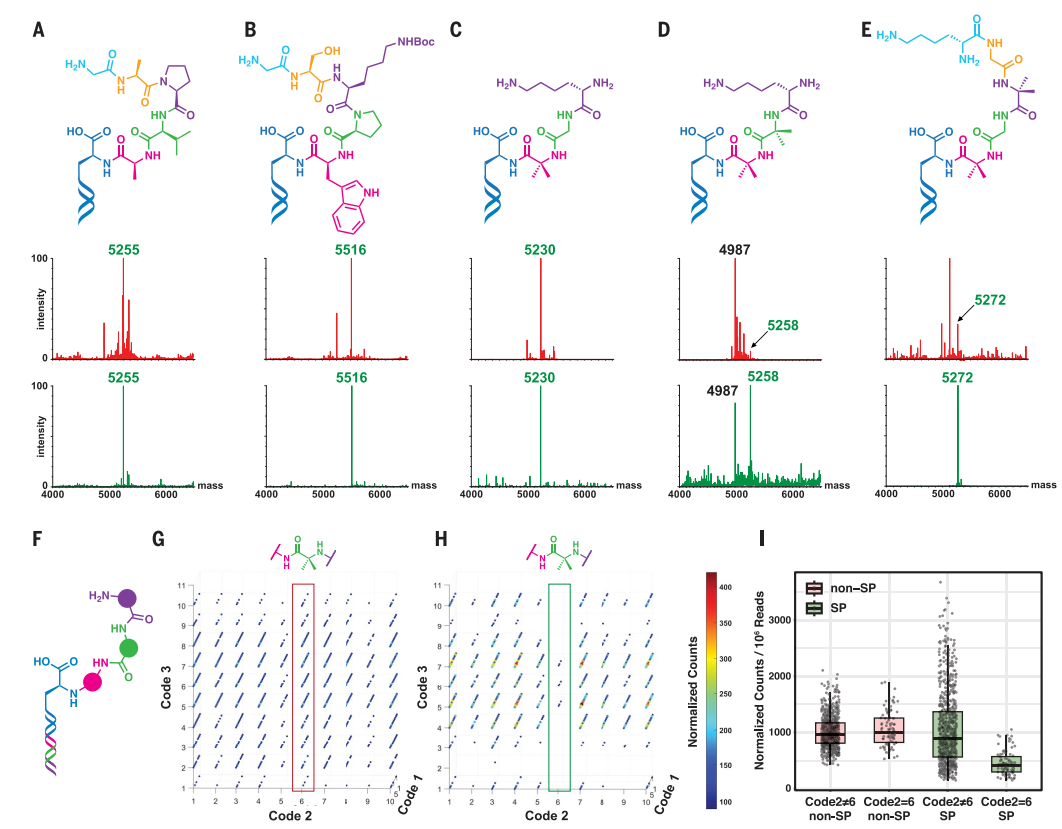
图3. 单个DNA编码化合物和DEL的自纯化。图片来源:Science
接下来,作者尝试实现合成DNA缀合物的自纯化。该策略使用两个正交可裂解的无痕linker,其中第一个linker使用了前面提到的碱可裂解的HMBA linker,而第二个linker则是Pentelute团队提出的氧化可裂解的isoseramox linker,其特点是醛能够通过还原胺化与最后一个构建砌块的游离伯氨基末端结合(图2E)。为了测试本文的two-linker设计,作者制备了由三个或五个化学构建砌块组成的单个DNA编码化合物(图3A-3E)。通过偶联Fmoc-Lys(Mtt)-OH制备氨基修饰的磁珠,然后进行Fmoc脱保护并与 HMBA linker(linker 1)结合,接着通过酯化将HMBA结合到三功能骨架Fmoc-Pra-OH上。在Mtt脱保护后,将DNA头段安装在炔丙基甘氨酸(Pra)的炔烃部分上,然后将赖氨酸的ε-氨基与5-叠氮戊酸进行偶联(图1B)。待Pra骨架的Fmoc脱保护后,通过在游离胺上添加第一个双功能化学构建砌块引发了DNA编码化合物的化学合成,然后用乙酸酐封端并进行Fmoc脱保护。反应、封端和脱保护步骤重复最多五个循环,然后通过还原胺化将linker 2安装在最终的构建砌块上。在铜催化点击偶联至叠氮戊酸修饰的赖氨酸后(图1B,step iii),linker 1与linker 2的乙酰基保护基同时被氢氧化锂水溶液裂解并产生邻氨基醇。当所有封端的截短结构都被释放并被冲洗掉时(图 1B,step iv),只有完整的产物仍然与磁珠结合并可以通过使用高碘酸盐氧化裂解释放(图1B,step v)。事实上,将自纯化应用于五种DNA编码的化合物时便可得到高纯度DNA缀合物(图3A-3E)。
随后,作者研究了由三个构建砌块(在有/无自纯化的情况下产生)组成的DEL的性能差异(图3F),其中前两组构建砌块由10 种不同的氨基酸组成,而第三个循环中使用了11种构建砌块,从而产生了1100个不同成员的DEL,这些DEL要么通过裂解HMBA linker1(非SP DEL)直接释放,要么在安装无痕linker 2、环化、linker 1裂解、清洗和linker 2裂解后通过自纯化释放(SP DEL)。另外,非SP DEL和SP DEL针对两种CA异构体进行基于亲和力的选择,未选择的(naïve) DEL以及选择输出均通过Illumina Novaseq测序进行PCR扩增和测序,并确定每个DEL成员的计数。对于naïve库,非SP DEL似乎显示所有库成员的分布更均匀(图3G),而naïve SP DEL则显示出更不均匀的分布(图3H),同时还包含那些未成功合成的库成员。
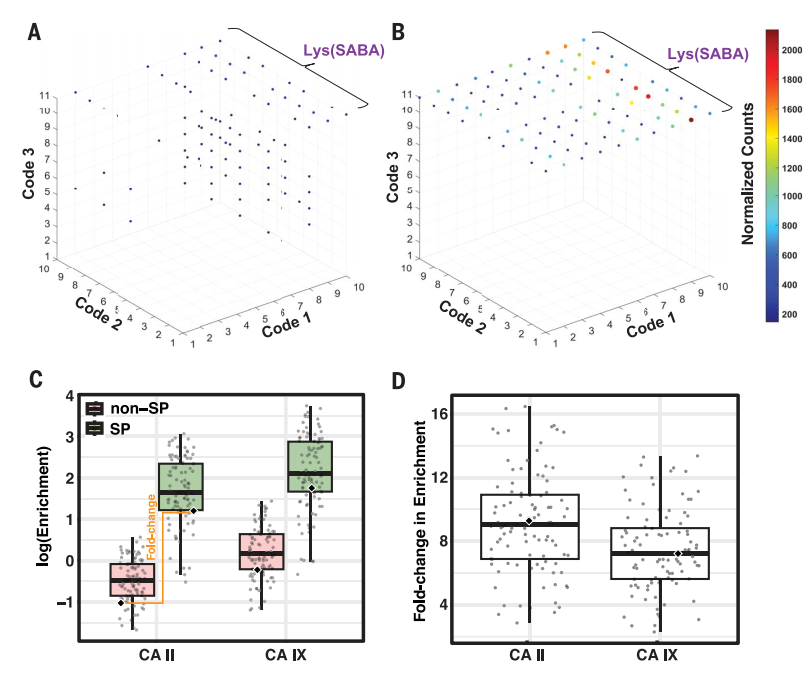
图4. 使用SP和非SP DEL进行基于亲和力的选择。图片来源:Science
当将两种DEL应用于针对CA IX的亲和力选择时(图4A、4B),自纯化对纯度的影响显而易见:尽管可以从非SP和SP DEL中检索到含有SABA构建砌块的化合物,但是在SP DEL情况下可观察到更好的富集。鉴于亲和力较低的SABA-CA II相互作用,SP DEL和非SP DEL选择之间的差异更加明显。图4C显示了在CA II和CA IX选择中使用SP(绿色)和非SP DELs(红色)的选择信号背景比(富集),其中SP DEL的平均富集率提高了8.31倍(P≪0.01;CA II为9.16倍;CA IX为7.46 倍)。通过改善DEL选择的富集率来提高信噪比,可大大促进从较大库中发现可靠配体,尤其是亲和力较低的配体(图4D)。
总结
Jörg Scheuermann课题组通过将固相合成与DEL的选择性自纯化释放相结合,为构建高纯度DEL提供了一个强有力工具。本文所提出的合成平台有望克服当前DEL技术所面临的几个主要限制性问题,可产生具有更多多样性元素(如:非天然大环)的、结构更复杂的DEL。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Highly pure DNA-encoded chemical libraries by dual-linker solid-phase synthesis
Michelle Keller, Dimitar Petrov, Andreas Gloger, Bastien Dietschi, Kilian Jobin, Timon Gradinger, Adriano Martinelli, Louise Plais, Yuichi Onda, Dario Neri, Jörg Scheuermann
Science, 2024, 384, 1259-1265, DOI: 10.1126/science.adn3412
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!













































 京公网安备 11010802027423号
京公网安备 11010802027423号