JACS:Pd催化α位选择性Michael加成芳基化反应
自从1887年Arthur Michael报道了经典的Michael加成反应后,α,β-不饱和羰基化合物作为Michael加成的π受体,被广泛应用于构建β位的碳-碳键或碳-杂原子键(图1A)。与之形成鲜明对比的是,α位选择性的Michael加成反应却鲜有报道。其主要原因,由于β位较高的亲电性,使得α位选择较为困难。目前已有报道的α位选择Michael加成反应,主要有两类策略:(1)利用底物的限制,如分子内环化反应;(2)在β位导入强吸电子基,如硝基等(图1B)。然而,此类策略均有较大的局限性,难以广泛应用于更多的复杂分子合成中。另一方面,尽管近年利用过渡金属催化α,β-不饱和羰基化合物的α氢芳基化反应被开发,并有少量报道,然而仍然存在β位选择副反应、芳基种类单一等局限。因此,开发更加具有普遍性的分子间α位选择性Michael加成反应具有很高的价值。
来自日本东京理科大学(Tokyo University of Science)的松田学則(Takanori Matsuda)教授课题组和日本福井大学(University of Fukui)的鈴木弘嗣(Hirotsugu Suzuki)助理教授合作,设想利用过渡金属对碳碳双键的配位来改变α,β-不饱和羰基化合物的电子分布,从而扭转Michael加成反应的β位选择性,实现α位选择的Michael加成反应。作者通过设计8-喹啉酰胺的α,β-不饱和羰基化合物,与Pd金属形成较为稳定的中间体,从而活化碳碳双键以扭转选择性,成功实现了分子间α位选择性Michael加成芳基化反应(图1C)。相关研究成果近期发表在Journal of the American Chemical Society 上。
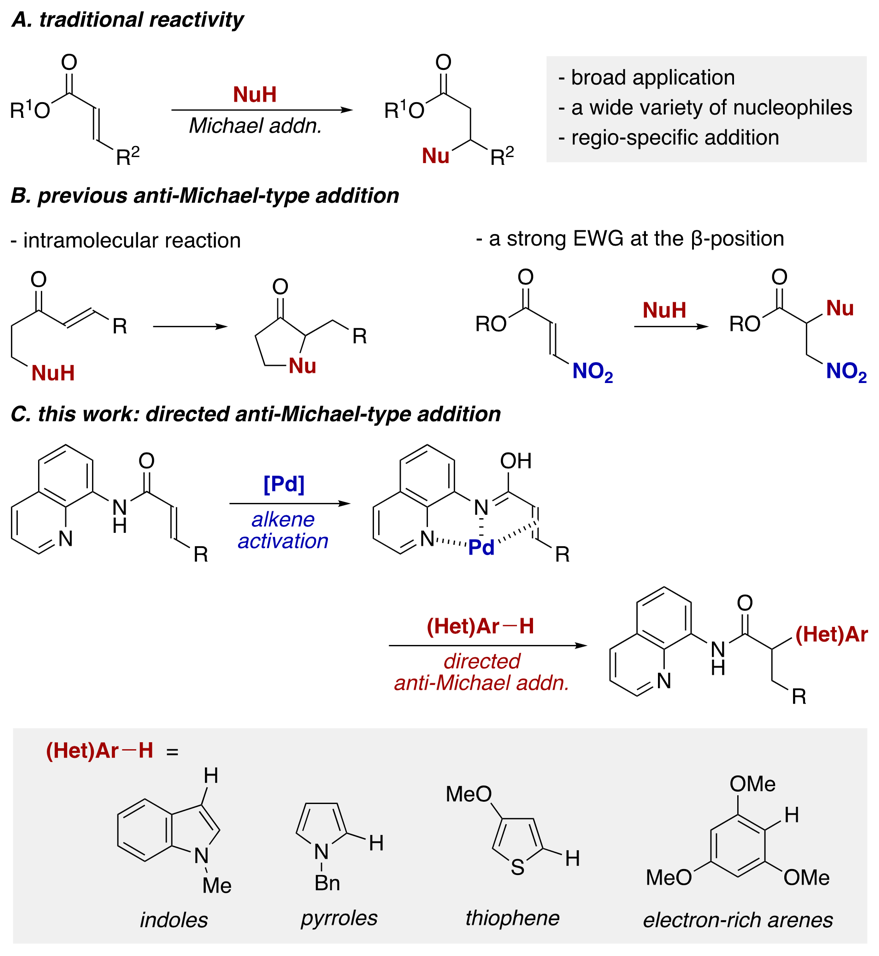
图1. 选择性Michael加成反应。图片来源:J. Am. Chem. Soc.
作者首先使用N-甲基吲哚(2a)和化合物1a作为反应物,Pd(TFA)2作为催化剂,在乙腈溶剂中120 ˚C进行反应,能够以80%产率得到α位选择的目标产物3a,而β位选择的副产物3a’则没有观测到(图2,entry 1)。通过条件筛选,最终能够以90%的分离产率得到3a(图2,entry 5)。随后,通过对比实验,无论是将化合物1a中的8-喹啉结构更换为1-萘结构(1a’,图2,entry 8),或是将酰胺结构氮上的H更换为甲基(1a”,图2,entry 9),反应均彻底停止。以上结果很好证明了1a中8-喹啉酰胺部分作为双氮配体对Pd的配位,是实现该反应的关键。
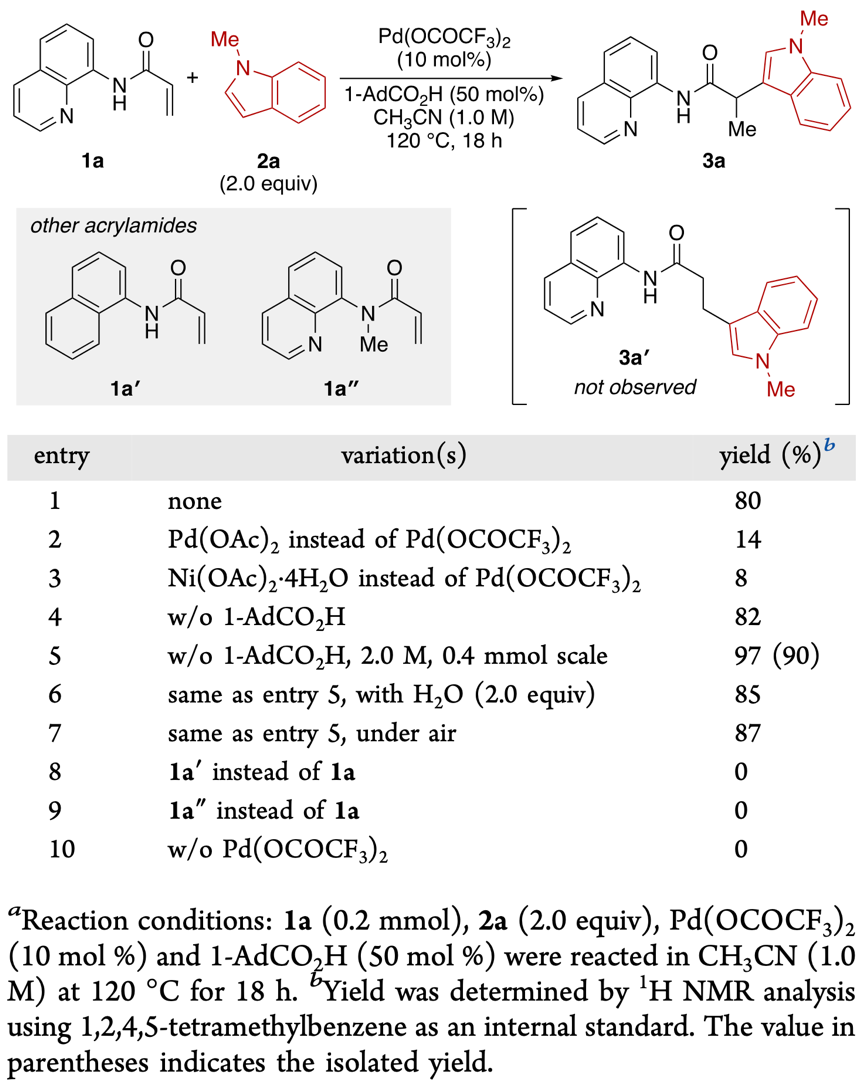
图2. 反应条件筛选与对比实验。图片来源:J. Am. Chem. Soc.
随后,作者对底物进行了拓展。如图3所示,该反应可以应用于各类吲哚衍生物,均可以较高的产率得到α位选择的目标产物(3a–s)。同时,双键端位取代的底物也可适用(3t–ag)。此外,除了吲哚衍生物,其他一些富电子的芳(杂)环也可以作为亲核试剂,实现α位选择的Michael加成芳基化反应(图4)。
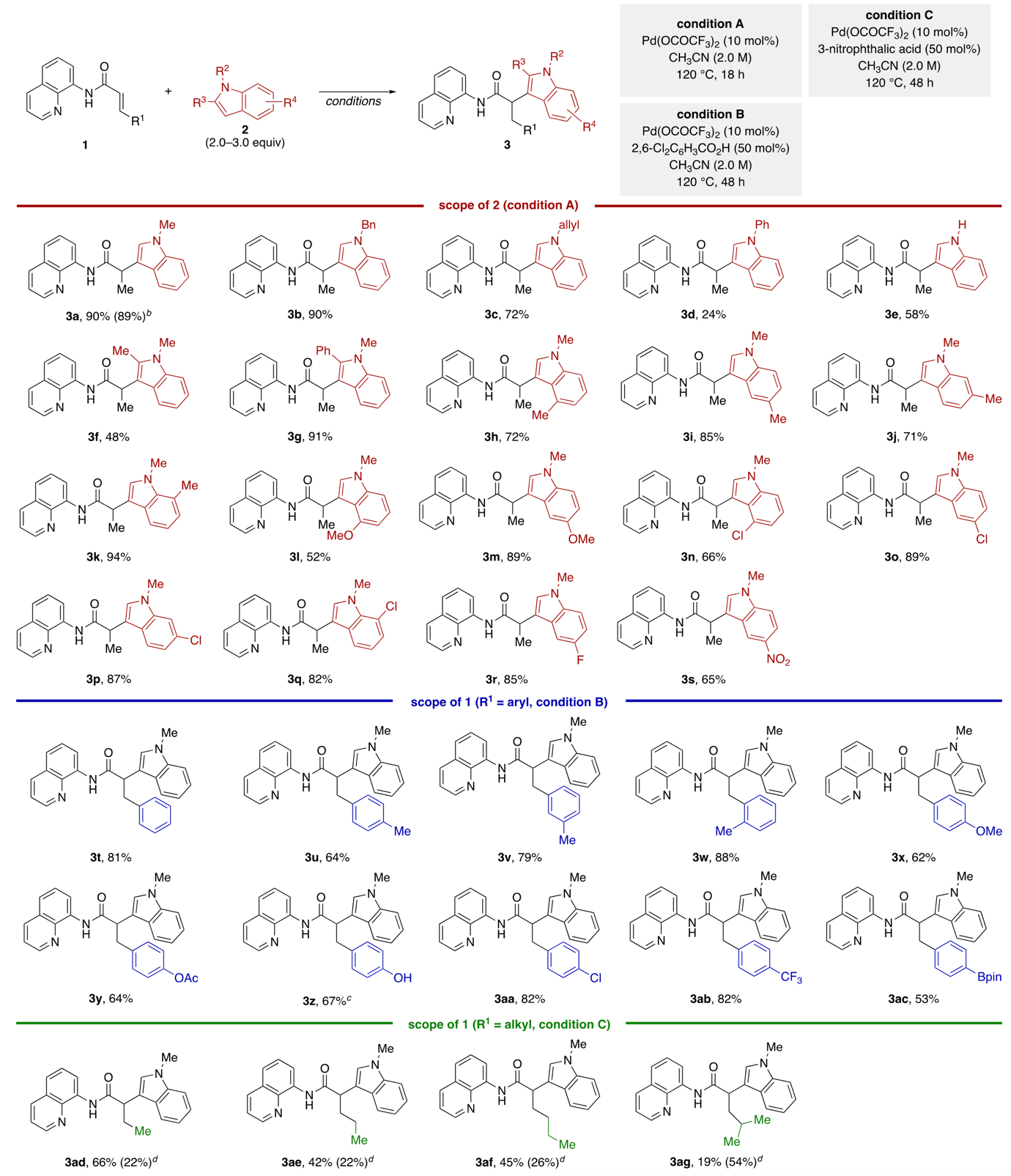
图3. 底物拓展(一)。图片来源:J. Am. Chem. Soc.
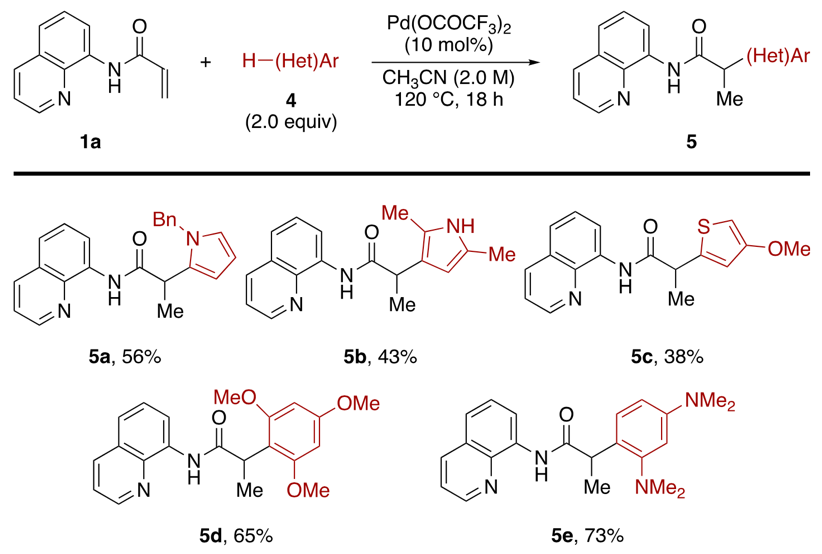
图4. 底物拓展(二)。图片来源:J. Am. Chem. Soc.
最后,为了探索反应机理,作者进行了一系列氘原子标记实验。当使用3-氘吲哚2a-d1作为原料进行反应,氘原子几乎全部在甲基上(图5A)。当使用α-氘代的α,β-不饱和羰基化合物1b-d1作为反应物时,产物3t-d1中的氘原子几乎全部停留在原位,而苄基位上完全没有氘原子(图5B)。以上结果说明了该反应中并没有β-氢消除步骤发生。最后,当使用β-氘代的α,β-不饱和羰基化合物1c-d1作为反应物时,尽管氘代比例略有减少,但产物3t-d1中的氘原子也大量保留在原位(图5C),表明了该反应中的主要步骤并非碳氢活化。
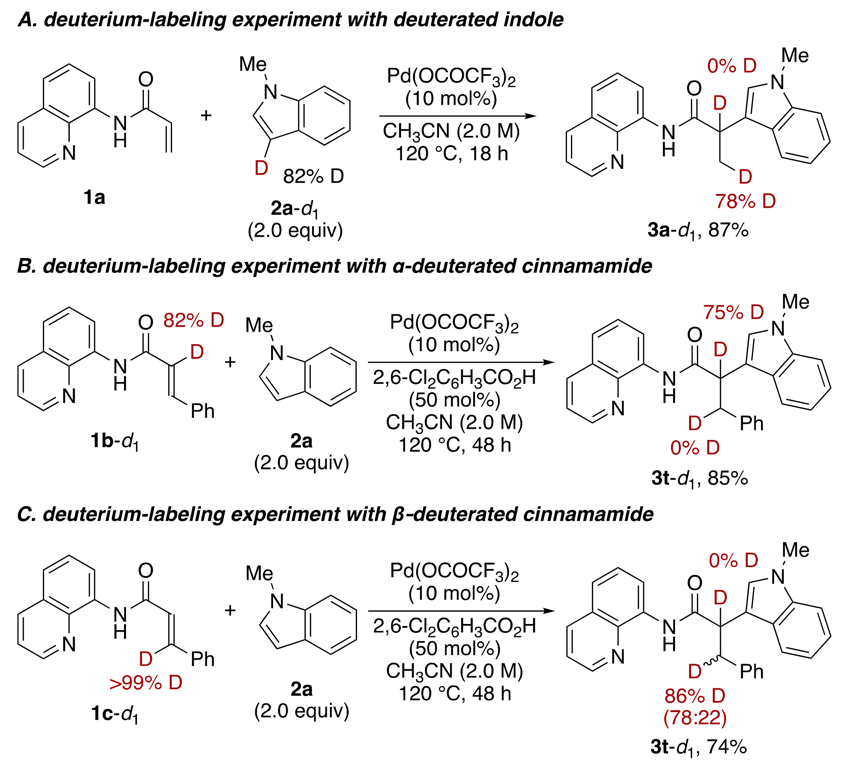
图5. 机理研究与氘标记实验。图片来源:J. Am. Chem. Soc.
基于以上结果,作者提出了该反应的机理(图6)。首先,Pd(TFA)2受1a中的双氮结构引导,对α,β-不饱和结构进行π-Lewis酸活化,形成Pd配合物B。随后,2a对B进行α位的亲核加成,形成较为稳定的含Pd的五元环结构C,可以用来解释α位选择性的由来。最后,三氟乙酸对C进行质子化,得到目标产物3a,并重新生成Pd(TFA)2进入下一个催化循环。
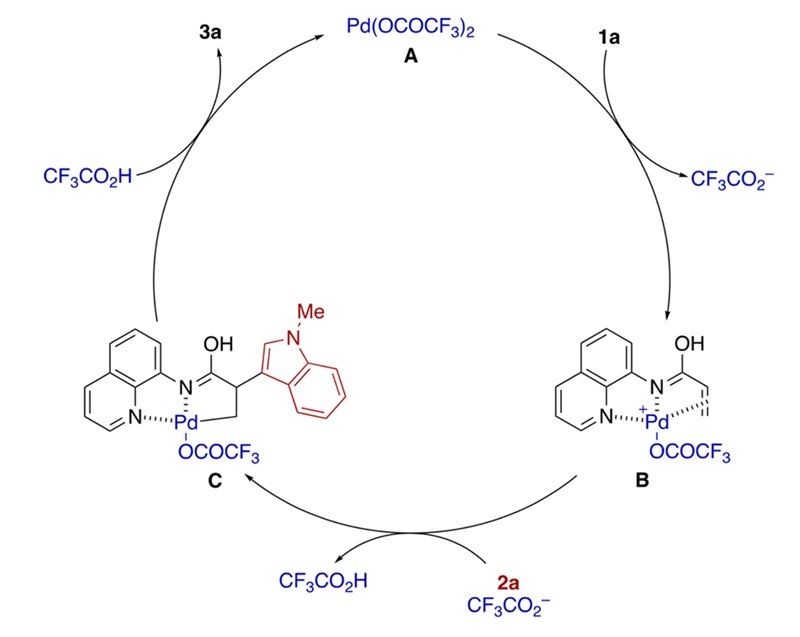
图6. 反应机理。图片来源:J. Am. Chem. Soc.
小结
松田学則(Takanori Matsuda)教授课题组和鈴木弘嗣(Hirotsugu Suzuki)助理教授合作,利用Pd对碳碳双键的π-Lewis酸活化,改变α,β-不饱和羰基化合物的电子分布,抑制Michael加成反应的β位选择性,成功实现了α位选择的Michael加成芳基化反应。相关研究成果已于近期发表在J. Am. Chem. Soc.上。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Palladium-Catalyzed anti-Michael-Type (Hetero)arylation of Acrylamides
Hirotsugu Suzuki, Ryota Moro, Takanori Matsuda
J. Am. Chem. Soc. 2024, 146, 13697–13702. DOI: 10.1021/jacs.4c00841
课题组与导师介绍
日本东京理科大学 理学部 应用化学科 松田-金 研究室(https://www.rs.tus.ac.jp/mtd/ )常年致力于有机合成、有机金属化学、过渡金属催化反应开发等相关研究。导师 松田学則(Takanori Matsuda)博士、教授,2002年于京都大学获得博士学位,2008年开始在东京理科大学任职,迄今在J. Am. Chem. Soc.、 Angew. Chem. Int. Ed. 等学术刊物上发表论文100余篇。导师 金玉树(Yushu Jin)博士、助理教授,2018年于九州大学获得博士学位,随后分别在东京工业大学、理化学研究所从事博士后研究工作,2024年开始在东京理科大学任助理教授,迄今在Science、Nat. Commun.、ChemSusChem等学术刊物上发表论文10余篇。
松田-金 研究室,所属 东京理科大学 神乐坂校区,地处国际大都市东京首都圈,饭田桥站繁华市区,生活交通便利,国际化氛围浓厚。现因研究室业务发展需求,招聘硕士、博士学生(长期有效)。
专业要求:化学专业,具有有机化学相关背景为优;勤奋刻苦,踏实肯干,具备团队精神。
语言能力:一定程度的英语会话和写作能力,有日语能力者更优。
所在地:目前已在日本的可较快办理,目前所在地为非日本地区的将协助办理签证和入学等手续。
有意者或相关咨询,请联系:金老师yushu.jin@rs.tus.ac.jp(申请者请附上简历)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号