Angew:超分子微反应器助力非生物胁迫下的ATP合成
超分子化学的快速发展使得科学家能够采用自下而上的方法,将功能和结构部分、生物或合成组分整合成集成系统,从而构建出类似细胞的人造结构(也称为“人工细胞”)。人工细胞不仅能够很好地模拟自然细胞的基本功能和行为,还能通过纳米结构工程实现更高的效率、更好的稳定性和多种复合功能。人工细胞有助于提高对复杂生命过程的理解,为生命科学研究提供了新的视角,有望在未来推动生物学和医学的发展。
非生物胁迫(如温度、光照、营养匮乏、干旱等因素)往往会诱导酶和细胞器的氧化损伤,从而阻碍叶绿体或线粒体的磷酸化过程、严重影响并降低能量三磷酸腺苷(ATP)的合成和供给。通过超分子组装手段,整合天然的功能基元和人工合成的纳米材料,精妙设计、融合组装构建超分子微反应器,有望缓解非生物胁迫损伤、实现能量的高效转化与储存。
植物常常通过激活不同的调控途径以对抗非生物胁迫,例如在面对低磷胁迫时,植物会诱导并分泌酸性磷酸酶(ACP)以提高对有机磷的利用率。受此启发,中国科学院化学研究所李峻柏研究员(点击查看介绍)团队构建了基于酸性磷酸酶的超分子微反应器,在光照和低磷胁迫条件下实现了生物能量分子ATP的高效合成。
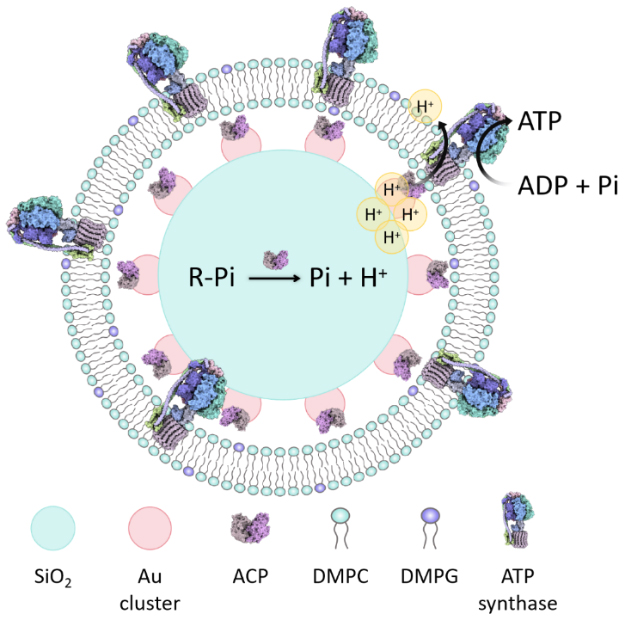
图1. 超分子微反应器结构示意图
研究表明,组装在Au纳米团簇上的ACP不仅可以催化底物产生质子流驱动ATP合成酶的旋转催化,同时还可以产生磷酸盐为ATP合成提供反应物,提高磷的可用性,以应对低磷胁迫。以抗坏血酸磷酸酯(AAP)为例,ACP催化AAP水解产生质子和磷酸盐,在脂蛋白体内外形成了质子浓度梯度势,进而驱动生物分子马达ATP合酶催化合成ATP。作者进一步将这一策略推广到其他磷酸盐(例如焦磷酸盐(P2)、三聚磷酸盐(P3)、多聚磷酸盐(Pn)),发现磷脂酶同样可以催化这些磷酸盐水解产生质子,驱动生物分子马达ATP合酶催化合成ATP。
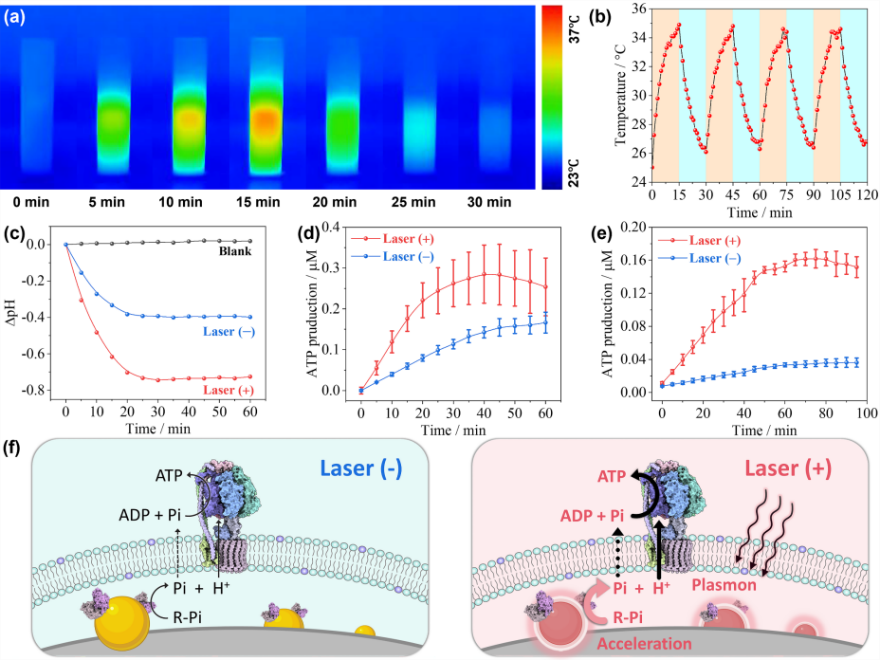
图2. 光照和低磷胁迫下的ATP合成
在光照和低磷胁迫环境下,光照下的超分子微反应器相较于无光照的体系具有更好的对抗低磷胁迫的能力。这是由于光照条件下,Au纳米团簇的光热功能加速了ACP催化反应速率,进而加速了磷酸离子的释放,为ATP合成提供了足够的底物,从而降低了低磷胁迫所带来的影响。该工作不仅实现了光诱导加速的ATP合成,同时也为设计构筑对抗非生物胁迫的生命能量合成系统提供了新的思路。
相关论文发表在Angewandte Chemie International Edition 杂志上。文章的第一作者是中国科学院化学研究所的博士研究生许阳。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Artificial Mitochondria Nanoarchitectonics via a Supramolecular Assembled Microreactor Covered by ATP Synthase
Yang Xu, Fanchen Yu, Yi Jia*, Xia Xu, Junbai Li*
Angew. Chem. Int. Ed., 2024, DOI: 10.1002/anie.202411164
导师介绍
李峻柏
https://www.x-mol.com/university/faculty/15516
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!












































 京公网安备 11010802027423号
京公网安备 11010802027423号