Nature:这个抗生素很“聪明”,只锤病菌不伤益菌
副标题:可保护肠道微生物群的革兰氏阴性选择性抗生素lolamicin
以青霉素为代表的抗生素的发现,绝对是人类对抗细菌感染的里程碑,各种类型的抗生素在数十年间挽救了无数人的生命。但细菌并非就此躺平挨锤,它们也在进化以适应并抵抗抗生素的打击,于是,各种耐药菌开始出现,甚至近年来还蹦出了几乎能够无视一切已有市售抗生素的超级细菌。病菌“魔高一尺”,人类就必须“道高一丈”,双方的斗争拉锯,至今也未分出胜负。除了会导致病菌产生耐药性甚至多重耐药性之外,抗生素的大量使用还有另外一个危害——目前大多数抗生素都没有选择性,特别是那些广谱抗生素,在杀灭病原菌的同时,也会重创我们体内的有益细菌,比如肠道中的共生菌,破坏肠道微生物群(gut microbiome),使患者更容易出现继发感染,并增加胃肠道、肾脏和血液系统异常的风险。另一方面,目前的抗生素开发也面临多重挑战,其中之一就是开发选择性针对革兰氏阴性菌的抗生素。现今绝大多数获批的抗生素只针对革兰氏阳性菌,或者同时针对革兰氏阳性菌和革兰氏阴性菌,选择性针对自我保护能力更强、危害更大的革兰氏阴性菌的抗生素寥寥无几,而且这少数几种革兰氏阴性菌抗生素也无法避免对肠道有益细菌的误伤。比如,粘菌素是目前获批的为数不多可以治疗革兰氏阴性菌感染的抗生素之一,但该药也会扰乱患者肠道微生物群,可引起与艰难梭菌(Clostridioides difficile)相关的继发感染,导致腹泻和假膜性结肠炎,这些并发症可能危及患者生命。
近日,伊利诺伊大学厄巴纳-香槟分校Paul J. Hergenrother教授课题组设计和发现了一种靶向脂蛋白转运系统的新型革兰氏阴性菌特异性抗生素lolamicin,对130多种耐多药临床分离株具有活性,在多种急性肺炎和败血症感染小鼠模型中显示出不错的疗效,并且还可保护小鼠的肠道微生物群,防止艰难梭菌的继发性感染。Lolamicin能选择性杀灭致病性革兰氏阴性菌,要归因于其靶点在致病性细菌与共生菌中的低序列同源性。这种双重选择性(在革兰氏阳性菌和革兰氏阴性菌之间选择后者,在革兰氏阴性致病菌和共生菌之间选择前者)策略,对于开发其他微生物组保护性抗生素来说是个很好的启发。相关论文发表于Nature 杂志。
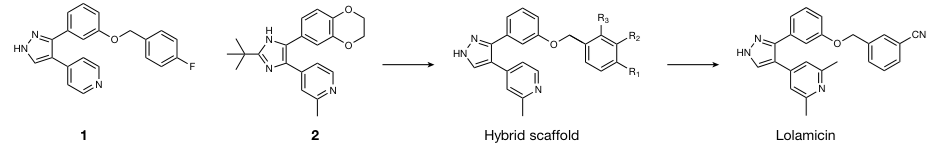
Lolamicin设计过程。图片来源:Nature
作者认为,开发一种不干扰微生物组的革兰氏阴性菌特异性抗生素的关键是寻找特异性靶点,该靶点存在于目标革兰氏阴性菌中,但与有益共生菌具有明显的同源性差异。Lol 系统就是这样的一个潜在靶点,它是一个位于革兰氏阴性菌周质内的五组分蛋白系统(LolA-E,其中LolC、D 和 E 形成 LolCDE 复合物),负责在内膜和外膜之间转运脂蛋白。革兰氏阳性菌的脂蛋白全部保留并锚定在细胞膜上,不需要脂蛋白转运,这使得Lol系统成为革兰氏阴性菌的独特“标志”。另一方面,大肠杆菌的Lol系统与人体内共生革兰氏阴性菌的Lol系统具有较低的序列同源性,因此利用该蛋白复合物作为靶点就有希望开发双重选择性抗生素——在革兰氏阳性菌和革兰氏阴性菌之间选择后者,在革兰氏阴性致病菌和共生菌之间选择前者。经过初步分析,作者选择LolCDE 抑制剂作为抗生素开发方向。2015 年阿斯利康的研究者设计了吡啶吡唑(1)和吡啶咪唑(2)类LolCDE抑制剂,虽然候选药物对野生型革兰氏阴性病原体缺乏显著的抗菌活性,且存在体内疗效欠佳、溶解性差和耐药频率高的问题,但这些化合物可通过抑制 LolCDE 复合物杀死大肠杆菌。以这两个化合物为出发点,作者重新设计了骨架,最终得到lolamicin。活性测试中,lolamicin对革兰氏阴性病原体实验室菌株(包括大肠杆菌、肺炎克雷伯菌和阴沟肠杆菌)具有显著活性,但对一系列革兰氏阳性需氧病原体以及一系列革兰氏阳性和革兰氏阴性厌氧共生菌没有明显活性(浓度在其水溶解度限之内)。这组共生菌包括拟杆菌属——人类肠道中最主要的革兰氏阴性菌。
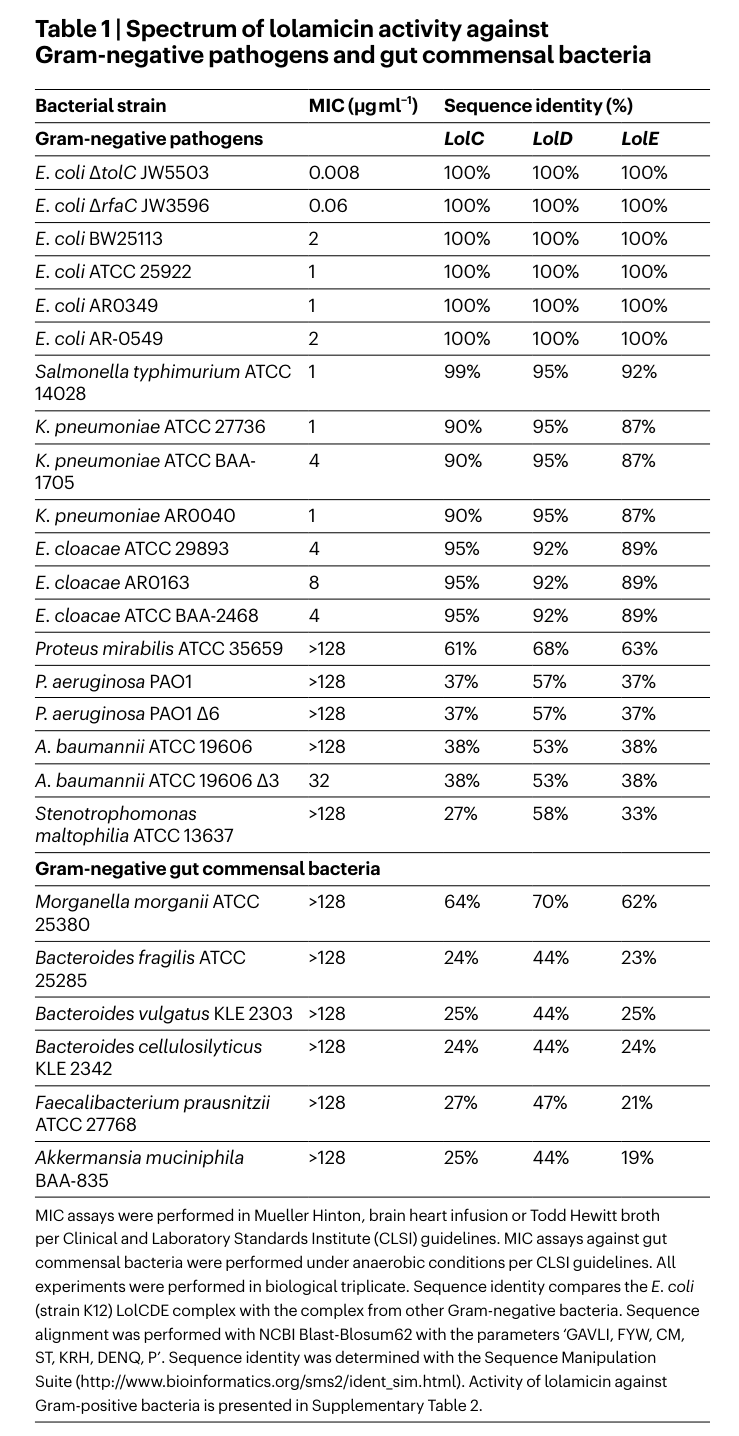
此外,lolamicin对哺乳动物细胞系和红细胞的毒性也很小。机理研究表明,lolamicin正是通过抑制脂蛋白转运途径实现了革兰氏阴性病原体的选择性灭杀。
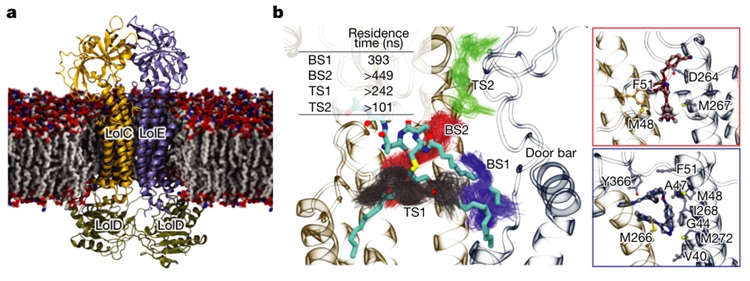
Lolamicin在LolCDE中的结合位点研究。图片来源:Nature
随后,作者进行了lolamicin的体内活性研究。小鼠接受lolamicin腹膜内注射(共3天、每天2次100 mg kg-1 ),耐受性表现良好。此外,在此剂量下进行的初步药代动力学评估表明lolamicin具有作为体内活性抗生素的潜力。接下来研究的感染模型分两种:急性肺炎感染模型用于检验细菌负担,以及败血症模型用于分析总体生存率。小鼠感染了大肠杆菌 AR0349(一种耐粘菌素的临床分离株,lolamicin的 最小抑制浓度MIC 为 1 µg ml-1,化合物 1 的 MIC 为 >32 µg ml-1),用lolamicin治疗的小鼠的细菌负担大大减少,而且败血症感染小鼠100% 成功获救。与lolamicin相比,化合物 1 在这些实验中表现欠佳。类似实验还证明了lolamicin对感染了粘菌素耐药性肺炎克雷伯菌、卡巴培南耐药性肺炎克雷伯菌和粘菌素耐药性阴沟肠杆菌的小鼠都有效。此外,药代动力学实验显示,lolamicin具有不错的口服生物利用度(F = 47%)。
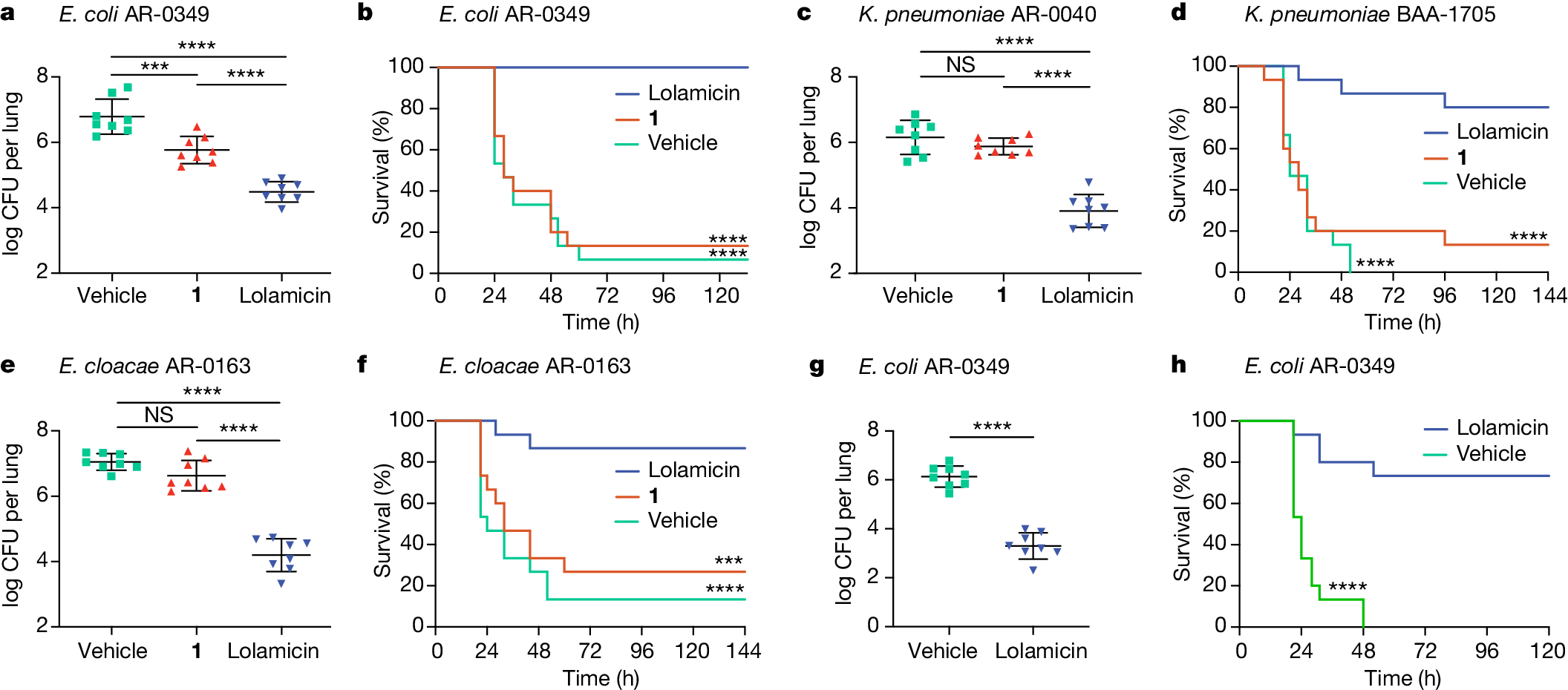
Lolamicin的体内活性研究。图片来源:Nature
接下来,作者针对lolamicin对小鼠肠道微生物群的影响进行了研究。他们从收集的小鼠粪便样本中提取 DNA,并通过全长 16S 核糖体 RNA (rRNA) 测序分析微生物组组成。作者观察到在使用阿莫西林和克林霉素后细菌种群发生了显著变化,克林霉素治疗导致芽孢杆菌和拟杆菌相对减少,而伽马变形菌明显增加。在用阿莫西林治疗的小鼠中也检测到了类似的变化,拟杆菌相对增加,而伽马变形菌富集。相比之下,lolamicin在三天治疗期间或随后的 28 天恢复期间未观察到对肠道微生物群的显著影响。作者还发现,使用lolamicin治疗的小鼠在随后的艰难梭菌攻击实验中,能够自发清除艰难梭菌病原体,这也证明了lolamicin没有干扰这些小鼠的肠道微生物组。而与之相反的是,用克林霉素或阿莫西林治疗的小鼠在相同的实验中导致了高水平的艰难梭菌定殖。
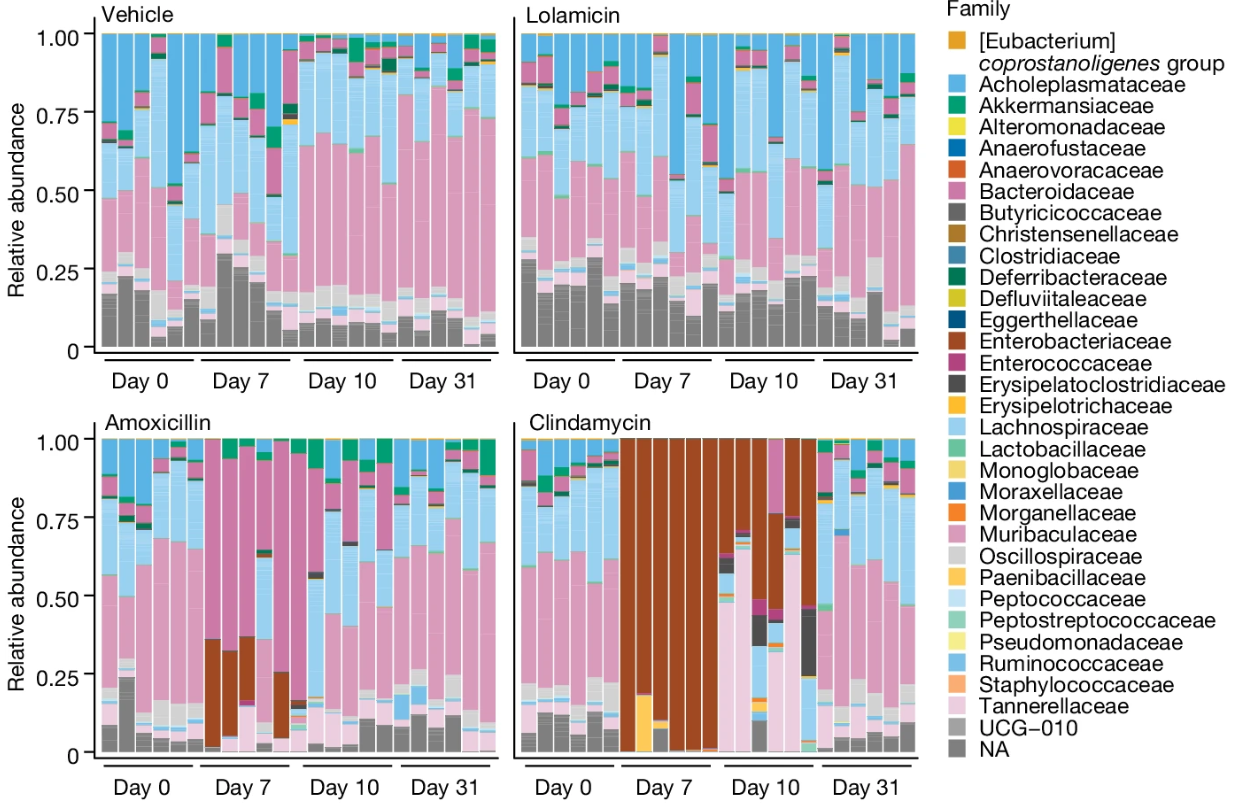
小鼠肠道微生物群研究。图片来源:Nature
总结
肠道微生物群对于维持宿主健康至关重要,其扰动可能导致许多有害影响,包括艰难梭菌感染等。Hergenrother教授课题组设计和发现了一种靶向脂蛋白转运系统的新型革兰氏阴性菌特异性抗生素lolamicin,对多重革兰氏阴性病原菌表现出良好的抗菌活性和选择性,不会杀死革兰氏阳性菌以及对人体有益的肠道共生细菌。这种双重选择性,归因于其作用靶点——脂蛋白转运系统。类似于lolamicin这样针对病原体的同时最大限度地减少对肠道微生物组损害的抗生素药物,代表了抗生素未来的发展方向。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

A Gram-negative-selective antibiotic that spares the gut microbiome
Kristen A. Muñoz, Rebecca J. Ulrich, Archit K. Vasan, Matt Sinclair, Po-Chao Wen, Jessica R. Holmes, Hyang Yeon Lee, Chien-Che Hung, Christopher J. Fields, Emad Tajkhorshid, Gee W. Lau & Paul J. Hergenrother
Nature, 2024, DOI: 10.1038/s41586-024-07502-0
(本文由北纬55°供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!

















































 京公网安备 11010802027423号
京公网安备 11010802027423号